Clear Sky Science · it
Un unico tag proteico che fa due cose: espressione solubile e purificazione dipendente dal calcio di frammenti di anticorpi a catena singola
Rendere più facile la produzione di anticorpi potenti
I farmaci moderni si basano sempre più spesso su frammenti di anticorpi—piccoli e precisi “missili guidati” in grado di riconoscere cellule tumorali, tessuti infiammati o molecole responsabili di malattie. Tuttavia questi promettenti agenti sono sorprendentemente difficili da produrre: nelle “fabbriche” batteriche tendono ad aggregarsi, a ripiegarsi in modo errato e a resistere ai metodi di purificazione standard. Questo studio descrive un nuovo elemento proteico aggiuntivo, chiamato CSQ-tag, che affronta contemporaneamente entrambi i problemi, rendendo questi frammenti più facili da produrre e purificare con un approccio semplice e a basso costo.
Perché gli anticorpi ridotti sono importanti
Gli anticorpi a grandezza naturale hanno trasformato il trattamento del cancro, delle malattie autoimmuni e dei disturbi oculari, ma la loro grandezza e struttura complessa comportano svantaggi. Possono essere lenti a eliminarsi dall’organismo, non penetrare efficacemente nei tumori o nei tessuti e risultare costosi da produrre. I frammenti variabili a catena singola, o scFv, mantengono solo la parte attiva dell’anticorpo—la porzione che riconosce il bersaglio—collegata in un’unica catena. Queste molecole compatte penetrano più facilmente nei tessuti e possono essere ingegnerizzate per terapie e diagnostiche sofisticate. Tuttavia, quando sono prodotti in batteri comuni come Escherichia coli, molti scFv si accumulano in ammassi insolubili detti corpi di inclusione, e non esiste un metodo universale e semplice per purificarli.
Un tag ausiliario due in uno
I ricercatori si sono rivolti alla calsequestrina, una proteina naturale che immagazzina calcio nelle cellule muscolari, per progettare un tag ausiliario chiamato CSQ-tag. Questo tag è insolitamente acido e altamente flessibile, con lunghe regioni disordinate che si comportano come “setole entropiche” spazzando lo spazio attorno alla proteina legata. Quando fuso a quattro diversi scFv terapeutici che normalmente aggregano, il CSQ-tag ha aumentato drasticamente la frazione rimasta solubile all’interno di ceppi standard di E. coli. Mentre gli stessi scFv con un semplice His‑tag risultavano quasi completamente insolubili, le versioni con CSQ-tag hanno raggiunto una solubilità media di circa l’84 percento—anche in un ceppo batterico che solitamente offre un ambiente chimicamente sfavorevole al corretto ripiegamento.
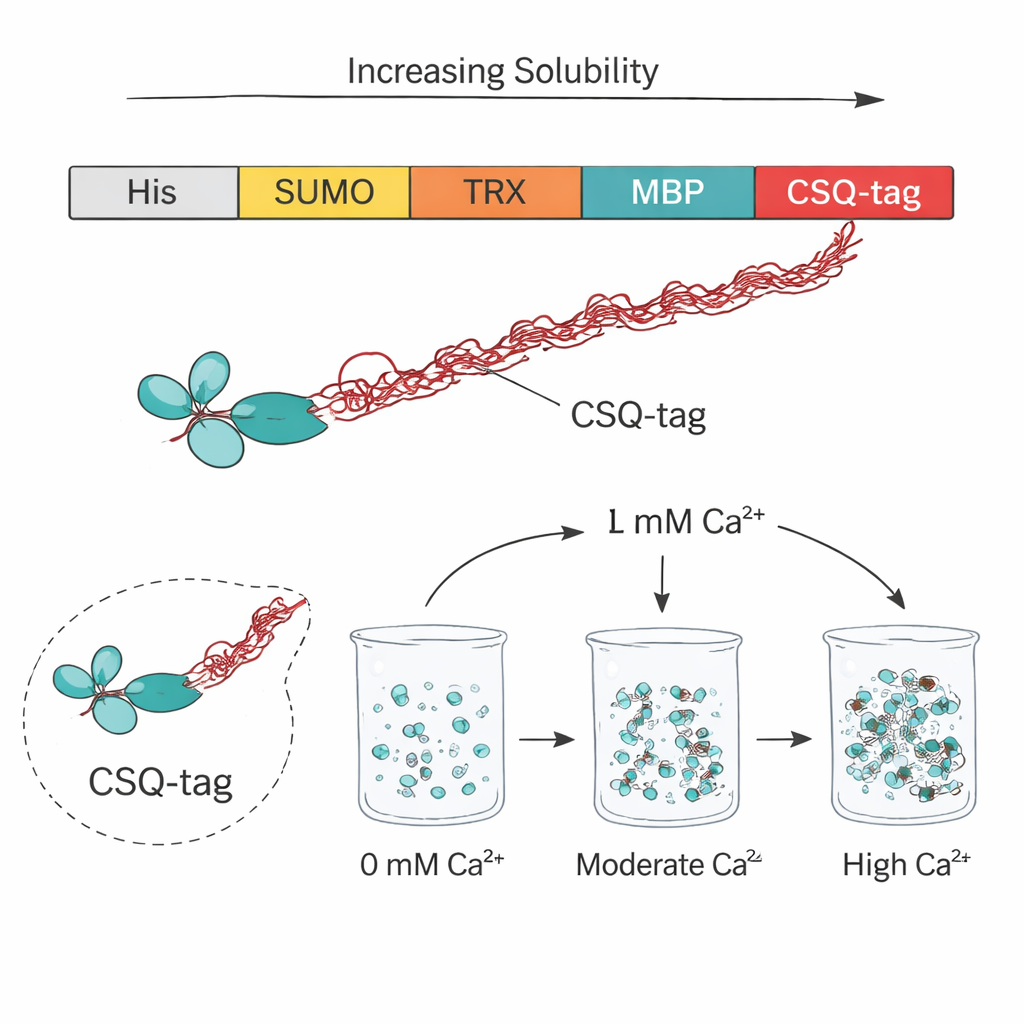
Superare le tecnologie di tag consolidate
Per confrontare le prestazioni del CSQ-tag con tag proteici popolari, il team lo ha messo a confronto con SUMO, thioredoxin, GST e MBP, spesso usati per indurre la solubilità di proteine problematiche. In questo confronto diretto con un frammento scFv anti‑VEGF (alla base del farmaco oftalmico brolucizumab), solo MBP e CSQ hanno migliorato in modo evidente la solubilità, e CSQ si è distinto nettamente. Su quattro diversi scFv, CSQ ha aumentato la produzione solubile di circa 1,8 volte rispetto a MBP, considerato a lungo una delle migliori opzioni. Ulteriori esperimenti hanno mostrato che la porzione più acida e disordinata della calsequestrina, nota come dominio 3, era cruciale per questo effetto: rimuoverla riduceva nettamente la solubilità, sottolineando come la carica negativa e la flessibilità strutturale del tag aiutino a impedire che le proteine partner si aggreghino.
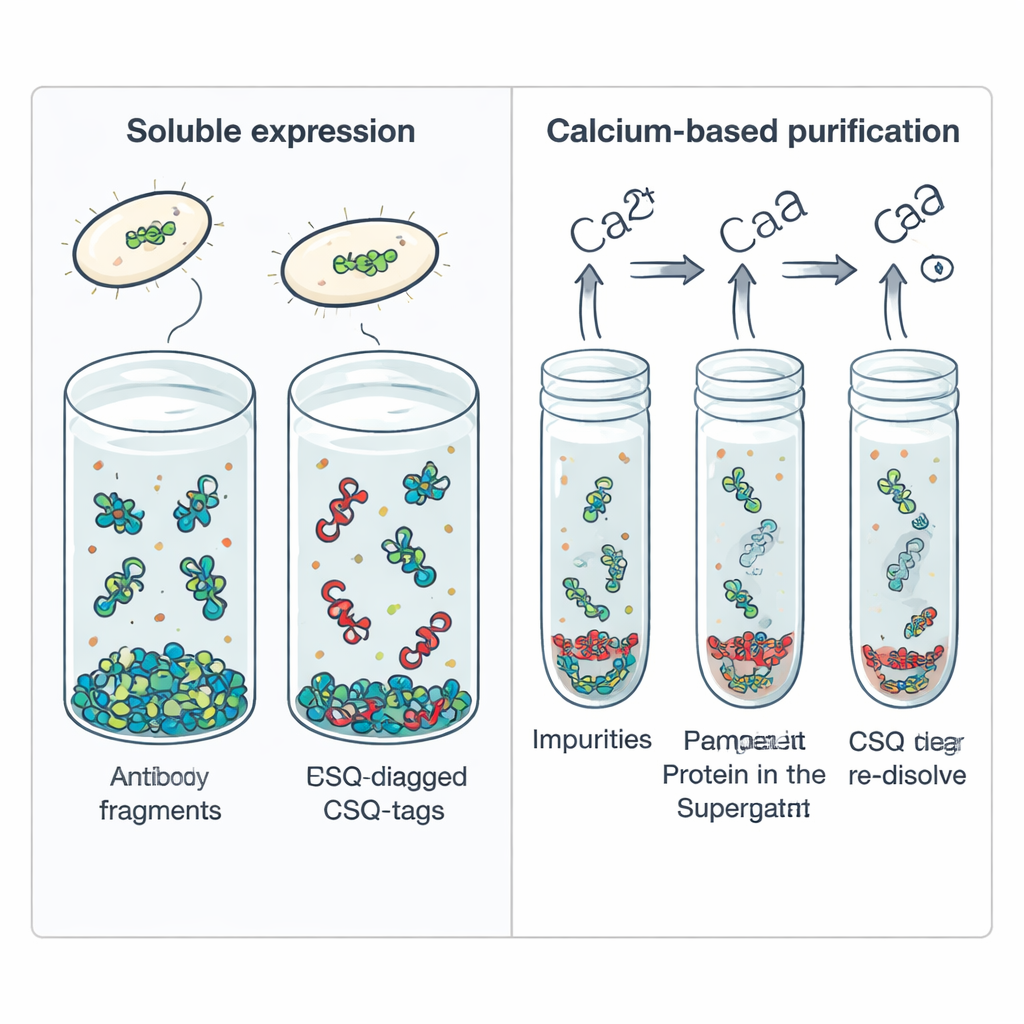
Usare il calcio come interruttore di purificazione semplice
Oltre a favorire la solubilità degli scFv, il CSQ-tag offre un trucco di purificazione integrato. La calsequestrina tende naturalmente ad aggregarsi quando lega il calcio e a disfarsi quando il calcio viene rimosso. Gli autori hanno sfruttato questo comportamento aggiungendo calcio a un estratto cellulare contenente scFv con CSQ-tag, il che ha provocato l’aggregazione delle proteine fuse taggate mentre la maggior parte dei contaminanti batterici restava in soluzione. Una breve centrifugazione ha precipitato il complesso CSQ‑tag; aggiungendo poi l’agente chelante EDTA il materiale si è nuovamente ridissolto con elevata purezza, oltre il 95 percento, senza l’uso di resine cromatografiche costose. Questa transizione di fase guidata dal calcio poteva essere ripetuta senza danneggiare la proteina, rendendola interessante per la produzione su larga scala.
Mantenere intatta la potenza del farmaco
Per qualsiasi prodotto terapeutico, aumentare la produzione conta solo se il prodotto finale mantiene la sua attività. Dopo aver rimosso il CSQ-tag con un enzima standard e aver eseguito un’ultima fase di lucidatura, il team ha testato lo scFv anti‑VEGF libero. Esso ha legato il bersaglio con un’affinità sostanzialmente identica al farmaco approvato brolucizumab, e saggi chimici dettagliati hanno confermato i legami interni corretti e l’assenza di aggregati dannosi. Un secondo scFv, particolarmente problematico, diretto al recettore CD3 ha mostrato una conservazione dell’attività simile. Le rese complessive ottenute con il processo CSQ‑tag sono state più volte superiori rispetto a quelle riportate per i metodi tradizionali di rifolding, utilizzando al contempo apparecchiature più semplici e reagenti meno costosi.
Cosa potrebbe significare per i trattamenti futuri
Combinando una migliore solubilità e una maniglia di purificazione semplice in un unico tag, il sistema CSQ affronta due colli di bottiglia di lunga data nella produzione di frammenti di anticorpi. Permette agli sviluppatori di farmaci di utilizzare ceppi di E. coli a crescita rapida e a basso costo ottenendo allo stesso tempo scFv di alta qualità che mantengono la loro capacità di legame. Sebbene siano necessari ancora alcuni aggiustamenti, in particolare per ridurre le perdite dopo la rimozione del tag, questo tag a regolazione tramite calcio potrebbe snellire la produzione non solo dei frammenti di anticorpi ma anche di altre proteine terapeutiche sensibili. Per i pazienti, ciò potrebbe tradursi in una gamma più ampia di farmaci biologici mirati, prodotti in modo più efficiente e a costi inferiori.
Citazione: Lee, J., Park, H., Jeong, S. et al. Two-in-one protein tag enables the soluble expression and calcium-dependent purification of single-chain antibody fragments. Commun Biol 9, 326 (2026). https://doi.org/10.1038/s42003-026-09611-0
Parole chiave: frammenti di anticorpi a catena singola, espressione proteica, tag calsequestrina, purificazione dipendente dal calcio, anticorpi terapeutici