Clear Sky Science · it
Il riconoscimento e il legame dei glicolipidi da parte di Siglec-6 dipendono dalle interazioni con la membrana cellulare
Come le nostre cellule distinguono amici e nemici
Il sistema immunitario sorveglia costantemente le nostre cellule, decidendo quando mantenere la calma e quando attaccare. Una parte fondamentale di questa sorveglianza è il riconoscimento di strutture zuccherine sulla superficie cellulare. Questo studio mostra che un recettore immunitario umano, chiamato Siglec-6, utilizza non solo quegli zuccheri ma anche la membrana cellulare circostante per prendere decisioni particolarmente precise sul cosa legare. Questa strategia insolita potrebbe aiutare a spiegare come il nostro corpo affina i segnali immunitari e aprire nuove strade per terapie mirate.
Un guardiano sensibile agli zuccheri sulle cellule immunitarie
I Siglec sono una famiglia di recettori presenti sulle cellule immunitarie che riconoscono zuccheri contenenti acido sialico, aiutando il sistema immunitario a distinguere il “self” dal “non-self”. La maggior parte dei Siglec si affida a un singolo elemento altamente conservato—un amminoacido arginina—per agganciarsi a questi zuccheri. Se quell’arginina viene rimossa, il legame di solito fallisce. Siglec-6, però, è un’eccezione: studi precedenti hanno mostrato che può ancora legare alcuni lipidi portatori di zucchero anche quando questa arginina chiave è mutata. Il nuovo studio si è proposto di scoprire come Siglec-6 riesca a violare questa apparente regola e cosa ciò significhi per il suo ruolo nei mastociti, nelle cellule B della memoria e nelle cellule della placenta umana.
I lipidi speciali che Siglec-6 cerca
Sulla superficie cellulare, gli zuccheri rilevanti possono essere esposti sia su proteine sia su lipidi. Questo lavoro si concentra su un gruppo di lipidi zuccherini chiamati gangliosidi, in particolare tre affini: GM1, GM2 e GM3. Tutti e tre espongono dalla membrana una singola “testa” terminata da acido sialico. Esperimenti precedenti avevano mostrato che Siglec-6 lega fortemente GM1 quando fa parte di una membrana, ma quasi per nulla GM2 o GM3, nonostante le loro teste zuccherine siano molto simili. Utilizzando simulazioni al computer dettagliate di membrane realistiche, gli autori hanno confermato che l’acido sialico in GM1 e GM3 è esposto e accessibile in egual misura. In altre parole, l’accesso fisico semplice non è ciò che conferisce a GM1 il suo status speciale. Al contrario, un zucchero aggiuntivo sulla punta di GM1—la galattosio terminale—è emerso come un elemento critico che aiuta a posizionare correttamente Siglec-6 contro la membrana.
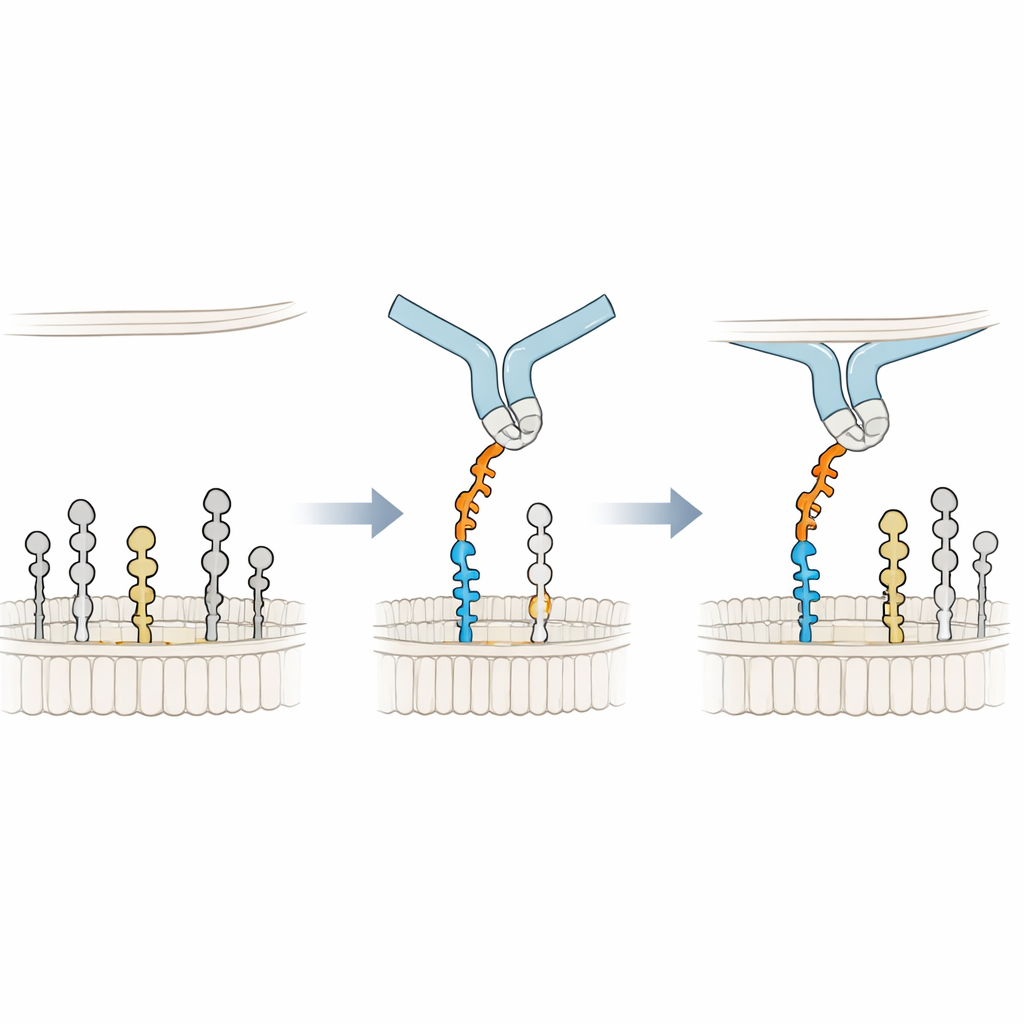
Appoggiarsi alla membrana per una presa migliore
Per comprendere il meccanismo di legame a livello atomico, i ricercatori hanno costruito modelli 3D di Siglec-6 che interagisce con GM1 in una membrana e hanno eseguito lunghe simulazioni di dinamica molecolare. Hanno scoperto che Siglec-6 continua a utilizzare la sua arginina canonica (Arg122) per contattare l’acido sialico, ma quel contatto si accende e si spegne nel tempo. Ciò che mantiene stabile il complesso è qualcosa di nuovo: un triptofano vicino (Trp127) si inserisce nella parte grassa della membrana, mentre una lisina adiacente (Lys126) interagisce con i gruppi di testa caricati dei lipidi circostanti. Questo “cuneo” nella membrana integra la consueta interazione zucchero–arginina, prendendo efficacemente energia di legame dall’ambiente lipidico. Quando la galattosio terminale di GM1 viene rimossa per mimare GM2, un’ansa flessibile di Siglec-6 occupa lo spazio vacante, tira il recettore lontano dalla membrana e interrompe questa presa assistita dalla membrana, spiegando la perdita del legame stabile.
Esperimenti che mettono alla prova il meccanismo
Il team ha quindi testato queste intuizioni computazionali in saggi cellulari e biochimici vivi. Hanno ingegnerizzato cellule per esprimere Siglec-6 normale o mutante e misurato quanto efficacemente queste cellule si legassero a liposomi fluorescenti e a piccole dischi lipidici contenenti GM1. La mutazione dell’arginina canonica riduceva solo modestamente il legame quando GM1 era nella membrana, confermando che Siglec-6 non dipende esclusivamente da questo residuo in quel contesto. Al contrario, la mutazione di Trp127 aboliva quasi completamente il legame ai liposomi contenenti GM1, e la mutazione contemporanea di Trp127 e Lys126 eliminava quasi del tutto il legame. Gli stessi mutanti, tuttavia, si legavano normalmente a zuccheri simili a GM1 presentati al di fuori di una membrana, mostrando che la struttura di base di Siglec-6 era intatta. Esperimenti di spettrometria di massa nativa rivelarono inoltre che Siglec-6 può legare non solo GM1 ma anche fosfolipidi ordinari, e che questa interazione lipidica scompare quando Trp127 è rimosso. In modo notevole, Siglec-6 si lega perfino a liposomi “nudi” privi di GM1, ancora in modo dipendente da Trp127, suggerendo che potrebbe prima sondare la membrana e poi stabilizzarsi quando incontra GM1.
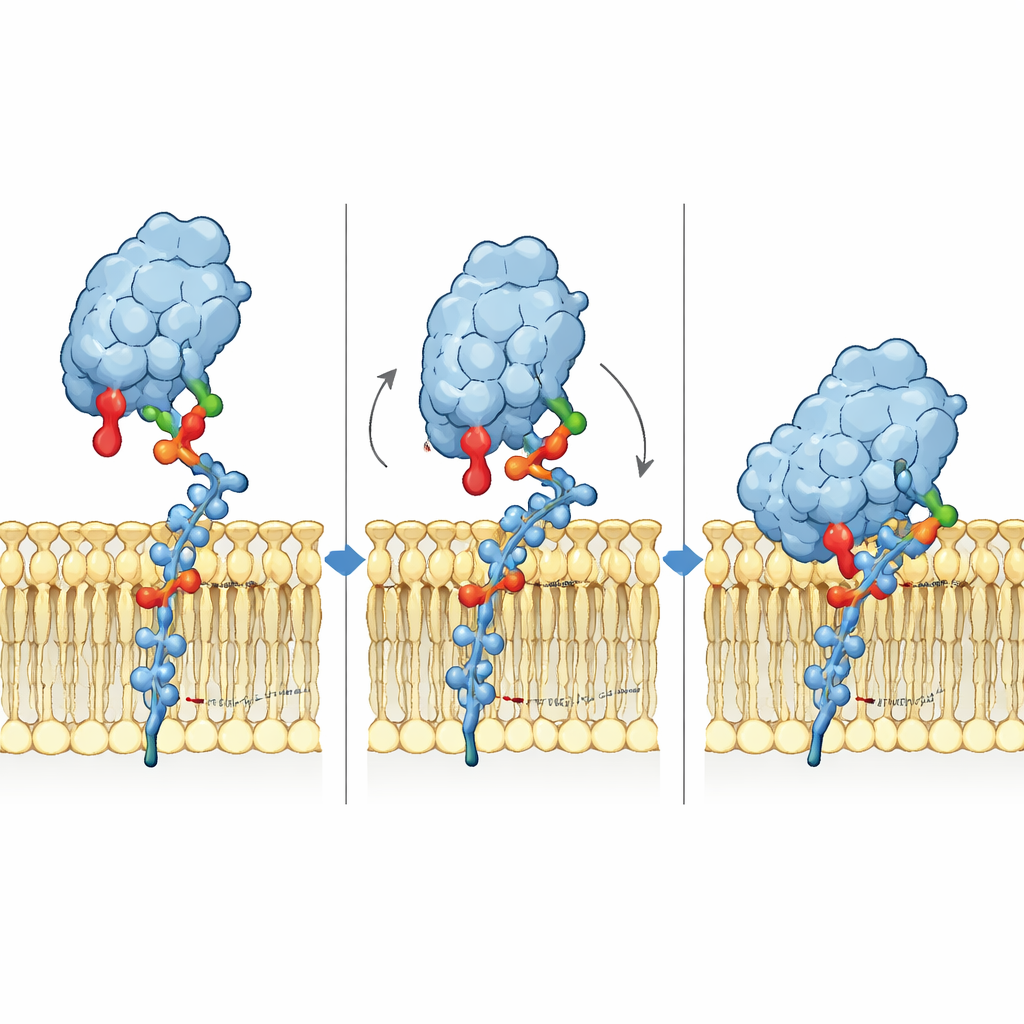
Gli zuccheri liberi raccontano una storia diversa
Quando gli stessi tre gangliosidi sono stati testati come frammenti zuccherini solubili invece che come parte di una membrana, Siglec-6 si comportava più come i suoi parenti. In soluzione, legava GM1, GM2 e GM3 con affinità deboli e simili, e ora l’arginina canonica era essenziale: mutare Arg122 riduceva nettamente il legame, mentre mutare Trp127 aveva scarso effetto. Questo contrasto mostra che Siglec-6 cambia efficacemente meccanismo a seconda che incontri zuccheri in una membrana o in forma libera. Nelle membrane, si affida a una partnership cooperativa tra la testa zuccherina, la galattosio terminale di GM1 e il contatto diretto con la membrana; in soluzione, ritorna al classico motivo di riconoscimento centrato sull’arginina.
Perché questo è importante per il controllo immunitario
Complessivamente, lo studio rivela Siglec-6 come un sensore finemente sintonizzato che sfrutta il contesto fisico della membrana per affinare la sua specificità. Ancorandosi parzialmente nei lipidi circostanti, può riconoscere selettivamente GM1 tra gangliosidi molto simili, trasformando di fatto un “lettore di acido sialico” generico in un rivelatore ad alta precisione di un particolare schema superficiale. Questa strategia assistita dalla membrana sembra unica tra i Siglec finora studiati e potrebbe aiutare Siglec-6 a scandagliare le superfici cellulari alla ricerca di specifiche firme glicolipidiche che regolano le risposte immunitarie o segnalano tessuti particolari, come la placenta umana. Comprendere questa doppia modalità di riconoscimento potrebbe agevolare la progettazione di terapie e strumenti diagnostici che sfruttino l’insolita combinazione di riconoscimento di zuccheri e membrana di Siglec-6.
Citazione: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Parole chiave: Siglec-6, gangliosidi, membrana cellulare, riconoscimento dei glicolipidi, regolazione immunitaria