Clear Sky Science · it
La destabilizzazione dell’involucro cellulare da sovraespressione di AcrAB2NodT collega la resistenza agli antibiotici alla sensibilità ai metalli in Caulobacter vibrioides
Quando combattere gli antibiotici ha un prezzo nascosto
Con la diffusione della resistenza agli antibiotici, tendiamo a immaginare i batteri semplicemente più robusti e più difficili da uccidere. Questo studio rivela una svolta sorprendente: in un comune batterio d’acqua dolce, una forma di resistenza ai farmaci rende in realtà le cellule più vulnerabili a certi metalli come rame e zinco. Comprendere questo compromesso nascosto potrebbe aprire nuove vie per riportare la bilancia a nostro favore abbinando gli antibiotici ad altri stress che sfruttano le debolezze batteriche.
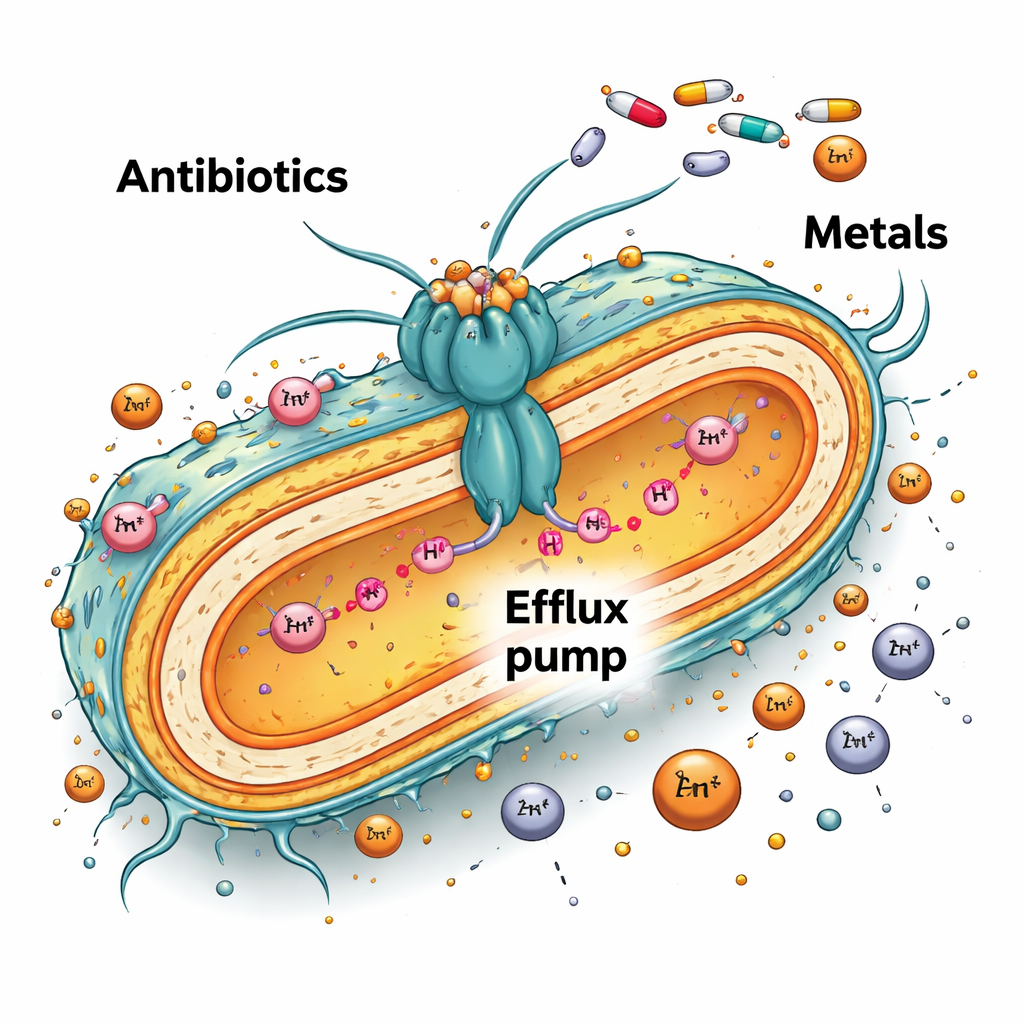
Una pompa batterica con doppio ruolo
Molti batteri si difendono usando potenti pompe molecolari che si trovano negli strati esterni e espellono composti nocivi, compresi gli antibiotici. In Caulobacter vibrioides, una di queste pompe è chiamata AcrAB2NodT. Essa attraversa le membrane interna ed esterna della cellula ed è normalmente tenuta sotto controllo da una proteina regolatrice chiamata TipR. Quando TipR è presente, la pompa viene prodotta solo quando serve. I ricercatori hanno esaminato cosa succede quando tipR viene eliminato, creando un mutante che tiene questa pompa costantemente al massimo.
Vincere contro i farmaci, perdere contro i metalli
Il mutante privo di tipR risultava effettivamente più resistente ad alcuni antibiotici beta-lattamici, confermando che la pompa iperattiva aiuta le cellule a respingere i farmaci. Ma quando il gruppo ha esposto queste cellule al rame e ad altri metalli, tra cui zinco, nichel e cadmio, il quadro si è capovolto: il mutante è diventato molto più sensibile rispetto alle cellule normali. Misurazioni accurate hanno mostrato che questa sensibilità non era dovuta al fatto che le cellule accumulassero più rame o producessero più specie reattive dell’ossigeno. Al contrario, il contenuto metallico totale all’interno del mutante rimaneva simile a quello delle cellule normali e gli indicatori standard di stress ossidativo non aumentavano. Ciò significa che la vulnerabilità doveva derivare da cambiamenti nella struttura o nella fisiologia di base della cellula, piuttosto che da un semplice sovraccarico di metalli.
Una pelle fragile e una barriera che perde
Osservando più da vicino la superficie cellulare, gli scienziati hanno utilizzato microscopi elettronici e rassegne proteiche e hanno rivelato che la sovraespressione di AcrAB2NodT altera la “pelle” batterica, nota come involucro cellulare. Le cellule mutanti mostravano rigonfiamenti, forme anomale e uno spazio ondulato e irregolare tra le membrane interna ed esterna. Le proteine coinvolte nella costruzione e nel rimodellamento dell’involucro erano più abbondanti, indicando che le cellule stavano compiendo uno sforzo costante di riparazione. Ulteriori test hanno rivelato che l’involucro del mutante era più permeabile, permettendo ai coloranti di entrare più facilmente una volta che la capacità della pompa di espellerli veniva disabilitata sperimentalmente. Quando i ricercatori hanno disattivato completamente la pompa—o eliminandone i geni o introducendo mutazioni sottili che la lasciavano presente ma per lo più inattiva—sia le strane forme cellulari sia la sensibilità ai metalli sono in gran parte scomparse, anche se alcuni componenti della pompa erano ancora presenti.
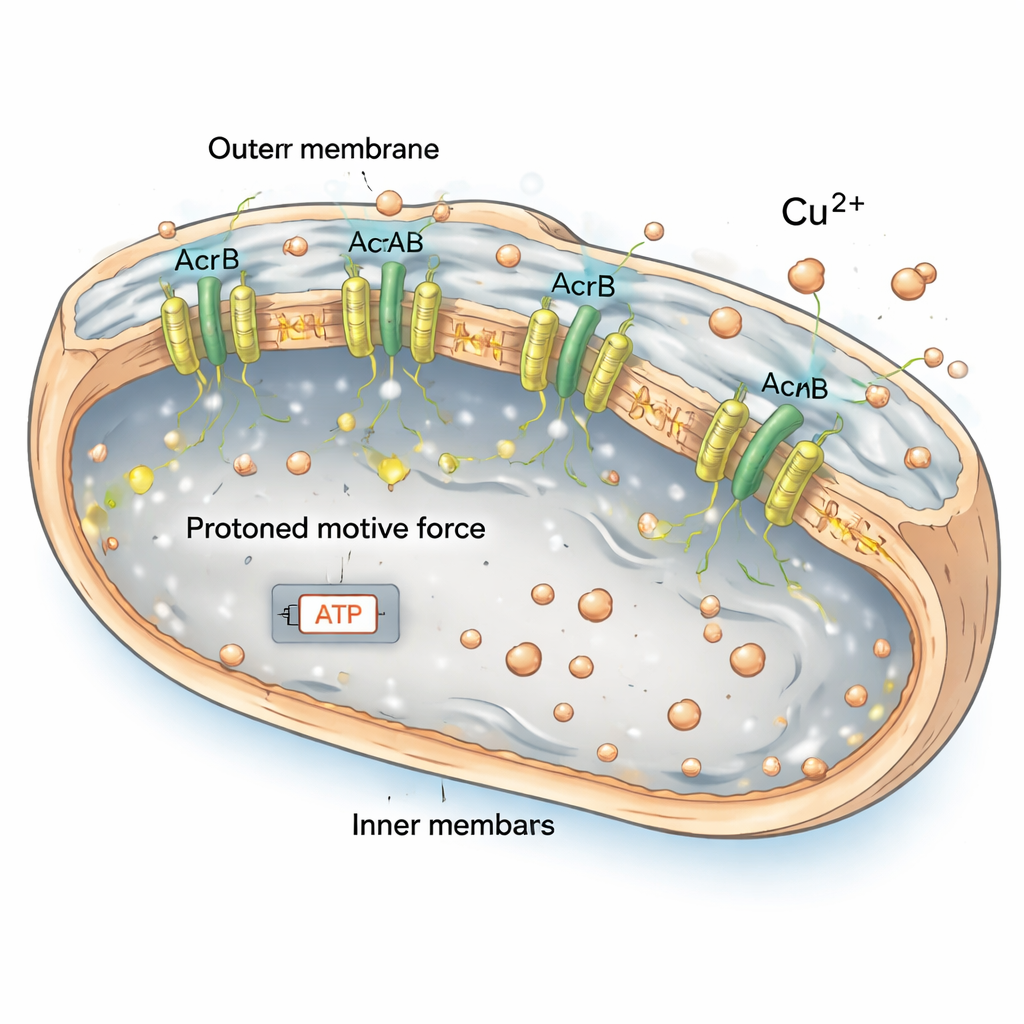
Batterie scariche e stress energetico
Le pompe di efflusso come AcrAB2NodT sono alimentate dalla forza motrice protonica, una sorta di piccola batteria creata da particelle cariche attraverso la membrana interna. Nel mutante che tiene la pompa sempre in funzione, questa batteria era in parte scaricata: un colorante che segnala la differenza di potenziale della membrana ha mostrato un segnale più debole e le cellule avevano livelli più bassi di ATP, la loro principale valuta energetica. I batteri hanno cercato di compensare aumentando le vie che producono energia, come quelle coinvolte nella degradazione degli acidi grassi, ma ciò non è stato sufficiente a evitare una carenza energetica complessiva. Quando i ricercatori hanno chimicamente compromesso il gradiente di protoni in cellule altrimenti normali, quelle cellule hanno cominciato a somigliare al mutante nel modo in cui gestivano male il rame. Ciò suggerisce con forza che la combinazione di un involucro indebolito e di energia cronicamente bassa rende i batteri che sovraproducono la pompa particolarmente vulnerabili allo stress metallico.
Trasformare una debolezza in una strategia terapeutica
Per i non specialisti, il messaggio chiave è che la resistenza agli antibiotici può avere un costo: i batteri possono sopravvivere meglio ai farmaci ma diventare più fragili sotto altri aspetti. In Caulobacter, tenere costantemente in funzione una potente pompa antidrug mette a dura prova gli strati esterni e le riserve energetiche della cellula, lasciandola meno capace di sopportare metalli come il rame. Questo compromesso suggerisce nuove idee terapeutiche. Se debolezze simili esistono nei batteri patogeni, i medici potrebbero aumentare l’efficacia degli antibiotici abbinandoli a metalli o ad altri agenti che sfruttano il carico energetico e strutturale dei meccanismi di resistenza, spingendo i microrganismi resistenti oltre il loro punto di rottura.
Citazione: Ote, M., Lardinois, L., Hendrickx, E. et al. Envelope destabilization by AcrAB2NodT overexpression links antibiotic resistance to metal sensitivity in Caulobacter vibrioides. Commun Biol 9, 313 (2026). https://doi.org/10.1038/s42003-026-09606-x
Parole chiave: resistenza agli antibiotici, pompe di efflusso, suscettibilità al rame, involucro batterico, metabolismo energetico