Clear Sky Science · it
Analisi integrata di GWAS e molQTLs rivela varianti genetiche specifiche delle cellule nel sistema immunitario suino
Perché l’immunità dei maiali ci riguarda tutti
I maiali contribuiscono a nutrire gran parte del mondo e fungono anche da importanti modelli per la ricerca medica umana. Eppure le malattie infettive nei suini costano agli allevatori miliardi di dollari ogni anno e portano a un uso intensivo di antibiotici. Questo studio pone una domanda semplice ma potente: come delle piccole differenze nel DNA influenzano il funzionamento delle cellule immunitarie dei suini, e possiamo rintracciare quegli effetti fino al comportamento di singoli tipi cellulari nel sangue? Comprendere quella catena di cause ed effetti potrebbe guidare la selezione per greggi più sani e offrire indizi sul funzionamento del nostro sistema immunitario.
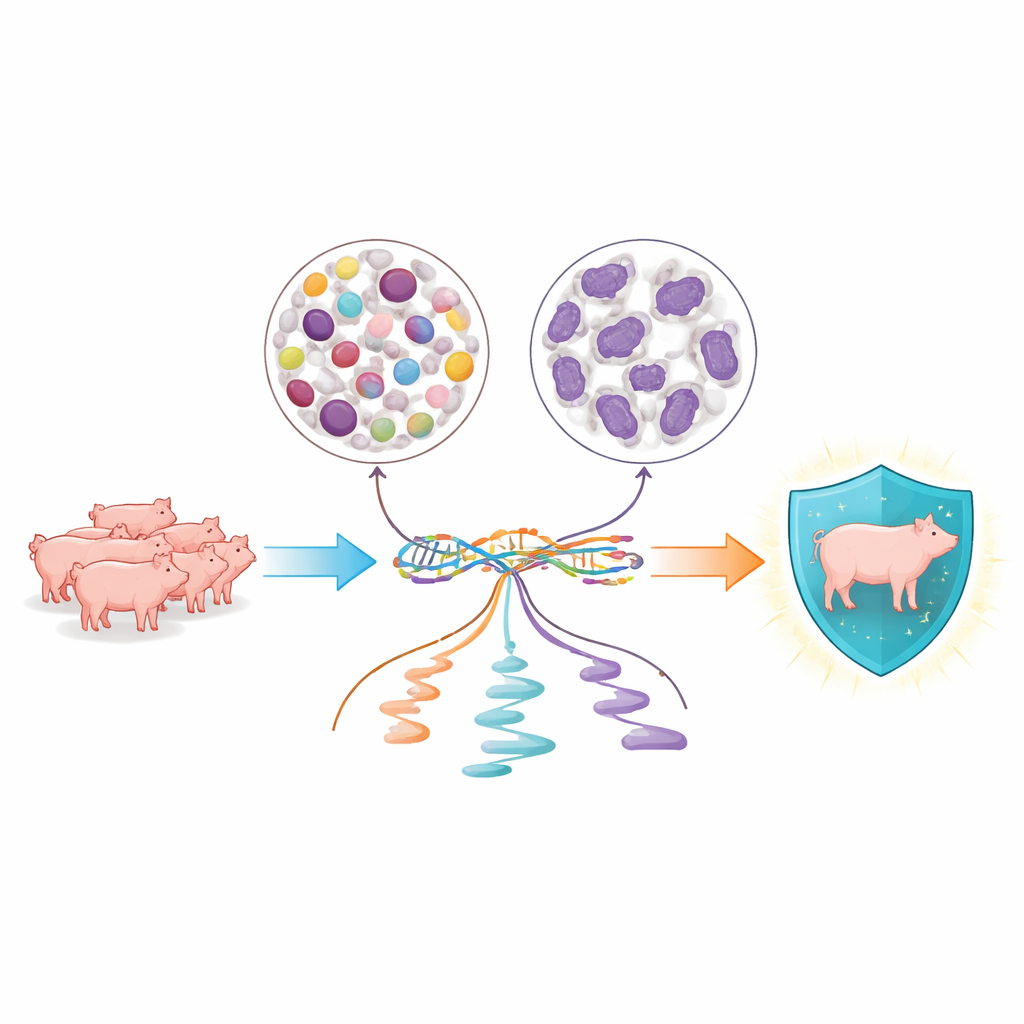
Un’analisi approfondita di due famiglie chiave di cellule del sangue
I ricercatori si sono concentrati su due gruppi principali di globuli bianchi che pattugliano costantemente il sangue suino: le cellule mononucleate del sangue periferico, che comprendono linfociti e monociti coinvolti in difese più lente e mirate, e i neutrofili, che svolgono attacchi rapidi e di prima linea contro i microbi. Da 134 suini Yorkshire giovani, hanno purificato ogni tipo cellulare separatamente e ottenuto sia dati del genoma completo sia istantanee dettagliate dell’RNA, le molecole che trasportano le istruzioni genetiche all’interno delle cellule. Questo ha permesso di vedere non solo quali geni erano attivi, ma anche come la cellula tagliava e completava quei messaggi prima di usarli.
Collegare le varianti del DNA agli interruttori molecolari
Invece di guardare solo a quali varianti del DNA si associano al rischio di malattia, il team ha mappato come le varianti influenzano tre tipi di caratteristiche molecolari in ciascun tipo cellulare. Alcune varianti modificavano la quantità di RNA prodotta da un gene. Altre cambiavano il modo in cui l’RNA veniva spaziato, tagliando o riorganizzando frammenti. Una terza classe spostava il punto in cui l’RNA veniva completato alla sua estremità terminale, un processo chiamato poliadenilazione che può influire sulla stabilità del messaggio. Queste coppie variante–effetto sono chiamate loci quantitativi molecolari, o molQTLs. Le mappe hanno rivelato migliaia di tali siti in ciascun tipo cellulare e, in modo significativo, più di quattro su cinque erano specifici o per le cellule mononucleate miste o per i neutrofili, sottolineando quanto diversamente lo stesso genoma possa essere letto in diverse cellule immunitarie.
Trovare reti che collegano i geni a tratti immunitari reali
Per capire come questi interruttori molecolari si relazionano all’immunità dell’animale intero, gli scienziati hanno combinato le mappe di molQTL con esami del sangue standard e misurazioni di proteine di segnalazione immunitaria. Hanno costruito reti di co-espressione—gruppi di geni che tendono ad aumentare o diminuire insieme—e hanno valutato quali si correlano con tratti come la proporzione di neutrofili o linfociti, il numero di globuli bianchi o i livelli di interferoni e fattore di necrosi tumorale. I moduli legati ai tratti dei linfociti erano arricchiti per vie dell’immunità adattativa, mentre quelli connessi ai tratti dei neutrofili evidenziavano difese innate rapide e segnali infiammatori. Molti geni chiave in questi moduli erano direttamente regolati da molQTL specifici del tipo cellulare, suggerendo percorsi chiari dalla variante del DNA alla modificazione della composizione o della funzione cellulare.
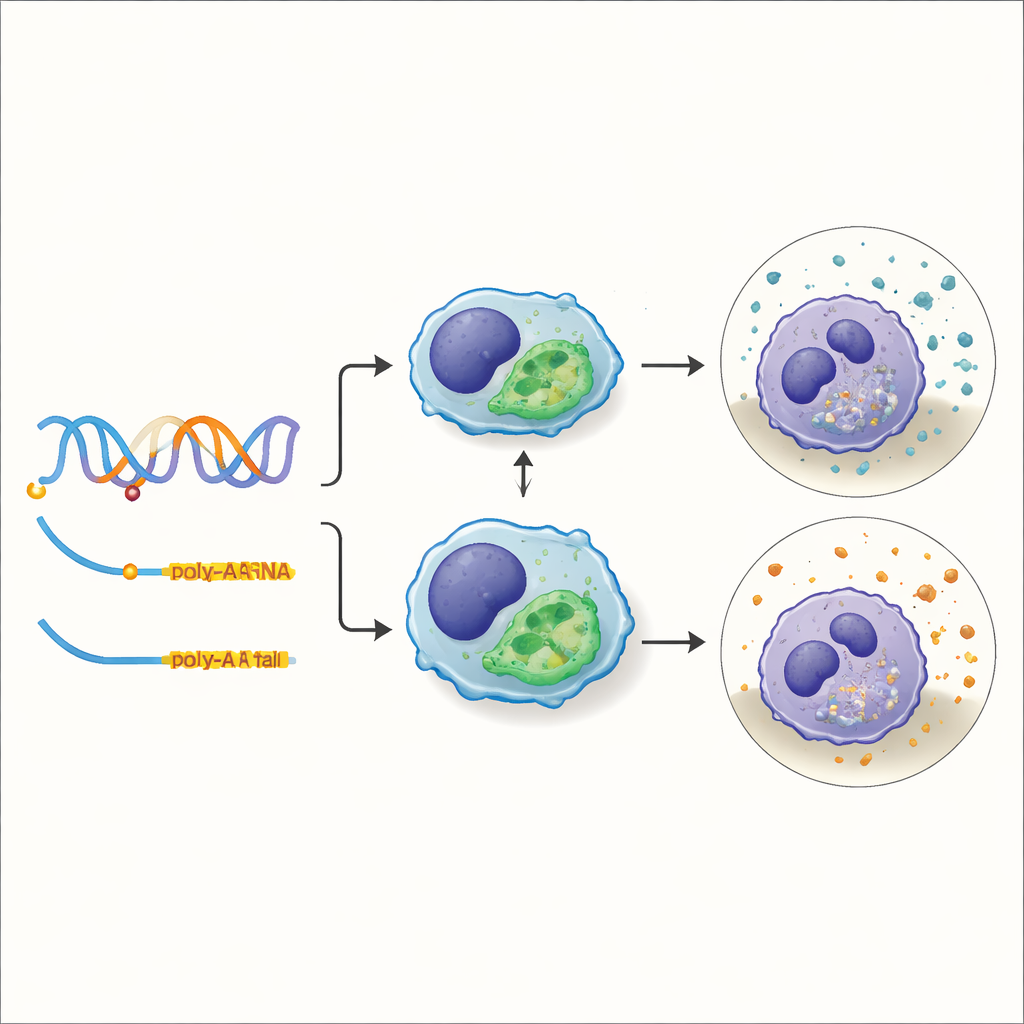
Un’analisi ravvicinata di una variante che modula la capacità di “pulizia” cellulare
Uno dei tratti più pratici esaminati dal team è stata la capacità fagocitaria—la capacità delle cellule immunitarie di inglobare e rimuovere detriti o patogeni. Sovrapponendo i loro molQTL con i risultati di precedenti studi di associazione genome-wide per la fagocitosi, hanno individuato 588 regioni in cui lo stesso cambiamento del DNA probabilmente guida sia uno spostamento molecolare sia una modifica della performance nella pulizia cellulare. Un esempio rilevante è stata una variante all’interno di un gene chiamato TXNDC15. Questa modifica non si limitava ad accendere o spegnere il gene; invece, alterava quale sito di poliadenilazione la cellula sceglieva per l’RNA del gene. I maiali portatori di una versione della variante privilegiavano una coda più corta sull’RNA, che risultava più stabile e si accumulava a livelli più alti, e questi animali mostravano una maggiore attività fagocitaria nelle loro cellule immunitarie.
Cosa significa per maiali più sani e oltre
In termini pratici, questo lavoro mostra come piccole differenze nel DNA possano riorganizzare le “istruzioni” all’interno di specifici tipi cellulari immunitari e, attraverso questo, influenzare quante di queste cellule esistono e quanto bene svolgono il loro lavoro. Separando attentamente i tipi cellulari e monitorando non solo l’attività genica ma anche come i messaggi vengono tagliati e completati, lo studio scopre punti di controllo nascosti che gli studi su tessuti omogenei perdono. La mappa genetica risultante fornisce una base per selezionare maiali naturalmente più resistenti alle malattie, riducendo potenzialmente la necessità di antibiotici. Allo stesso tempo, poiché l’immunità suina somiglia strettamente a quella umana, questi risultati potrebbero aiutare gli scienziati a comprendere come meccanismi simili operino nella salute e nella malattia umane.
Citazione: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Parole chiave: immunità suina, varianti genetiche, cellule immunitarie, fagocitosi, QTL molecolari