Clear Sky Science · it
L'inibizione di ATM aumenta l'efficienza del knock-in sopprimendo l'attivazione delle vie apoptotiche indotte da AAV
Rendere l'editing genetico più efficace
L'editing genetico con CRISPR promette terapie per malattie genetiche, colture più resistenti e potenti strumenti di ricerca. Ma uno dei suoi strumenti più preziosi — l'inserimento preciso di nuovo DNA in un punto scelto del genoma, noto come “knock-in” — funziona ancora in modo inefficiente. Questo studio esplora perché alcune cellule accettano il DNA esogeno più facilmente di altre e rivela un modo per indurre le cellule a eseguire modifiche precise più spesso, soprattutto quando si utilizza l'adenovirus associato (AAV), un vettore di punta per la terapia genica.
Osservare la riparazione del DNA in tempo reale
Per capire cosa favorisce o ostacola l'inserimento preciso dei geni, i ricercatori hanno costruito un intricato “cruscotto” all'interno di cellule staminali embrionali di topo. Questo sistema a triplo reporter usa tre marcatori fluorescenti per monitorare, nelle stesse cellule, se CRISPR ha tagliato il DNA, se è avvenuto un knock-in preciso e se la cellula ha invece inserito il DNA donatore tramite un metodo di riparazione più approssimativo. Leggendo diverse combinazioni di colori con la citometria a flusso, hanno potuto separare le modifiche pulite basate su template dalle inserzioni soggette a errori e dalle cellule non modificate. Questo monitoraggio affiancato ha permesso di mappare come diverse vie di riparazione del DNA contribuiscono a ciascun esito con molta più risoluzione rispetto ai test PCR tradizionali.
Due tipi di donatori di DNA, due risposte molto diverse
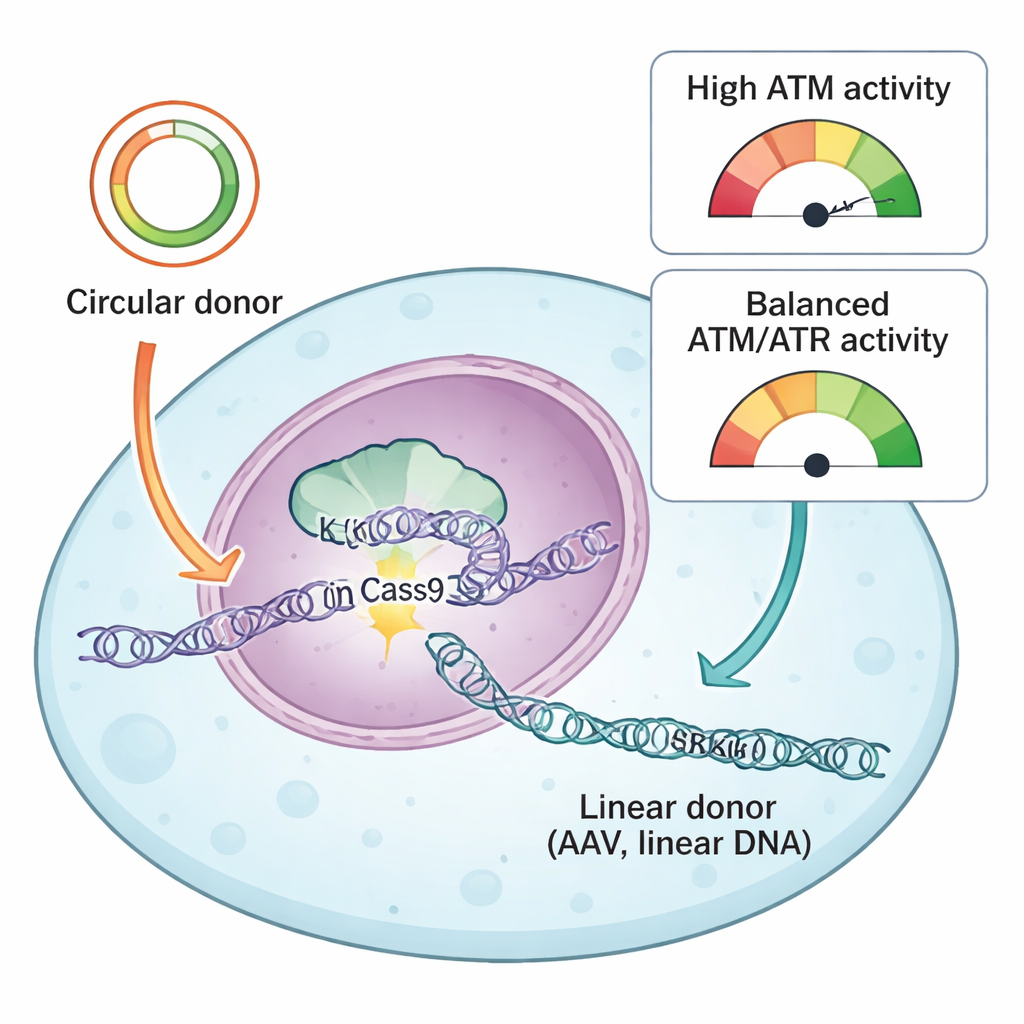
Il gruppo ha confrontato due tipi comuni di DNA donatore usati per guidare le riparazioni indotte da CRISPR: plasmidi circolari e DNA lineare derivato da AAV. Entrambi portano bracci di omologia che indicano alla cellula dove inserire la nuova sequenza, ma entrano nella cellula in forme fisiche diverse. I plasmidi circolari sono anelli chiusi di DNA a doppio filamento, mentre i donatori AAV arrivano tipicamente come molecole lineari singole. Usando il loro sistema reporter e una libreria di farmaci che prendono di mira proteine della risposta al danno del DNA, gli autori hanno scoperto che una proteina chiave, ATR, è stata uniformemente essenziale per knock-in riusciti con entrambi i tipi di donatore. L'inibizione di ATR ha ridotto nettamente l'inserimento preciso, mentre un lieve potenziamento dell'attività di ATR tramite la via KEAP1–NRF2 ha reso i knock-in più efficienti, specialmente con donatori AAV.
Quando la protezione del DNA si ritorce contro
Un altro sensore del danno al DNA, ATM, si è comportato in modo sorprendentemente dipendente dal tipo di donatore. Con donatori plasmidici circolari, il blocco di ATM ha ridotto sia i knock-in precisi sia le inserzioni mediate dall'end-joining, in linea con il suo ruolo classico nell'aiutare la riparazione dei doppio filamenti. Ma con DNA lineare — sia da AAV, AAV auto-complementare, sia da plasmidi tagliati in frammenti lineari — l'inibizione di ATM ha avuto l'effetto opposto: ha aumentato l'efficienza del knock-in. I ricercatori hanno ricondotto questo effetto al modo in cui le cellule interpretano ondate di DNA lineare. Alte dosi di AAV attivavano fortemente ATM, che a sua volta attivava p53 e caspasi 3, attori centrali nella morte cellulare programmata. Le cellule che avevano incorporato molte copie del DNA donatore, e quindi avevano la probabilità più alta di un knock-in riuscito, erano anche le più suscettibili a essere eliminate da questo sistema di allarme.
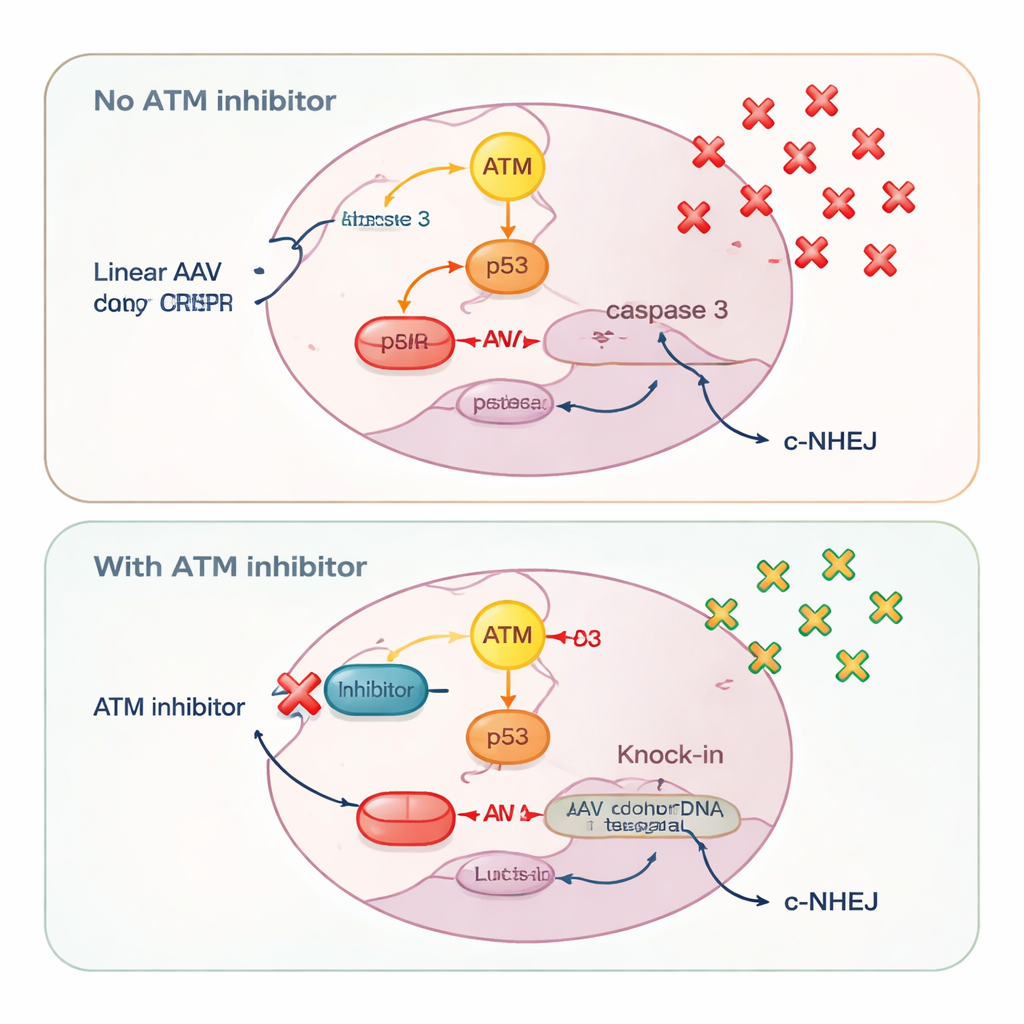
Salvare le cellule meglio equipaggiate
Aggiungendo inibitori di ATM, gli scienziati hanno silenziato la via di morte ATM–p53–caspasi 3. Questo ha risparmiato le cellule che contenevano grandi quantità di DNA donatore, permettendo a più di esse di sopravvivere abbastanza a lungo da completare un knock-in preciso. Le misurazioni delle copie del genoma virale hanno confermato che l'inibizione di ATM aumentava il numero di molecole AAV trattenute all'interno delle cellule. Allo stesso tempo, il blocco di ATM ha attenuato leggermente una via di riparazione rapida e rozza chiamata giunzione non omologa classica (classical non-homologous end-joining), come mostrato dalla ridotta attivazione di DNA-PK, un enzima centrale di quella via. Indebolire questa opzione di riparazione concorrente ha diretto più tagli indotti da CRISPR verso il knock-in basato sull'omologia piuttosto che a riparazioni rapide che ignorano il template donatore.
Cosa significa per le future terapie geniche
Per i non specialisti, il messaggio è che gli stessi meccanismi cellulari che ci proteggono dai danni al DNA possono involontariamente sabotare l'editing genetico preciso, soprattutto quando si usano grandi quantità di DNA donatore virale. Questo lavoro mostra che modulare con attenzione questi meccanismi — mantenendo ATR attivo ma trattenendo temporaneamente ATM quando sono presenti donatori lineari come l'AAV — può rendere i knock-in CRISPR più affidabili ed efficienti. Una simile strategia potrebbe migliorare le terapie geniche, l'ingegneria cellulare e i modelli di malattia aiutando più cellule ad accettare la modifica voluta riducendo nel contempo perdite cellulari non necessarie.
Citazione: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Parole chiave: knock-in CRISPR, editing genico AAV, risposta al danno del DNA, inibizione di ATM, ingegneria del genoma