Clear Sky Science · it
STING controlla la glicolisi e la lattilazione degli istoni per guidare la riprogrammazione metabolica dei macrofagi nellileo postoperatorio
Quando l’intervento chirurgico mette il tubo digerente in pausa
Dopo un’operazione addominale, molti pazienti scoprono che il loro intestino semplicemente non vuole riattivarsi. Questo rallentamento, chiamato ileo postoperatorio, può tradursi in giorni di nausea, gonfiore e recupero ritardato. Lo studio riassunto qui si pone una domanda apparentemente semplice: perché certe cellule immunitarie nell’intestino mantengono l’intestino bloccato e potrebbe bastare modulare un singolo interruttore molecolare per far ripartire la motilità intestinale?
Come un’operazione di routine scatena l’infiammazione intestinale
L’intervento addominale disturba inevitabilmente l’intestino. Nei topi, una manipolazione delicata dell’intestino è stata sufficiente a causare gonfiore, accumulo di liquidi e blocco del contenuto nel piccolo intestino. Quando i ricercatori hanno monitorato quanto lontano un colorante fluorescente innocuo si spostava lungo il tratto intestinale, hanno osservato che l’intervento rallentava bruscamente il suo progresso, segno di motilità compromessa. L’esame microscopico della parete intestinale ha mostrato che lo strato muscolare — il tessuto che effettivamente si contrae per spingere il cibo — diventava infiammato e affollato di cellule immunitarie in arrivo, in particolare macrofagi e neutrofili. Questi riscontri suggeriscono che la tonaca muscolare intestinale diventa un campo di battaglia infiammato dopo l’intervento e che questa infiammazione locale è strettamente legata alla paralisi intestinale.
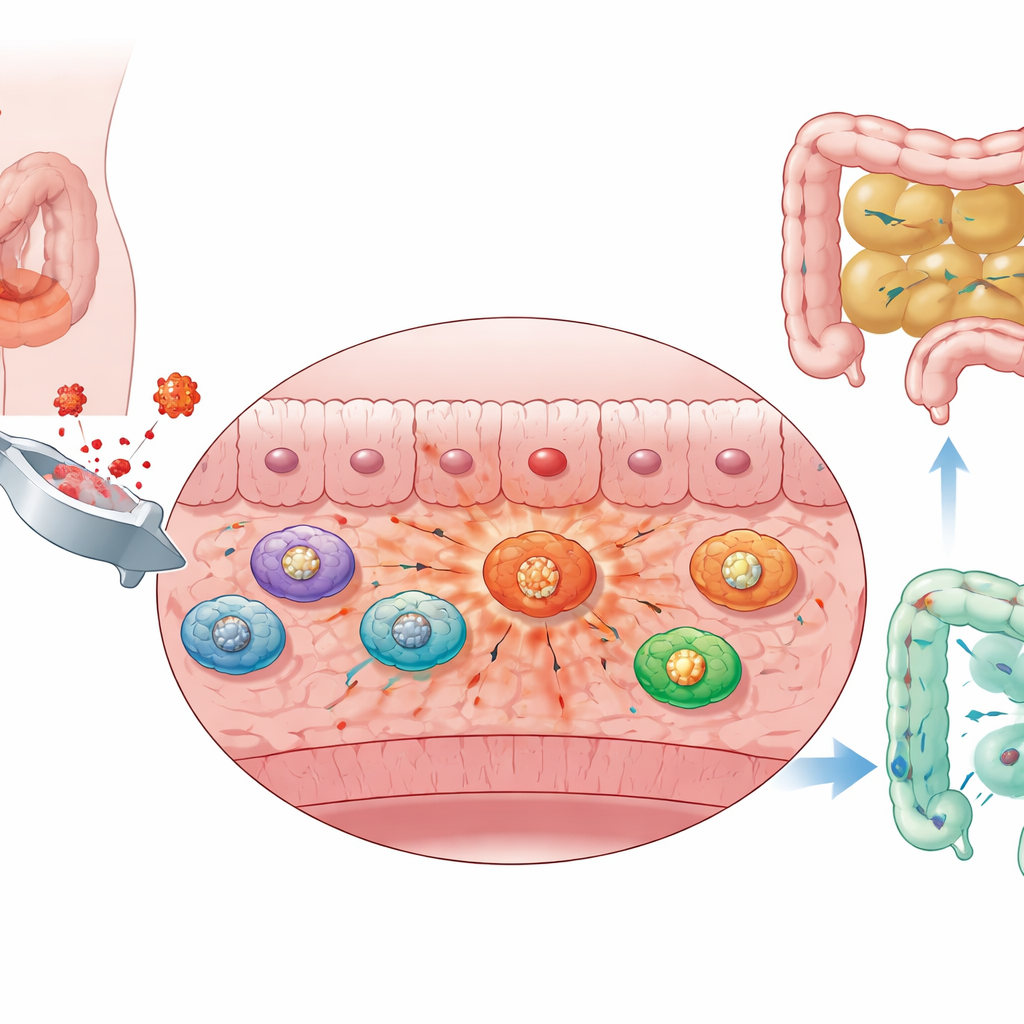
I macrofagi cambiano carburante e alimentano le fiamme
Per capire cosa stessero facendo questi macrofagi infiltranti, il gruppo ha analizzato dati di RNA su larga scala e di sequenziamento a singola cellula provenienti dallo strato muscolare intestinale. Hanno riscontrato che i macrofagi negli animali operati aumentavano in modo marcato una via rapida di consumo di zuccheri nota come glicolisi. Rispetto ad altre cellule immunitarie nello stesso tessuto, i macrofagi infiltranti mostravano i punteggi di glicolisi più elevati ed esprimevano livelli aumentati di enzimi glicolitici chiave. Un sottogruppo distinto di queste cellule faceva forte affidamento sulla glicolisi, presentava marcature infiammatorie pronunciate e rispondeva vigorosamente a componenti batterici come il lipopolisaccaride. In sostanza, i macrofagi erano passati a una modalità ad alto consumo di zucchero e alta infiammazione che sembra aggravare l’infiammazione dello strato muscolare e mantenere l’intestino fermo.
Un interruttore molecolare che collega il rilevamento del pericolo al consumo di zucchero
I ricercatori si sono quindi concentrati su STING, una proteina nota principalmente come sistema di allarme per il DNA estraneo ma sempre più riconosciuta come regolatrice metabolica. Nel muscolo intestinale infiammato, il sottogruppo di macrofagi altamente glicolitici mostrava livelli di STING marcatamente maggiori, un pattern confermato dall’immunocolorazione tissutale. In coltura cellulare, l’esposizione dei macrofagi al lipopolisaccaride batterico aumentava sia l’attività di STING sia gli enzimi glicolitici che aiutano a convertire il glucosio in energia e lattato. Quando gli scienziati hanno eliminato il gene STING, questo picco di consumo di zucchero crollava: gli intermedi glicolitici diminuivano, l’acidificazione del mezzo di coltura calava e si producevano meno specie reattive dell’ossigeno. Queste cellule prive di STING generavano anche meno lattato, suggerendo che la via dell’allarme e il motore metabolico sono strettamente accoppiati.
Dal rifiuto zuccherino alla memoria epigenetica
Il lattato è spesso considerato un prodotto di scarto metabolico, ma qui gioca un ruolo più sottile. Il gruppo ha mostrato che nei macrofagi normali l’ondata di lattato viene utilizzata per modificare chimicamente gli istoni — le proteine che impacchettano il DNA — attraverso un processo chiamato lattilazione. Questa modificazione era particolarmente evidente in un sito chiamato H4K8 sugli istoni vicino al gene per HK2, un enzima glicolitico chiave. Nelle cellule prive di STING, la lattilazione degli istoni e l’accessibilità della cromatina al promotore di HK2 risultavano entrambe ridotte, e metodi di sequenziamento specializzati confermarono che questi cambiamenti limitavano l’attivazione di HK2. Allo stesso tempo, un fattore di trascrizione a valle, IRF3, è risultato legarsi direttamente al promotore di HK2 più facilmente quando questo marcatore di lattilazione degli istoni era presente. Insieme, questi passaggi creano un circuito auto-rinforzante: STING stabilizza fattori che potenziano la glicolisi, la glicolisi produce lattato, il lattato decora gli istoni per aprire il gene HK2, e IRF3 aumenta l’espressione di HK2, alimentando ulteriormente glicolisi e infiammazione.
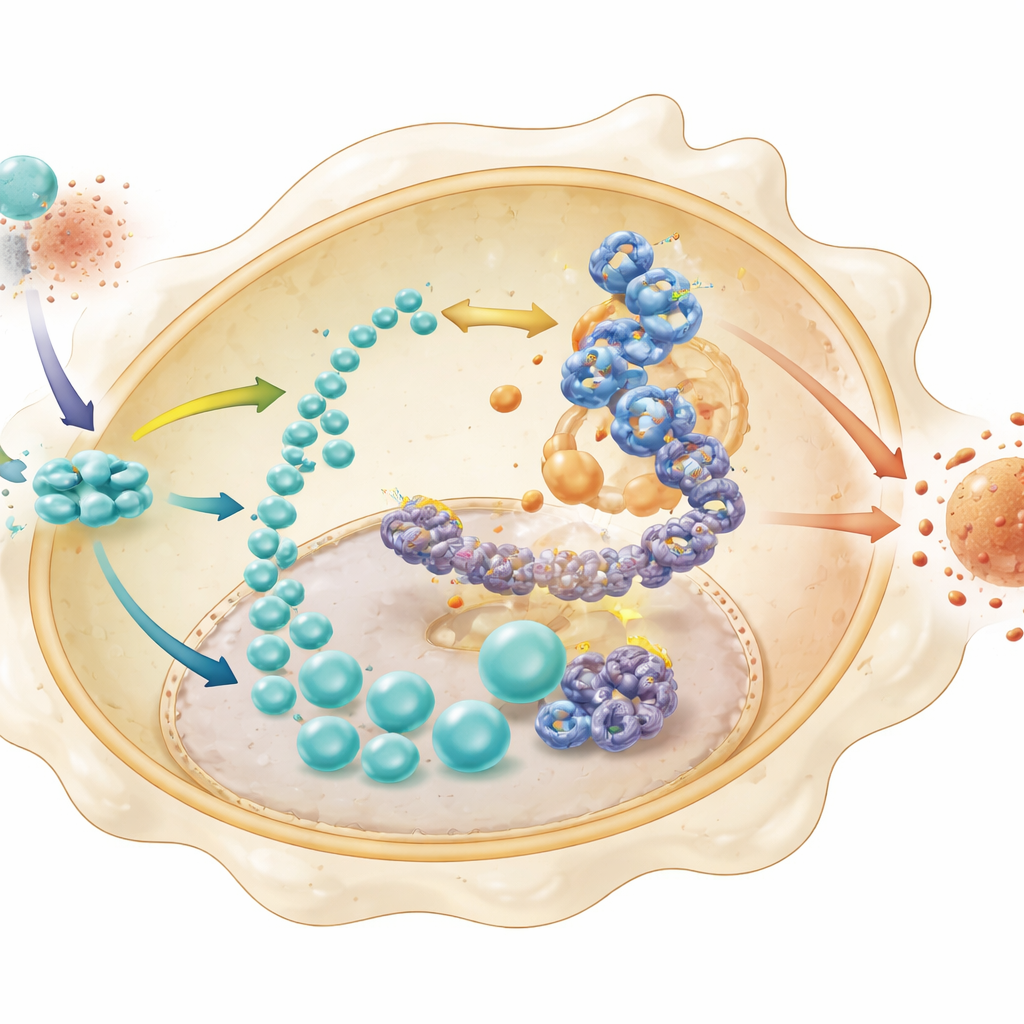
Spezzare il circuito per permettere la ripresa intestinale
Infine, il gruppo si è chiesto se interrompere questo circuito potesse effettivamente aiutare gli animali a recuperare dall’ileo postoperatorio. Nei topi privi di STING, il tessuto muscolare intestinale esprimeva meno enzimi glicolitici, conteneva meno macrofagi infiammatori e mostrava uno spostamento da uno stato macrofagico aggressivo e pro-infiammatorio verso un profilo più orientato alla risoluzione. L’infiltrazione di neutrofili era ridotta e il transito intestinale migliorava. Il blocco farmacologico di STING nei topi normali ha prodotto benefici simili, mentre la riattivazione dell’enzima HK2 negli animali carenti di STING ha parzialmente ripristinato infiammazione e problemi di motilità. Per un lettore non specialista, il messaggio è chiaro: un singolo interruttore di rilevamento del pericolo nei macrofagi intestinali può rimodellare il loro metabolismo in modo da bloccare l’intestino in una lunga pausa dopo l’intervento. Mirare a STING — o al circuito di feedback che governa il consumo di zucchero e la scrittura del lattato sugli istoni — offre una strada promettente per accelerare il recupero e alleviare una delle complicanze più ostinate degli interventi addominali.
Citazione: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Parole chiave: ileo postoperatorio, metabolismo dei macrofagi, via STING, glicolisi, infiammazione intestinale