Clear Sky Science · it
Caratterizzare la sviluppabilità dei nanocorpi per migliorare la progettazione terapeutica con il Therapeutic Nanobody Profiler
Perché i cugini minuscoli degli anticorpi contano per i farmaci del futuro
Molti dei farmaci di grande successo di oggi sono anticorpi—proteine che si legano ai bersagli patologici con grande precisione. Una classe più recente di leganti ancora più piccoli, chiamati nanocorpi, può infilarsi in tasche difficili da raggiungere su virus, tumori e altre molecole. Ma saper legare un bersaglio non basta: un potenziale farmaco deve anche essere facile da produrre, stabile in bottiglia e sicuro nell’organismo. Questo articolo presenta il Therapeutic Nanobody Profiler, uno strumento computazionale pensato per aiutare gli scienziati a valutare, precocemente e a partire solo dalla sequenza, quali nanocorpi hanno maggiori probabilità di diventare farmaci pratici.
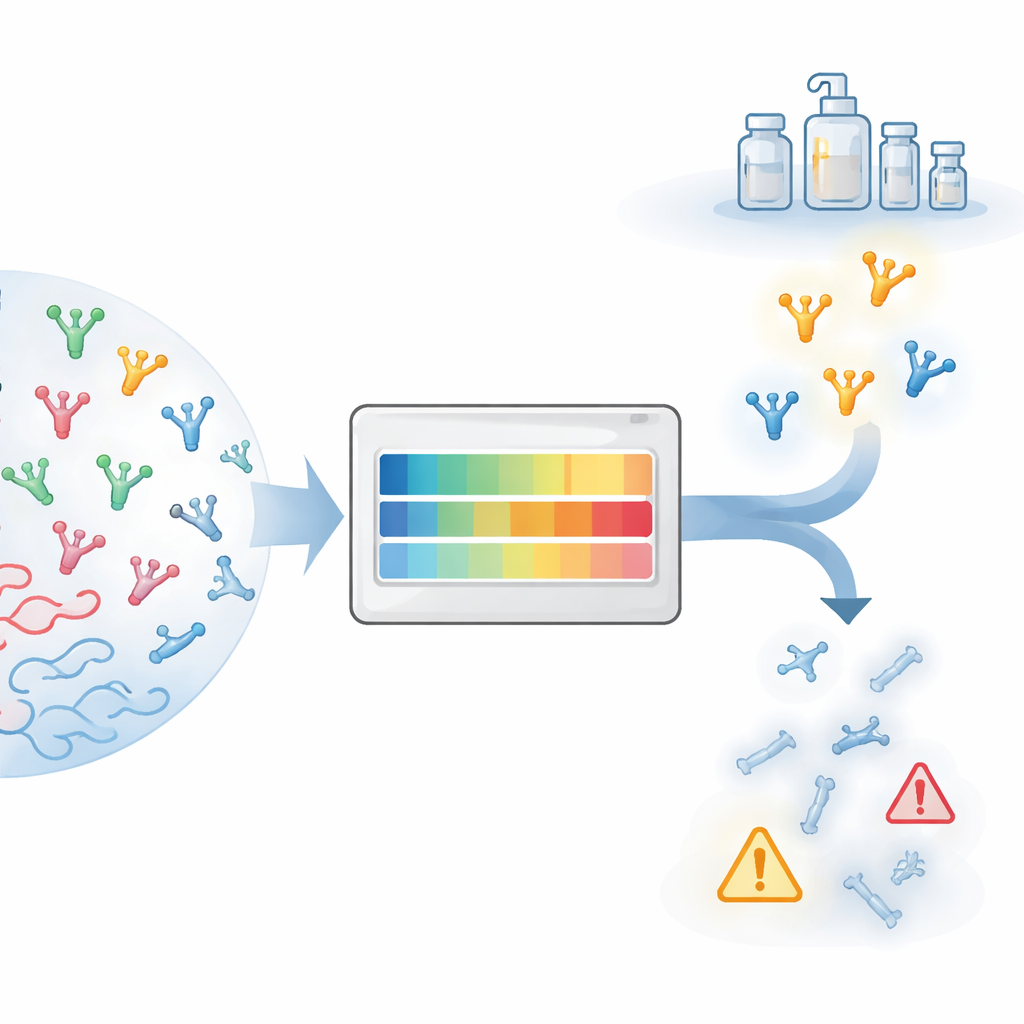
Dall’idea promettente al farmaco pratico
Trasformare una proteina in una terapia reale comporta una serie di ostacoli pratici riuniti sotto il termine “sviluppabilità”. Le proteine devono poter essere prodotte in grandi quantità, rimanere solubili, evitare di aggregarsi e mantenersi stabili durante il trasporto e lo stoccaggio. Nell’ultimo decennio i ricercatori hanno imparato a prevedere molti di questi tratti per gli anticorpi monoclonali di dimensioni normali, supportati da abbondanti dati clinici e test di laboratorio specialistici. I nanocorpi, però, sono strutturalmente diversi: sono costituiti da un singolo dominio anziché da una coppia di catene, spesso hanno anse di legame più lunghe e espongono regioni superficiali che negli anticorpi convenzionali sono sepolte. Di conseguenza, metodi tarati sugli anticorpi standard possono dare risposte fuorvianti se applicati ai nanocorpi.
Un profiler costruito sulle particolarità dei nanocorpi
Per affrontare questo disallineamento, gli autori hanno progettato il Therapeutic Nanobody Profiler (TNP), ispirato a uno strumento precedente per anticorpi standard ma rielaborato attorno alla biologia dei nanocorpi. Hanno raccolto sequenze di nanocorpi da molte fonti: trial clinici, repertori immunitari naturali, brevetti, articoli scientifici e strutture cristallografiche note. Usando predittori strutturali basati sul deep learning adattati agli anticorpi a dominio singolo, hanno generato modelli 3D per queste sequenze. Da ciascun modello hanno misurato la lunghezza delle anse di legame, quanto una ansa chiave si protende dal corpo della proteina e come cluster di residui idrofobici e carichi sono disposti sulla superficie—caratteristiche che influenzano fortemente solubilità, aggregazione e adesione non specifica.
Due sapori strutturali, entrambi utilizzabili
Una delle osservazioni più rilevanti riguarda l’ansa di legame principale, nota come CDR3. Quando il team ha quantificato quanto questa ansa sia “compatta”—confrontando la sua lunghezza con quanto si estende dalla proteina—ha trovato una netta divisione in due stili strutturali. In un sottotipo, l’ansa è più lunga e si ripiega sul fianco della proteina, formando numerosi contatti stabilizzanti con un insieme di residui caratteristici. Nell’altro, l’ansa sporge di più, come in un frammento di anticorpo convenzionale. I nanocorpi in fase clinica appartengono a entrambi i sottotipi e, quando i ricercatori hanno confrontato dozzine di misure di laboratorio pratiche—come aggregazione, auto‑associazione e stabilità termica—non hanno osservato una penalità sistematica per uno stile rispetto all’altro. Ciò significa che i progettisti di farmaci non devono favorire a priori una forma complessiva dell’ansa rispetto all’altra, purché le altre proprietà risultino accettabili.
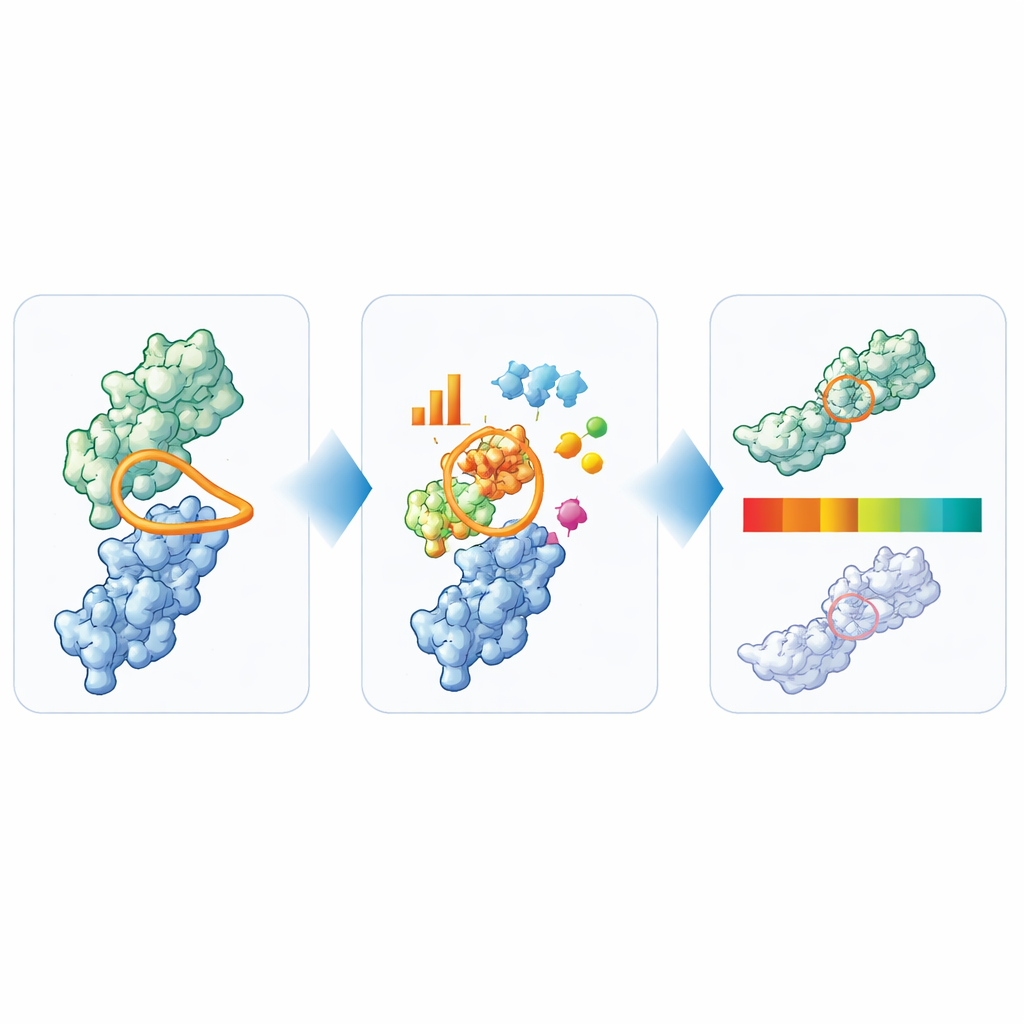
Trasformare la struttura in semafori semplici
Dalla loro ampia analisi, gli autori hanno distillato sei caratteristiche chiave che insieme catturano le principali preoccupazioni di sviluppabilità per i nanocorpi: la lunghezza totale delle anse, la lunghezza specifica e la compattezza della CDR3, e le dimensioni delle patch superficiali idrofobiche, cariche positivamente e cariche negativamente attorno al sito di legame. Hanno quindi utilizzato i 36 nanocorpi che hanno raggiunto la sperimentazione clinica per fissare confini pratici per ciascuna misura. I valori nella regione centrale, ben rappresentata, sono etichettati “verde”, i valori al limite “ambra” e i chiari valori anomali “rosso”. Per verificare quanto questi segnali siano informativi, hanno applicato il TNP a 72 nanocorpi proprietari aggiuntivi e hanno confrontato le segnalazioni con un ampio pannello di saggi di laboratorio. I nanocorpi che TNP ha marcato come chiari outlier mostravano spesso anche molteplici segnali di allarme sperimentali, mentre quelli che apparivano puliti computazionalmente si comportavano più spesso bene in laboratorio.
Cosa significa per i trattamenti di domani
Per i non specialisti, il messaggio fondamentale è che la forma e il motivo superficiale di un nanocorpo possono ora essere convertiti in un profilo di sviluppabilità immediatamente interpretabile prima che inizino costosi lavori di laboratorio. Il Therapeutic Nanobody Profiler non sostituisce gli esperimenti, e rimangono occasionali discrepanze tra previsioni e saggi, soprattutto perché i test di laboratorio sono stati condotti su nanocorpi fusi a frammenti anticorpali più grandi. Ma segnalando rapidamente candidati con anse insolitamente lunghe o strettamente ripiegate o con patch superficiali problematiche, il TNP aiuta a indirizzare l’attenzione verso nanocorpi che hanno maggiori probabilità di diventare farmaci affidabili. Man mano che più nanocorpi entreranno in sperimentazioni cliniche e il set di riferimento si amplierà, questo strumento dovrebbe diventare ancora più accurato, accelerando la progettazione di medicine piccole e robuste simili ad anticorpi per un’ampia gamma di malattie.
Citazione: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Parole chiave: nanocorpi, sviluppabilità dei farmaci biologici, profilazione computazionale, ingegneria degli anticorpi, stabilità delle proteine