Clear Sky Science · it
La degradazione mediata da DTX1 di TUBB3 nelle cellule di Kupffer mitiga la progressione del carcinoma epatocellulare regolando la polarizzazione M1/M2
Perché contano i “vicini” immunitari del fegato
La maggior parte delle persone pensa al cancro come a una malattia di cellule fuorilegge che crescono senza controllo. Ma i tumori vivono in un quartiere affollato di cellule immunitarie, vasi sanguigni e tessuto di supporto che possono sia combattere il cancro sia, silenziosamente, favorirne la crescita. Questo studio esamina il cancro al fegato—in particolare il carcinoma epatocellulare—e rivela come una proteina all’interno di cellule immunitarie specializzate del fegato possa inclinare l’equilibrio tra una risposta anti‑tumorale e un ambiente favorevole al tumore. Capire questo interruttore nascosto potrebbe aprire strade nuove per migliorare le immunoterapie attuali.
Un cancro del fegato guidato dall’ambiente circostante
Il fegato è ricco di cellule immunitarie, compresa una popolazione residente chiamata cellule di Kupffer che normalmente aiuta a mantenere l’organo sano. Nel cancro del fegato molte di queste cellule si trasformano in macrofagi associati al tumore che possono o attaccare il cancro (uno stato di tipo M1) o proteggerlo (uno stato di tipo M2). I pazienti i cui tumori sono infarciti di macrofagi di tipo M2 in genere hanno esiti peggiori e spesso rispondono male a farmaci che sbloccano le difese immunitarie, come gli inibitori di PD‑1. Gli autori hanno iniziato analizzando banche dati geniche pubbliche e campioni di pazienti per cercare molecole collegate sia al carcinoma epatocellulare sia a questi macrofagi, concentrandosi su una proteina strutturale chiamata TUBB3 che si è rivelata inaspettatamente abbondante nel tessuto tumorale.
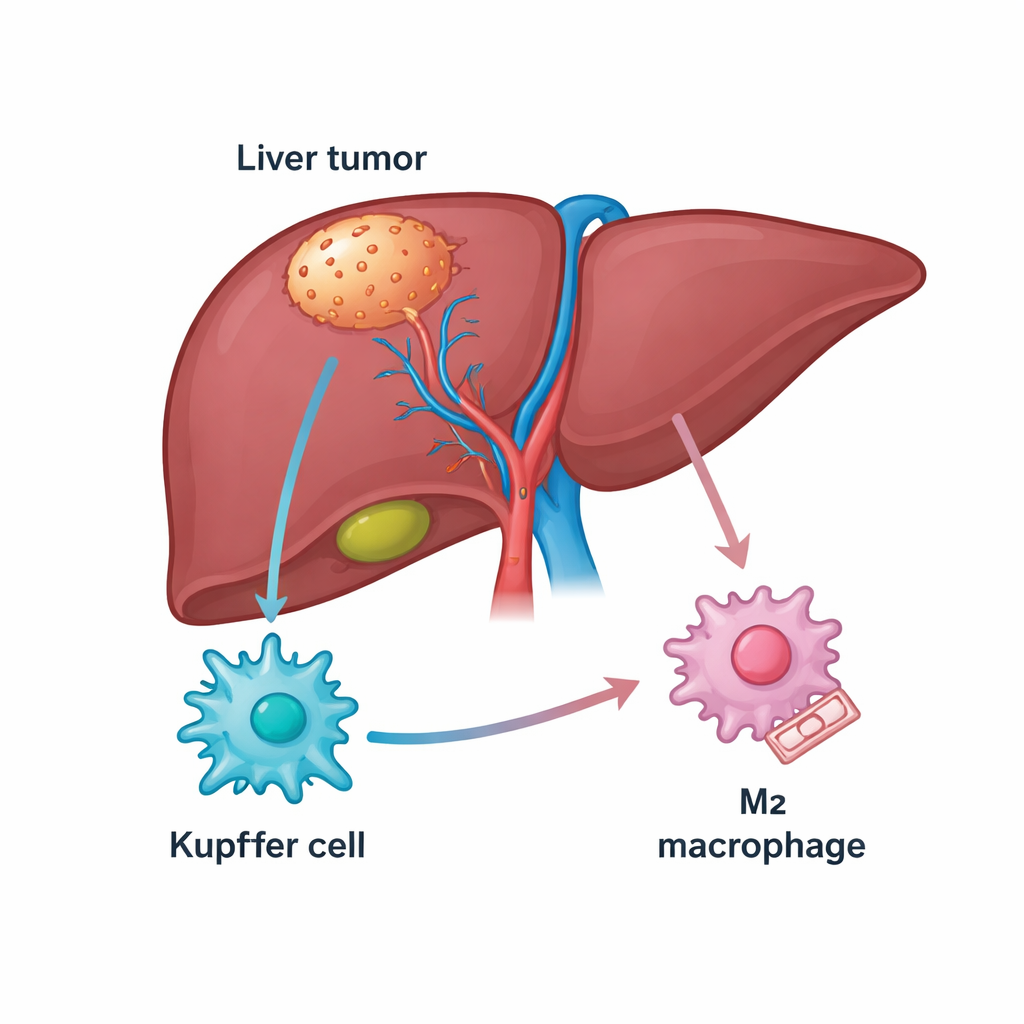
Una proteina sorprendente che spinge le cellule immunitarie a favorire il tumore
TUBB3 è nota soprattutto come componente dei “binari” microscopici all’interno delle cellule, ma è stata anche collegata a comportamenti aggressivi e resistenza ai farmaci in diversi tumori. Qui, i ricercatori hanno osservato che i livelli di TUBB3 erano molto più alti nei tumori del fegato rispetto al tessuto sano circostante e che i pazienti con più TUBB3 tendevano ad avere una sopravvivenza più corta. Mediante tecniche di colorazione, hanno mostrato che TUBB3 era particolarmente arricchita nelle cellule di Kupffer all’interno dei tumori e che la sua presenza si associava fortemente a marcatori dello stato M2 che aiuta il tumore. In altre parole, le cellule di Kupffer ricche di TUBB3 erano più propense a comportarsi in modo da attenuare l’attacco immunitario e sostenere la crescita tumorale.
Riprogrammare i macrofagi per contenere i tumori epatici
Per mettere alla prova causa ed effetto, il gruppo ha ridotto i livelli di TUBB3 nelle cellule di Kupffer in esperimenti di laboratorio. Quando TUBB3 è stato silenziato, queste cellule producevano meno segnali di tipo M2, più segnali di tipo M1 e secernevano meno molecole che normalmente sopprimono l’attività immunitaria. Le cellule di carcinoma epatocellulare esposte a questi macrofagi riprogrammati crescevano più lentamente, si dividevano meno e avevano minore capacità di migrare e invadere. Nei topi, miscelare cellule tumorali del fegato con cellule di Kupffer carenti di TUBB3 ha portato a tumori più piccoli, maggiore morte delle cellule tumorali e un maggior afflusso di cellule T CD8 citotossiche dotate di proteine distruttive. Se i macrofagi venivano rimossi dagli animali, il beneficio derivante dal blocco di TUBB3 scompariva in gran parte, sottolineando che l’effetto passa attraverso queste cellule immunitarie piuttosto che attraverso le sole cellule tumorali.
Scoprire un freno interno su una via di segnalazione chiave
Lo studio ha anche indagato come TUBB3 eserciti questa influenza. Gli autori si sono concentrati su una nota via di crescita e sopravvivenza controllata dalle proteine PTEN e AKT, che influenza anche se i macrofagi adottino un’identità M1 o M2. Hanno scoperto che abbassare TUBB3 aumentava PTEN, il che a sua volta riduceva i “tag” di fosfato attivanti su AKT, spingendo i macrofagi verso lo stato anti‑tumorale. Quando hanno riattivato artificialmente AKT, i macrofagi sono tornati al profilo M2 e le cellule tumorali hanno riacquistato un comportamento aggressivo, anche in assenza di TUBB3. Ciò colloca TUBB3 a monte di PTEN e AKT come una sorta di manopola interna del comportamento dei macrofagi.
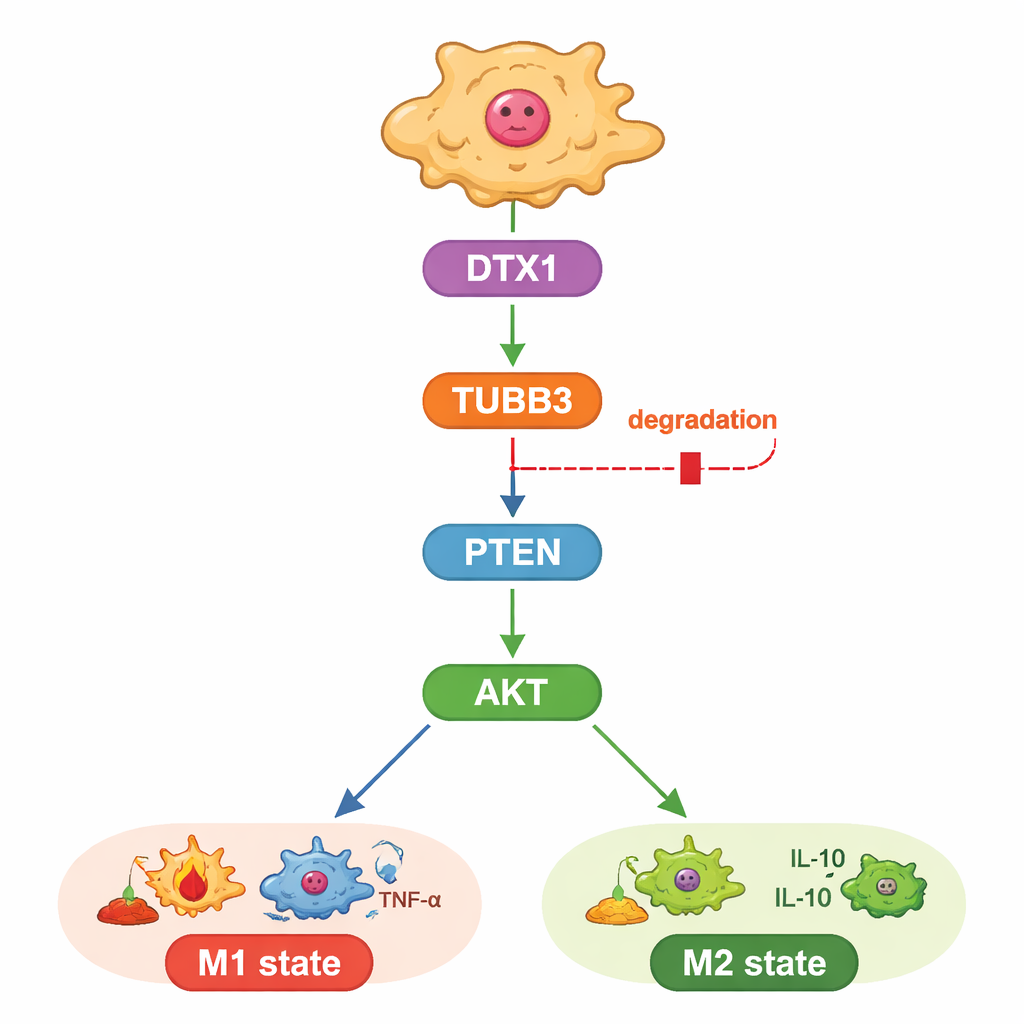
Un’etichetta di smaltimento incorporata che potrebbe essere riattivata
Infine, i ricercatori si sono chiesti perché TUBB3 sia così abbondante nei tumori del fegato. Combinando previsioni bioinformatiche con dati di espressione, hanno identificato un enzima chiamato DTX1, parte di una famiglia che etichetta le proteine per lo smaltimento, come un probabile regolatore. I livelli di DTX1 erano più bassi nei tumori del fegato rispetto al tessuto sano e si correlavano a migliori esiti nei pazienti e a una maggiore presenza di macrofagi di tipo M1. Nelle cellule, aumentare DTX1 accelerava la degradazione di TUBB3, attenuava l’attività di AKT e spingeva i macrofagi verso lo stato anti‑tumorale, rallentando la crescita delle cellule cancerose. Sovrascrivere questo effetto reintrodurrendo TUBB3 eliminava i benefici di DTX1, sia nelle colture che nei tumori nei topi. Nel complesso, questi risultati tracciano una linea chiara da DTX1 attraverso TUBB3 e PTEN/AKT fino al tono immunitario del tumore.
Cosa significa per il futuro del trattamento del cancro del fegato
Per chi non è specialista, il messaggio chiave è che questo lavoro identifica un sistema di controllo finora nascosto all’interno delle cellule immunitarie residenti del fegato che decide se esse aiutano o ostacolano il cancro. Quando l’enzima che marca per lo smaltimento DTX1 è basso, TUBB3 si accumula, una via di crescita si accende e le cellule di Kupffer scivolano in una modalità che supporta il tumore e attenua l’effetto dell’immunoterapia. Ripristinare questo circuito—abbassando TUBB3, potenziando DTX1 o modulando con cura il segnale PTEN/AKT—potrebbe risvegliare le difese immunitarie locali e rendere trattamenti come gli inibitori di PD‑1 più efficaci. Pur essendo strategie ancora a uno stadio sperimentale, evidenziano la promessa di trattare non solo le cellule tumorali, ma anche i “vicini” immunitari circostanti che influenzano fortemente il comportamento del carcinoma epatocellulare.
Citazione: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Parole chiave: carcinoma epatocellulare, macrofagi associati al tumore, cellule di Kupffer, immunoterapia, segnalazione AKT