Clear Sky Science · it
Sparsificazione e decorrelazione dell’attività delle cellule granulari nel giro dentato da parte della noradrenalina
Perché un picco di attenzione può affinare i ricordi
I momenti che ci scuotono—un quasi incidente in auto, un commento inaspettato, una svolta sorprendente in un film—spesso restano impigliati nella memoria molto più di una giornata qualunque. Questo studio esplora un motivo chiave: una sostanza chimica cerebrale legata all’eccitazione, la noradrenalina, rimodella silenziosamente il modo in cui un importante filtro mnemonico nell’ippocampo seleziona e separa le esperienze, aiutando eventi simili a risultare più facilmente distinguibili in seguito.
Il regolatore del cervello per esperienze simili
All’interno dell’ippocampo si trova il giro dentato, una regione che funziona come un guardiano per i nuovi ricordi. Riceve informazioni ricche dalla corteccia entorinale—segnali su dove siamo e su cosa succede intorno a noi—e le converte in schemi di attività nelle cellule granulari, i suoi neuroni principali. Teoria ed esperimenti suggeriscono che questi schemi debbano essere “sparsi” (poche cellule attive alla volta) e “decorrelati” (esperienze diverse attivano insiemi differenti di cellule) affinché i ricordi non si mescolino. Tuttavia, come avvenga questa trasformazione a livello di singole cellule e circuiti è rimasto poco chiaro.
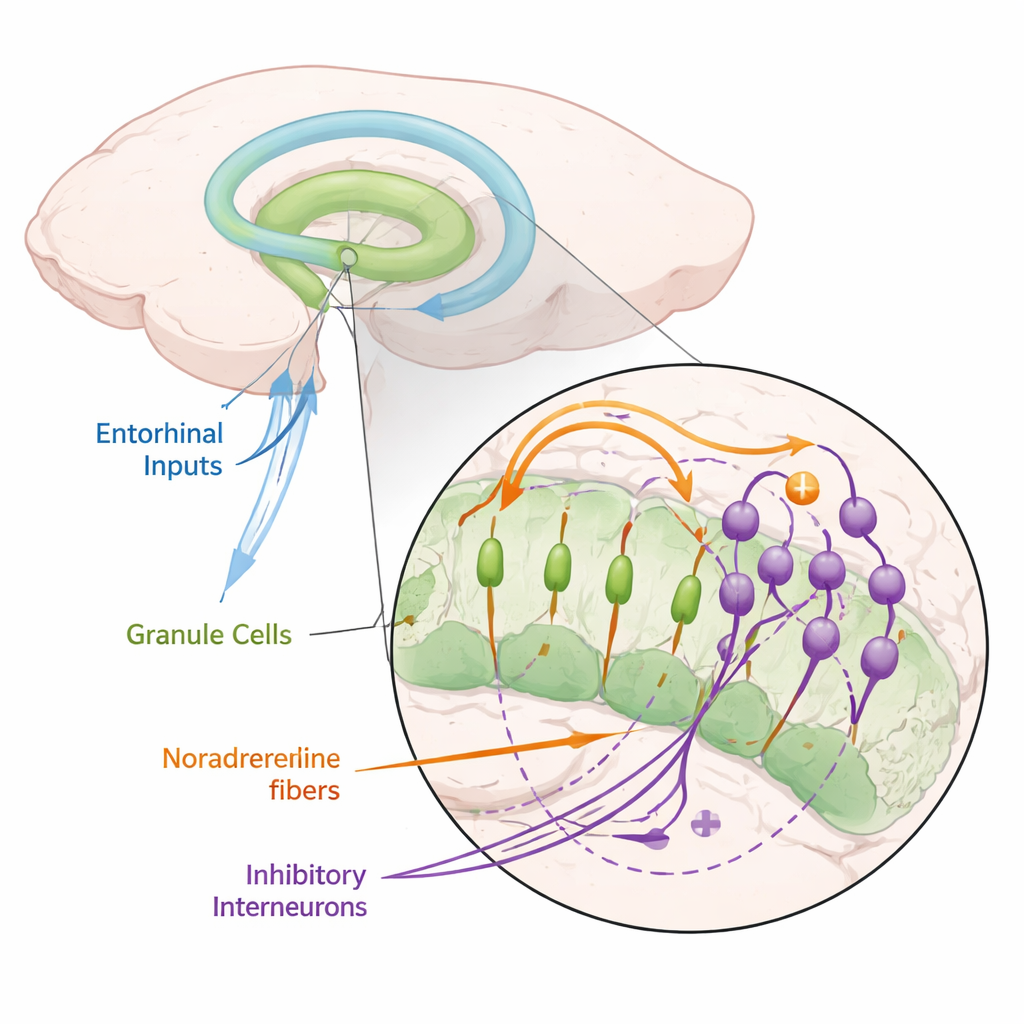
Sostanza dell’eccitazione che zittisce cellule chiave della memoria
Gli autori si sono concentrati sulla noradrenalina, un neuromodulatore rilasciato da neuroni in una piccola area del tronco encefalico chiamata locus coeruleus, che si attiva durante attenzione, novità e stress. Usando topi, hanno espresso proteine sensibili alla luce in questi neuroni noradrenergici, permettendo di rilasciare noradrenalina a comando con lampi di luce. Quando hanno stimolato la principale via di ingresso verso il giro dentato e registrato dalle cellule granulari, hanno constatato che il rilascio di noradrenalina riduceva fortemente la tendenza di queste cellule a sparare. Questa soppressione si è vista sia a livello di singoli neuroni sia nei segnali di popolazione, ed è stata riprodotta semplicemente immergendo fette di tessuto nella noradrenalina. Il blocco dei recettori della noradrenalina ha eliminato l’effetto, dimostrando che dipendeva davvero da questo messaggero chimico.
Non meno eccitazione, ma freni più potenti
Per capire come la noradrenalina silenziasse le cellule granulari, il team ha controllato le possibilità ovvie. Non ha modificato in modo significativo la tensione di riposo o la resistenza d’ingresso delle cellule granulari, il che significa che la loro eccitabilità di base è rimasta più o meno la stessa. Né ha indebolito le correnti eccitatorie che queste cellule ricevono dalla corteccia entorinale. Invece, quando hanno bloccato i recettori GABAA, che mediano l’inibizione, la noradrenalina non è più riuscita a sopprimere l’attività delle cellule granulari. Misurazioni dettagliate delle correnti hanno mostrato che la noradrenalina potenziava selettivamente una forma rapida di inibizione feedforward: i segnali eccitatori in arrivo attivavano prima un insieme di interneuroni, che poi inibivano rapidamente le cellule granulari prima che queste potessero generare potenziali d’azione. Analisi temporali hanno rivelato che questa corrente inibitoria sensibile alla noradrenalina arrivava subito dopo l’eccitazione diretta, ma prima che la popolazione principale di cellule granulari sparasse, un tratto distintivo dei freni feedforward.
Interneuroni specializzati che impongono il timing
Quali interneuroni fornivano questa inibizione cruciale? Sorprendentemente, le cellule che esprimono parvalbumina, a lungo ritenute dominanti nel controllo rapido feedforward, non erano responsabili—la noradrenalina le rendeva in realtà meno attive. I protagonisti chiave erano invece gli interneuroni che esprimono colecistochinina (cellule CCK). Queste cellule ricevono input diretti dalle stesse fibre corticali che eccitano le cellule granulari e sparano appena prima di esse, indicando un ruolo feedforward. La noradrenalina depolarizzava le cellule CCK, rendendole più facilmente reclutabili, e aumentava la frequenza con cui gli input le attivavano, senza cambiare la forza di ciascuna singola connessione inibitoria. Quando i ricercatori bloccarono farmacologicamente l’output delle cellule CCK, la noradrenalina non riuscì più a sopprimere l’attività delle cellule granulari. Di fatto, la noradrenalina attiva un circuito di interneuroni CCK che impone una finestra temporale molto stretta durante la quale i spike eccitatori in arrivo possono effettivamente attivare le cellule granulari.
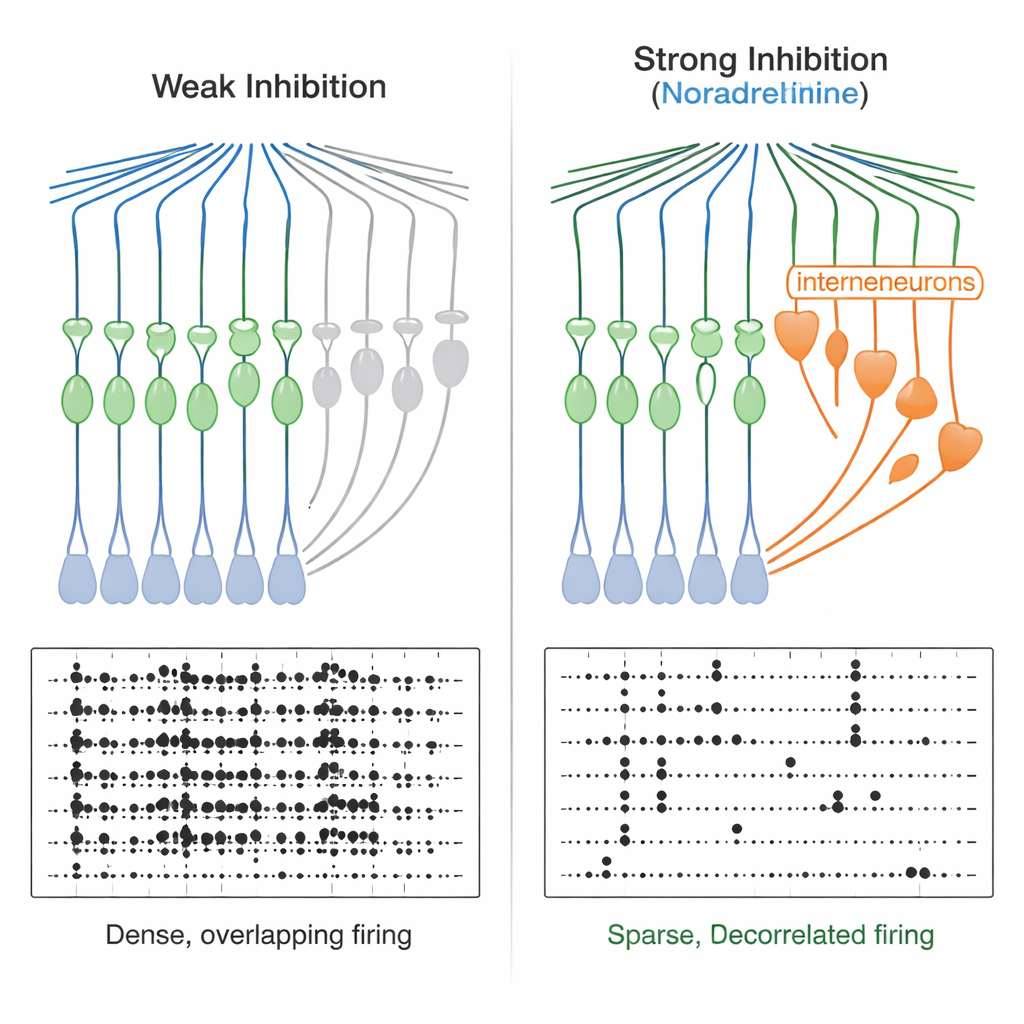
Dalle finestre strette a codici mnemonici più puliti
Questo affinamento del timing ha conseguenze potenti. Quando il team ha somministrato coppie di brevi input eccitatori, ha scoperto che in condizioni normali le cellule granulari potevano integrare input separati da decine di millisecondi in uno spike. Con la noradrenalina presente, la finestra si è ridotta a pochi millisecondi—le cellule granulari rispondevano quasi esclusivamente a input altamente sincronizzati. Modelli computazionali di rete hanno confermato che rendere l’inibizione feedforward più forte e più rapida produceva un output più sparso e riduceva le sovrapposizioni tra schemi di attività, migliorando la “decorrelazione”. Sperimenticamente, quando i ricercatori hanno inviato nel giro dentato due pattern di input simili, ma non identici, le cellule granulari hanno risposto con schemi di scarica più distinti in presenza di noradrenalina, sia nelle registrazioni a singola cellula sia nell’imaging del calcio su molte cellule. Contemporaneamente, l’attività complessiva delle cellule granulari è diventata più sparsa.
Come l’eccitazione può aiutarci a separare ricordi simili
Per il lettore non esperto, la conclusione è che la noradrenalina, rilasciata quando siamo all’erta o emotivamente coinvolti, aiuta un importante filtro mnemonico nell’ippocampo a diventare più selettivo. Energizzando una specifica classe di cellule inibitorie, restringe la finestra temporale durante la quale gli input possono attivare le cellule granulari, così soltanto segnali strettamente sincronizzati e significativi passano. Questo riduce l’attività complessiva, rende i pattern di attività meno sovrapposti e aiuta il cervello a memorizzare esperienze simili—come due aule o due conversazioni—come ricordi separati anziché un’unica macchia confusa. Il lavoro rivela un meccanismo di circuito concreto che collega l’eccitazione momentanea a ricordi più precisi e meno confondibili.
Citazione: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Parole chiave: noradrenalina, giro dentato, interneuroni inibitori, separazione dei pattern, memoria episodica