Clear Sky Science · it
Approfondimenti strutturali sull’elica WRN rivelano stati conformazionali e opportunità per la scoperta di farmaci contro i tumori MSI‑H
Perché questo è importante per il trattamento del cancro
Alcuni tumori hanno una debolezza intrinseca: faticano a riparare gli errori nel loro DNA. Una proteina chiamata elicasi WRN funziona come uno strumento molecolare di riparazione che mantiene in vita questi tumori fragili. Questo studio rivela, a livello atomico, come WRN si muove lungo il DNA e come farmaci sperimentali possano incepparne il moto — offrendo una mappa per nuovi trattamenti che uccidono selettivamente queste cellule tumorali vulnerabili risparmiando il tessuto sano.
Il tuttofare del DNA sotto il microscopio
L’elicasi WRN fa parte della squadra di manutenzione della cellula, aiutando a svolgere il DNA affinché il danno possa essere individuato e riparato. Le persone nate senza una WRN funzionante sviluppano la sindrome di Werner, una rara patologia caratterizzata da invecchiamento precoce, che mostra quanto questa proteina sia cruciale per la conservazione del genoma. I tumori con “instabilità dei microsatelliti elevata” (MSI‑H) — un difetto comune nel cancro del colon-retto e in altri tumori — si rivelano particolarmente dipendenti da WRN. Quando WRN viene disattivata in queste cellule, il loro DNA già instabile collassa rapidamente e le cellule tumorali muoiono. Ciò rende WRN un bersaglio farmaceutico interessante, ma fino ad ora mancava una visione chiara di come la proteina cambi forma mentre afferra il DNA, consuma carburante chimico e si muove lungo il materiale genetico.
Osservare WRN flettersi e respirare
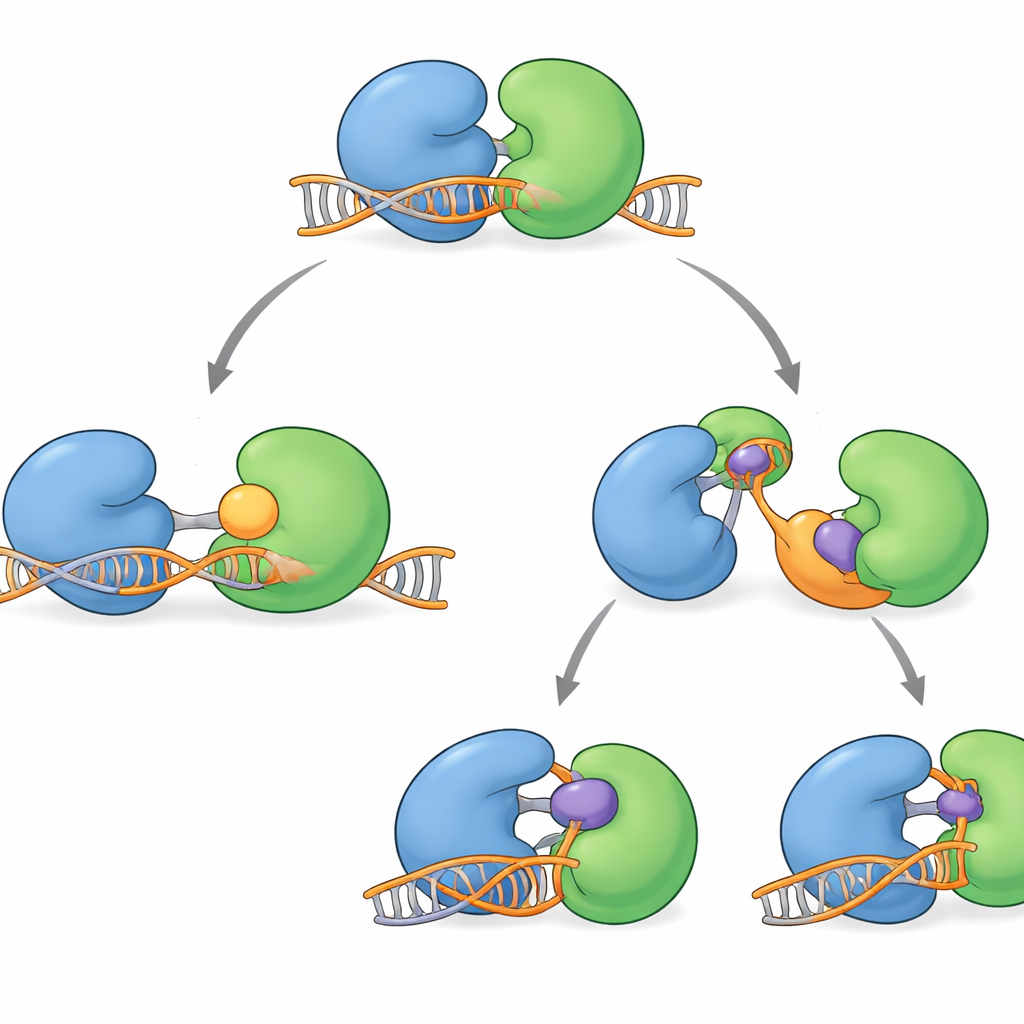
Gli autori hanno usato la cristallografia a raggi X per catturare diversi “istantanei” ad alta risoluzione del nucleo dell’elicasi WRN umana. Hanno risolto strutture di WRN isolata e di WRN legata a DNA a filamento singolo e a una molecola di carburante simile all’ATP non degradabile. Queste immagini hanno rivelato che la proteina è composta da due lobi principali collegati da una cerniera flessibile che si comporta come un’articolazione che «respira». Nel suo stato di riposo, privo di carburante, WRN adotta una forma compatta «chiusa» in cui i lobi stanno vicini. Quando sono presenti una molecola simile all’ATP e il DNA, i lobi si allontanano assumendo una configurazione più «aperta» che può accogliere il DNA in una gola carica positivamente. Un piccolo anello aromatico all’interno di WRN si rimodella in un breve elica e si inserisce tra le basi del DNA, agendo come un cricchetto che aiuta la proteina a fare passi in avanti senza scivolare indietro.
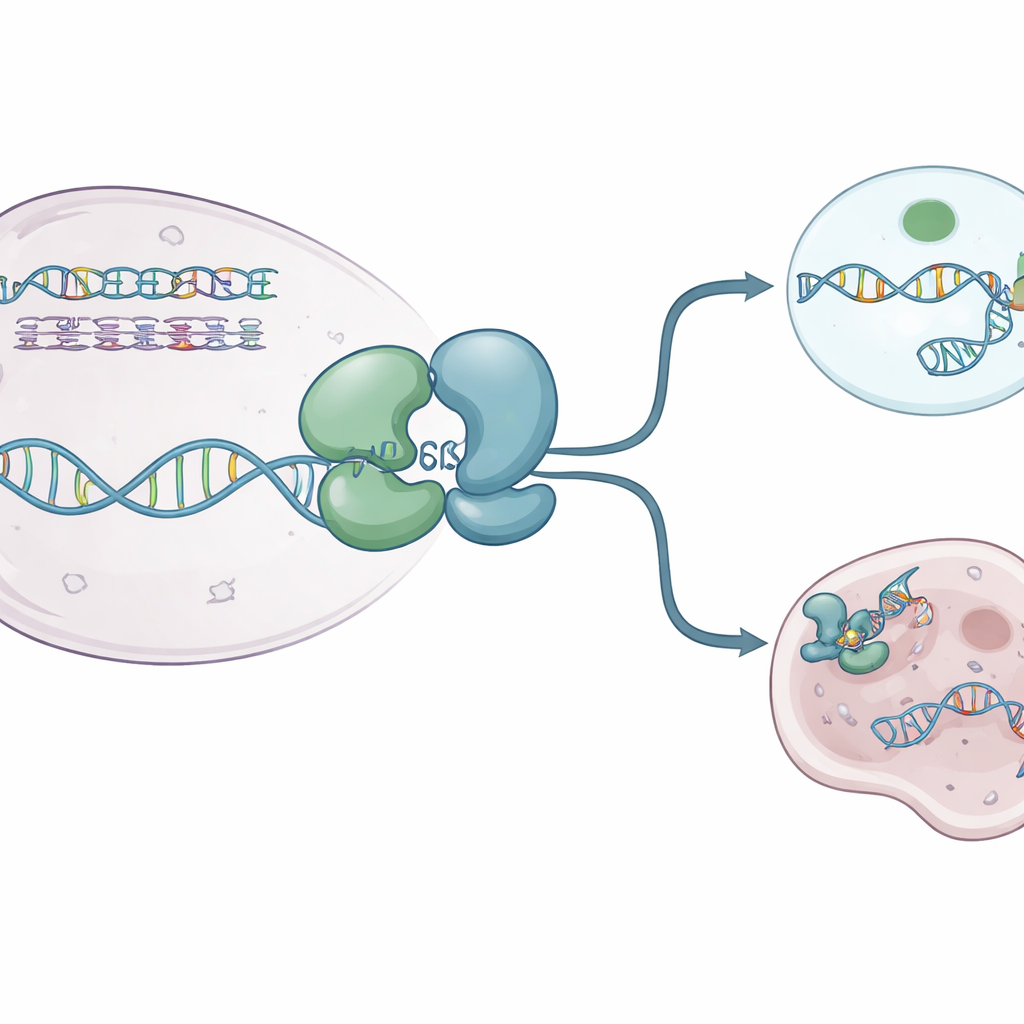
Come gli attuali farmaci spengono WRN
Diversi composti che bloccano WRN sono recentemente entrati in sperimentazioni cliniche. Non ostruiscono direttamente la gola attiva della proteina. Agiscono invece a distanza, aggrappandosi alla regione della cerniera e bloccando WRN in conformazioni che non possono interagire correttamente con il DNA. Alcune molecole, come HRO761 e un candidato clinico correlato di GSK, ruotano un lobo di circa 180 gradi rispetto all’altro, creando una forma «torcigliata» che si posiziona lontano dal DNA. Altre, inclusi VVD‑133214 e un composto strettamente correlato studiato qui, fissano WRN in un assetto strettamente «chiuso» che non espone le superfici chiave per afferrare il DNA. Esperimenti biofisici hanno confermato che quando questi farmaci sono legati, WRN non può più formare un complesso stabile con il DNA a filamento singolo, interrompendo efficacemente il collegamento tra l’uso di ATP e lo svolgimento del DNA.
Come le cellule tumorali imparano a sfuggire
Per capire come i tumori possano eludere questi farmaci, il team ha coltivato cellule di carcinoma colorettale MSI‑H in presenza di inibitori di WRN per settimane o mesi. Sono emerse popolazioni resistenti rapidamente. L’analisi genetica ha mostrato che, in ogni caso, le cellule avevano acquisito una singola e precisa modifica nel gene WRN vicino alla cerniera di legame del farmaco. Una mutazione ha indebolito l’effetto dell’inibitore che induce lo «stato torcigliato» HRO761, mentre una diversa mutazione ha ridotto la sensibilità a VVD‑133214, che favorisce lo stato chiuso. Inoltre, molte cellule resistenti aumentavano la produzione di WRN, ottenendo più copie del bersaglio e diluendo parzialmente l’impatto del farmaco. Questi risultati riecheggiano i modelli di resistenza osservati con altri farmaci oncologici mirati, dove piccoli ritocchi strutturali nella proteina bersaglio o la sovraespressione possono attenuare l’efficacia del trattamento.
Verso inibitori di WRN più intelligenti
Nel complesso, le nuove strutture mappano un intero ciclo operativo di WRN mentre si aggancia al DNA, avanza e poi si resetta. Mostrano anche che i composti clinici attuali stabilizzano principalmente le forme della proteina «fuori dal DNA». Per il lettore generale, il punto chiave è che ora comprendiamo dove WRN è vulnerabile e come i tumori possono adattarsi. Questo suggerisce una nuova ondata di inibitori che si leghino a WRN quando è bloccata sul DNA, intrappolandola in uno stato tossico — in modo simile ai farmaci di successo che intrappolano altri enzimi di riparazione del DNA. Tali bloccanti «on‑DNA» di WRN, usati da soli o in combinazione con agenti esistenti, potrebbero offrire modalità più durature per sfruttare la debolezza nascosta dei tumori MSI‑H.
Citazione: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Parole chiave: elicasi WRN, instabilità dei microsatelliti, riparazione del DNA, inibitori allosterici, resistenza ai farmaci