Clear Sky Science · it
PiR48444 inibisce la differenziazione osteogenica delle MSC e la rigenerazione ossea mediante il targeting della metilazione m6A di BMP2 mediata da METTL7A/eIF4E
Perché le molecole piccole contano per le ossa rotte
Fratture e perdita ossea legata all’età sono problemi comuni e i medici cercano di sfruttare le cellule staminali per aiutare l’organismo a ricostruire lo scheletro danneggiato. Tuttavia queste cellule staminali non sempre formano nuovo tessuto osseo con l’efficienza desiderata, soprattutto nelle persone anziane o in tessuti infiammati. Questo studio individua una piccola molecola di RNA, chiamata piR48444, che funziona come un freno molecolare sulle cellule staminali osteogeniche. Rimuovendo quel freno, i ricercatori mostrano che potrebbe essere possibile potenziare la riparazione ossea e proteggere dalla perdita di massa ossea.
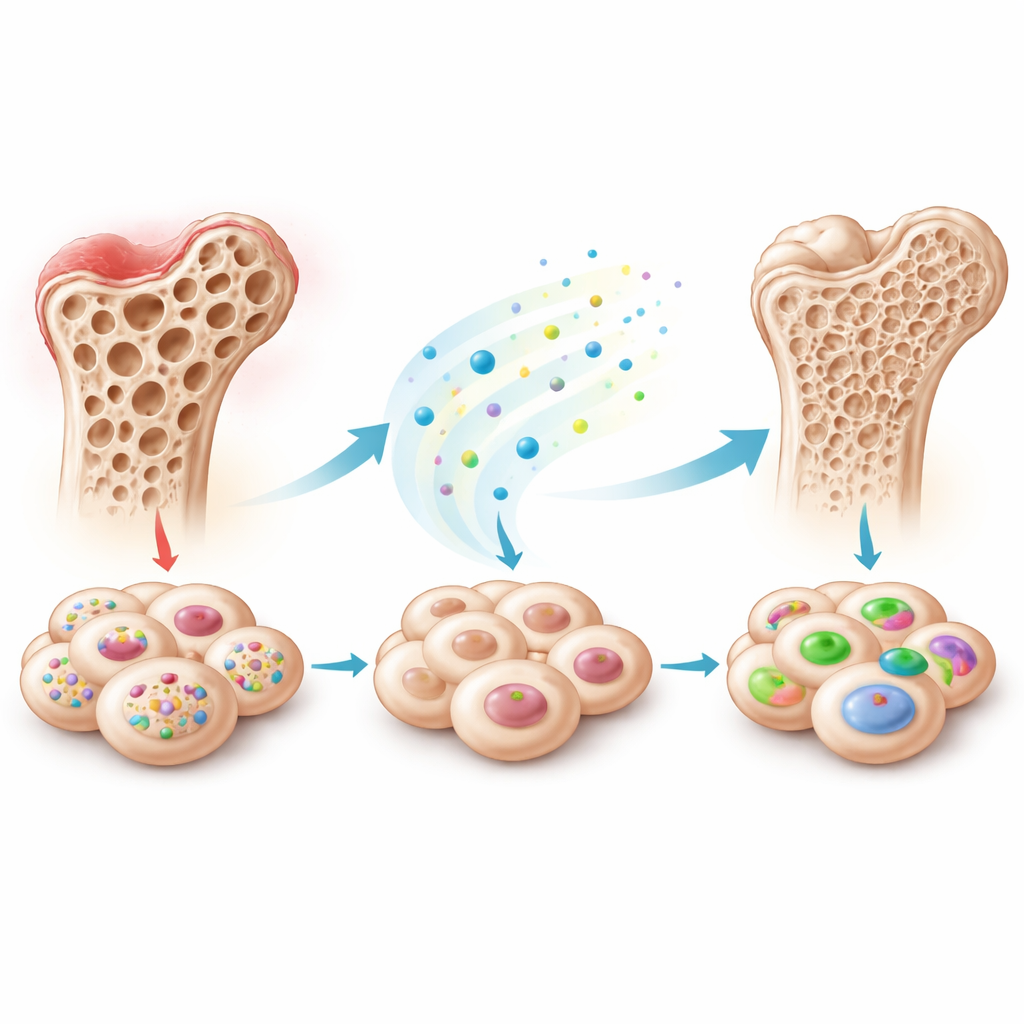
Un freno nascosto all’interno di molti tipi di cellule staminali
Il gruppo si è concentrato sulle cellule staminali mesenchimali, cellule versatili che possono differenziarsi in osso, cartilagine, tessuto adiposo e altro, e che si isolano da tessuti come midollo osseo, denti da latte ed adipe. Quando queste cellule vengono indirizzate a diventare osso in laboratorio, migliaia di geni e piccoli RNA modificano la loro attività. Sequenziando queste molecole in cellule staminali ricavate da denti da latte esfoliati, i ricercatori hanno osservato che un particolare piccolo RNA, piR48444, diminuiva progressivamente man mano che le cellule si orientavano verso l’osteogenesi. Hanno poi verificato altri tipi di cellule staminali e visto lo stesso schema: le cellule che producevano più osso presentavano meno piR48444, suggerendo che questa molecola potrebbe normalmente limitare la loro capacità di formare osso.
Dalle piastre di laboratorio alle ossa viventi
Per mettere alla prova questa ipotesi, gli scienziati hanno alterato i livelli di piR48444 in diversi tipi di cellule staminali. Quando hanno ridotto piR48444, le cellule depositavano più calcio, attivavano geni associati all’osso e assumevano un aspetto più simile a tessuto osseo immaturo al microscopio. Forzando invece la produzione di piR48444, si osservava l’effetto opposto: l’attività legata all’osso diminuiva. Il team è poi passato a modelli animali. Cellule staminali con piR48444 spento sono state utilizzate per riempire piccoli difetti cranici nei topi. Queste cellule modificate hanno prodotto molto più nuovo osso rispetto alle cellule di controllo, come evidenziato da scansioni 3D ai raggi X e da colorazioni tissutali, suggerendo che bloccare piR48444 può migliorare concretamente la riparazione ossea negli organismi viventi.
Proteggere ossa fragili nelle malattie e nell’invecchiamento
La perdita ossea non è causata solo da lesioni, ma anche da infiammazione e invecchiamento. Nelle cellule staminali del midollo esposte a tossine batteriche e nelle cellule staminali provenienti da animali anziani, i livelli di piR48444 erano insolitamente elevati mentre i marcatori di formazione ossea risultavano bassi. I ricercatori hanno creato un "antagomir" — una breve molecola progettata per neutralizzare piR48444 nel circolo sanguigno — e l’hanno iniettato in topi con perdita ossea indotta da infiammazione o in topi naturalmente anziani. In entrambi i modelli, gli animali trattati hanno mantenuto molta più parte spugnosa dell’osso interno, con travicelli ossei più densi e numerosi, mentre la corticale esterna è rimasta sostanzialmente invariata. Ciò indica che bloccare piR48444 può proteggere selettivamente la porzione di scheletro più fragile e metabolicamente attiva, quella maggiormente vulnerabile durante l’invecchiamento e l’infiammazione cronica.
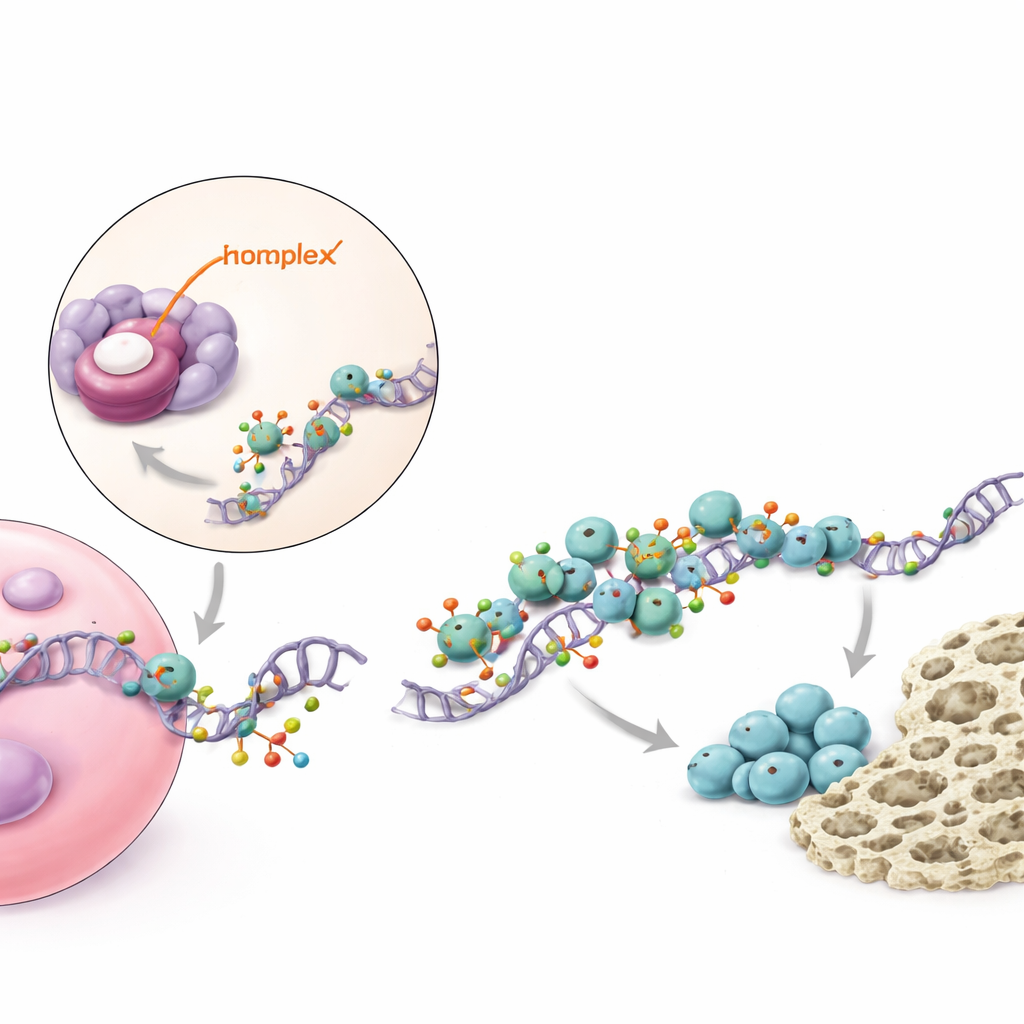
Un relè molecolare che amplifica un segnale chiave per l’osso
Approfondendo i meccanismi, lo studio ha mappato come piR48444 esercita i suoi effetti all’interno delle cellule. Il piccolo RNA si lega e sopprime una proteina chiamata METTL7A, che agisce come un enzima che modifica gli mRNA che portano il codice per BMP2, un noto fattore di crescita che stimola fortemente la formazione ossea. METTL7A aggiunge piccole modifiche chimiche ai messaggi di BMP2, rendendoli più stabili e più facilmente tradotti dalla macchina proteica della cellula. METTL7A coopera inoltre con un’altra proteina, eIF4E, che aiuta a iniziare la produzione proteica. Quando piR48444 è abbondante, METTL7A viene inibito, meno messaggi di BMP2 sono modificati e tradotti, e viene prodotta meno proteina BMP2, perciò le cellule staminali sono meno propense a diventare osso. Quando piR48444 viene bloccato, METTL7A e BMP2 aumentano, spingendo le cellule verso l’osteogenesi.
Cosa significa per la riparazione ossea futura
In termini semplici, gli autori rivelano una catena di controllo in cui un piccolo RNA (piR48444) attenua un enzima ausiliario (METTL7A), che a sua volta limita un potente segnale osteogenico (BMP2). Interrompendo questa catena a livello di piR48444, si può rendere più efficiente la formazione di osso da parte di varie cellule staminali e ridurre la perdita ossea nei topi. Sebbene siano necessari ulteriori test su sicurezza, effetti off‑target e risultati a lungo termine, il lavoro indica piR48444 sia come possibile marcatore ematico del rischio di osteoporosi sia come promettibile bersaglio farmacologico per potenziare la rigenerazione ossea basata su cellule staminali in ambito clinico.
Citazione: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Parole chiave: rigenerazione ossea, cellule staminali mesenchimali, osteoporosi, RNA non codificante, segnalazione BMP2