Clear Sky Science · it
Valutazione della qualità dei modelli 3D dell’RNA mediante deep learning e mappe 2D intermedie
Perché è importante valutare le forme dell’RNA
All’interno di ogni cellula, le molecole di RNA si piegano e si ripiegano in complesse forme tridimensionali che controllano quali geni vengono attivati, guidano reazioni chimiche e persino difendono contro i virus. Oggi potenti programmi informatici possono prevedere molte di queste forme, ma i ricercatori si trovano ancora davanti a un problema fondamentale: quando il computer genera dozzine o centinaia di forme candidate per lo stesso RNA, quale di queste è davvero vicina alla realtà? Questo articolo presenta RNArank, uno strumento di intelligenza artificiale progettato per affrontare questa domanda valutando i modelli 3D dell’RNA, come un ispettore della qualità strutturale, in modo che gli scienziati possano concentrarsi sulle previsioni più affidabili.
Un nuovo ispettore per i modelli di RNA
RNArank è costruito per giudicare la qualità di una forma proposta di RNA senza bisogno di sapere come quella forma sia stata prodotta. Che il modello provenga da un sistema di deep learning, da una simulazione basata sulla fisica o da un esperto umano, RNArank considera solo le coordinate 3D finali. Si chiede, in pratica, “Questa struttura assomiglia a un RNA realistico?” Questo tipo di valutazione indipendente è essenziale perché, a differenza del mondo delle proteine dove strumenti come AlphaFold spesso forniscono risposte molto affidabili già di base, la previsione dell’RNA beneficia ancora della combinazione di più metodi e dell’intuizione umana — e di un modo intelligente per classificare i modelli risultanti.
Insegnare all’IA come appare un buon RNA
Per addestrare RNArank, gli autori hanno raccolto circa 200.000 strutture di RNA, coprendo un ampio spettro da chiaramente errate a quasi perfette. Queste sono state ottenute a partire da strutture sperimentali note usando una grande varietà di approcci, inclusi predittori moderni basati su deep learning, simulazioni di dinamica molecolare che imitano il movimento atomico e distorsioni deliberate di strutture accurate per creare “esche” (decoy). Per ciascun modello, il gruppo ha calcolato quanto fosse vicino alla struttura reale determinata sperimentalmente, usando un punteggio di accuratezza affinato per l’RNA denominato lDDT_RNA. Questo punteggio si concentra su quanto bene vengono riprodistate le distanze tra coppie di nucleotidi, catturando sia il ripiegamento complessivo sia i dettagli locali senza essere eccessivamente sensibile alla lunghezza della molecola.
Come RNArank legge e valuta un RNA
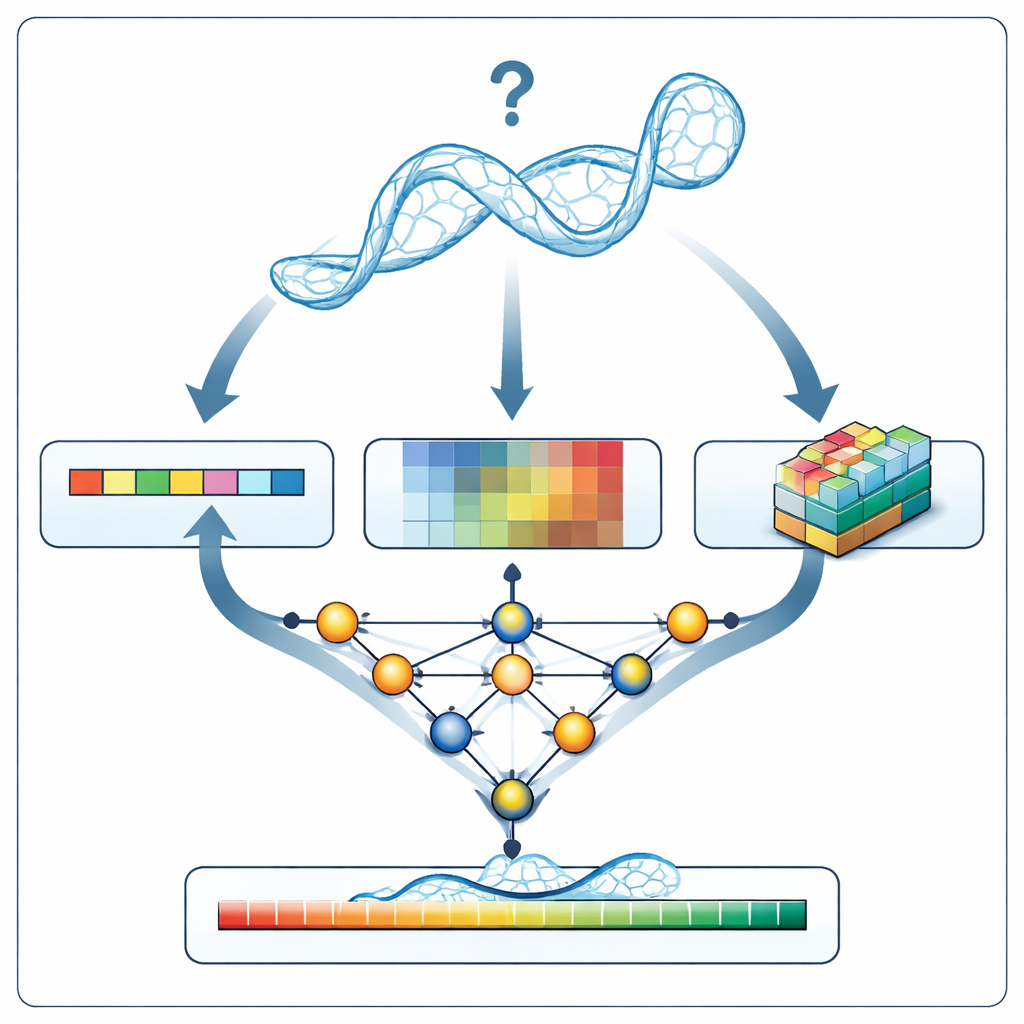
Quando RNArank esamina un nuovo modello di RNA, prima traduce la struttura in tre tipi di informazioni: una descrizione 1D della sequenza e della geometria dello scheletro lungo la catena, descrizioni 2D di come ogni coppia di nucleotidi è correlata (le loro distanze, le energie di interazione stimate e possibili clash atomici) e istantanee 3D “voxel”, piccole griglie che catturano la nube locale di atomi attorno a ciascun nucleotide. Una rete neurale multipartita intreccia questi indizi in un quadro unificato e poi predice due mappe 2D intermedie: quali nucleotidi sono probabilmente in contatto e quanto ogni distanza modellata è probabile che si discosti dalla struttura vera sconosciuta. Da queste mappe, RNArank ricostruisce sia un punteggio di confidenza per nucleotide sia un punteggio complessivo per l’intero modello di RNA.
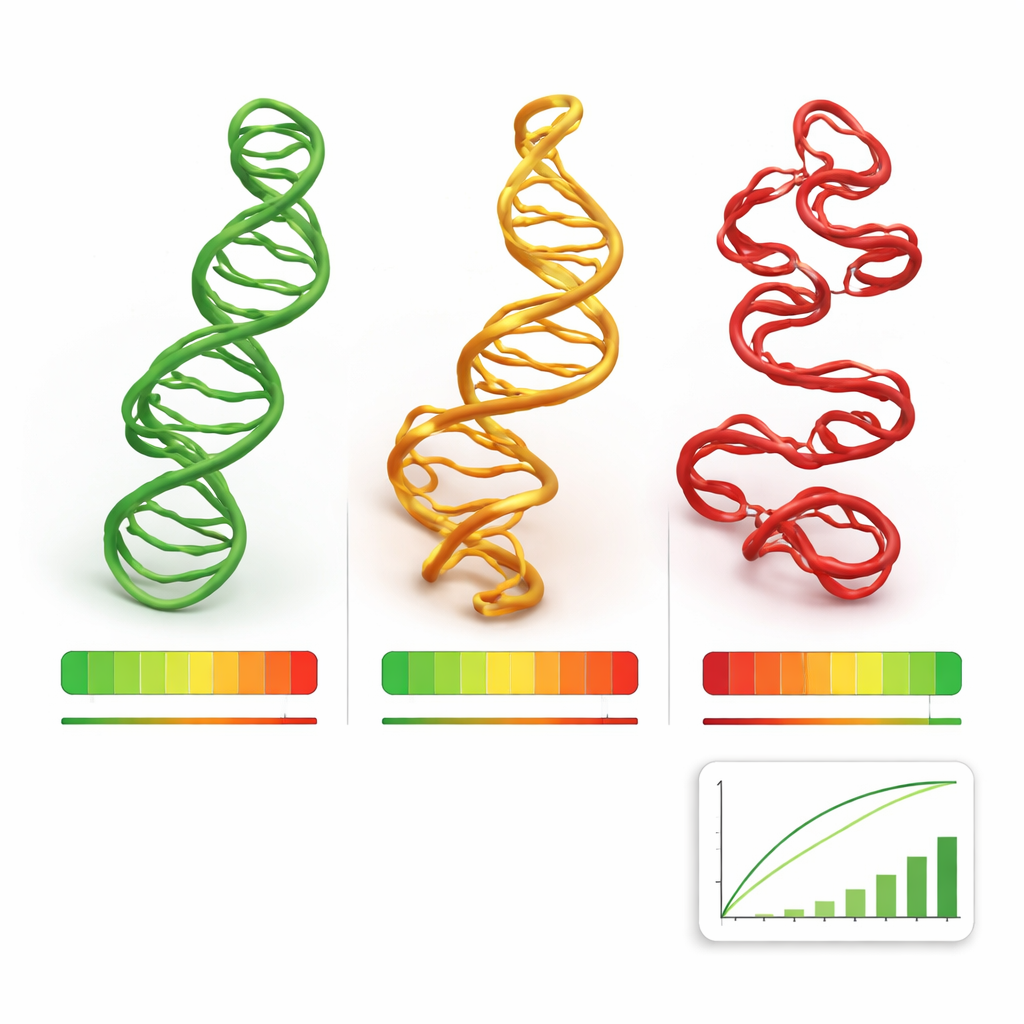
Mettere il metodo alla prova
Il gruppo ha valutato RNArank su tre set di dati impegnativi: un insieme di 24 RNA recentemente risolti provenienti dal Protein Data Bank e gli obiettivi RNA di due contest internazionali di predizione alla cieca, CASP15 e CASP16, dove molti team presentano modelli senza conoscere le risposte in anticipo. Su migliaia di strutture candidate, i punteggi di RNArank hanno seguito la qualità reale dei modelli più da vicino rispetto a diversi metodi consolidati basati sull’energia e ad altri approcci di deep learning. Si è dimostrato particolarmente efficace nel selezionare i modelli migliori o quasi migliori da un pool e nell’identificare quali parti di una struttura erano probabilmente inaffidabili. Gli autori hanno anche mostrato che RNArank manteneva le sue prestazioni anche su RNA chiaramente diversi nella sequenza rispetto a quelli visti durante l’addestramento, segno di una vera generalizzazione piuttosto che di memorizzazione.
Limiti attuali e prospettive future
RNArank non è perfetto: fatica ancora con RNA particolarmente flessibili che adottano molte conformazioni e con RNA che cambiano forma quando sono vincolati da proteine all’interno di grandi macchine molecolari. Tuttavia è sufficientemente rapido da gestire molti modelli per RNA di alcune centinaia di nucleotidi in pochi secondi, e già aiuta server automatizzati a scegliere previsioni di qualità superiore nei test comunitari. Fornendo un giudice indipendente dal metodo e basato solo sulla struttura per i modelli di RNA, RNArank offre ai biologi un filtro più netto per trasformare l’output grezzo dei computer in ipotesi strutturali affidabili, avvicinando il campo a previsioni delle forme di RNA più routinarie e affidabili e, di conseguenza, a una comprensione più profonda di come funzionano queste molecole versatili.
Citazione: Liu, X., Wang, W., Du, Z. et al. Quality assessment of RNA 3D structure models using deep learning and intermediate 2D maps. Commun Biol 9, 293 (2026). https://doi.org/10.1038/s42003-026-09582-2
Parole chiave: Struttura 3D dell’RNA, deep learning, valutazione della qualità dei modelli, bioinformatica strutturale, RNArank