Clear Sky Science · it
Un blando bloccaggio di cationi locale deforma e ammorbidisce il duplex di RNA
Perché questa piccola torsione nell'RNA conta
All'interno di ogni cellula, DNA e RNA vengono costantemente piegati, allungati e torcigliati mentre immagazzinano e usano l'informazione genetica. Questi movimenti non sono solo dettagli meccanici: regolano come i geni vengono letti, come i virus si replicano e come funzioneranno nuovi farmaci e nanodispositivi a base di RNA. Questo studio mostra che semplici sali composti da ioni carichi positivamente e negativamente possono cambiare in modo marcato quanto l'RNA sia rigido o flessibile, e che l'RNA risponde in modo molto diverso rispetto al DNA. Capire questa sottile danza di “ammorbidimento e irrigidimento” potrebbe aiutare gli scienziati a progettare meglio farmaci a base di RNA, vaccini e strumenti molecolari.
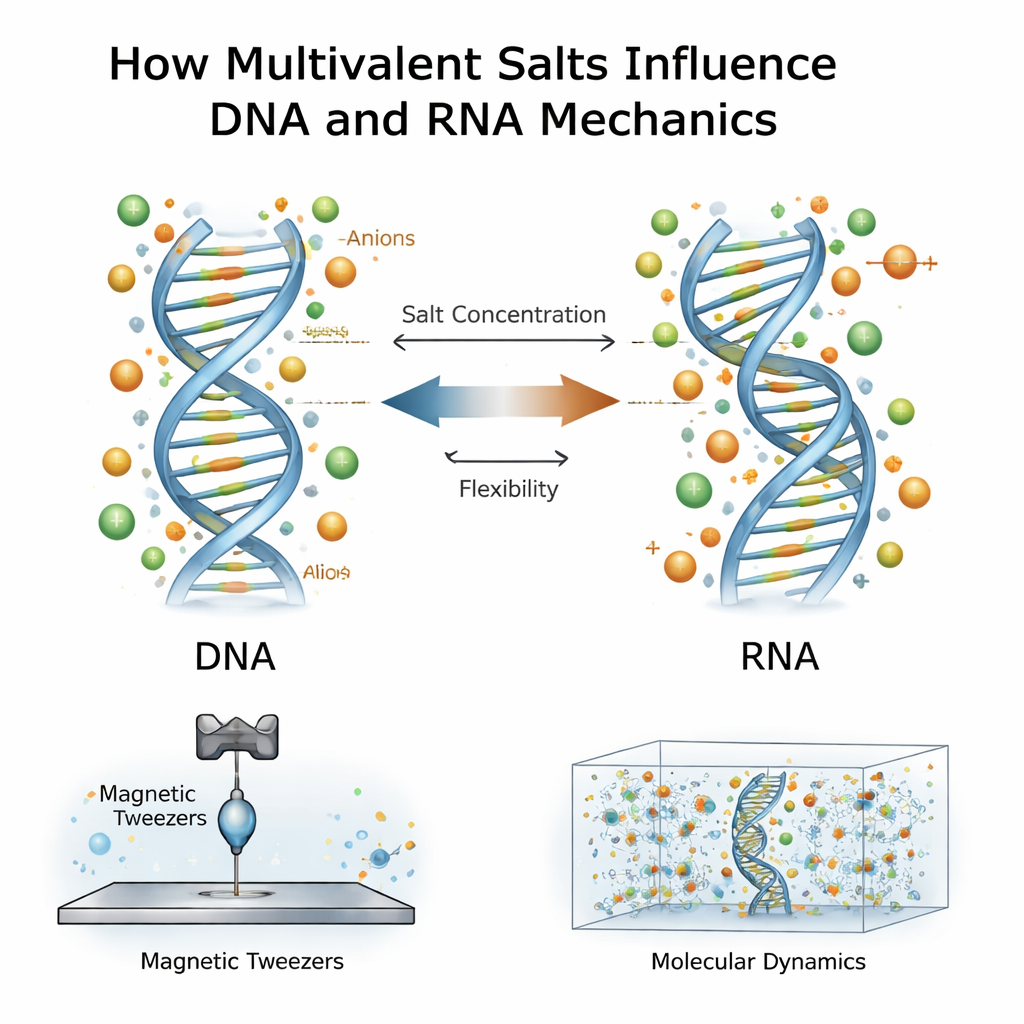
Ambienti salini e molecole genetiche
DNA e RNA portano una forte carica elettrica negativa, quindi sono circondati in acqua da nuvole di ioni con carica opposta. La maggior parte dei lavori precedenti si è concentrata sugli ioni positivi, specialmente quelli multivalenti che portano due o tre cariche positive, come il magnesio o la spermidina. Si sa che questi ioni tengono insieme i filamenti di DNA, li condensano o ne modificano la facilità di piegatura. L'RNA, pur essendo chimicamente simile al DNA, si comporta differentemente: in genere è più difficile da piegare ma più facile da allungare. Il nuovo lavoro pone una domanda più profonda: cosa succede quando sia gli ioni positivi sia i loro partner negativi — chiamati anioni — interagiscono con DNA e RNA a livelli di sale molto elevati, molto più alti di quelli tipici nelle cellule?
Tirando singole molecole per misurarne la rigidezza
I ricercatori hanno usato una tecnica chiamata pinzette magnetiche per allungare individualmente eliche doppie di DNA o RNA una alla volta. Ogni molecola era ancorata a una superficie di vetro a un'estremità e a una minuscola sfera magnetica all'altra. Muovendo magneti sopra il campione potevano tirare con forze controllate e registrare quanto si estendeva ciascuna molecola e come si torceva sotto tensione. Da queste curve forza–estensione hanno estratto quattro caratteri meccanici chiave: quanto è difficile piegare la molecola, quanto è difficile allungarla, la sua lunghezza efficace per coppia di basi e come la torsione ne cambia la lunghezza. Hanno ripetuto queste misure su un ampio intervallo di concentrazioni di sali multivalenti per diversi sali, inclusi spermidina e cloruro di calcio.
Il DNA si irrigidisce di nuovo, ma l'RNA si ammorbidisce all'improvviso
Per il DNA, il comportamento è stato in gran parte quello previsto. Con l'aumentare della concentrazione di ioni positivi multivalenti, il DNA prima diventava più facile da piegare — la sua rigidità diminuiva — perché gli ioni neutralizzavano la sua carica negativa. A livelli ancora più alti, l'eccesso di ioni positivi sovracompensava, ribaltando effettivamente la carica netta del DNA. Questa “inversione di carica” rendeva di nuovo il DNA più difficile da piegare, quindi la sua rigidità aumentava. Sorprendentemente, l'RNA ha mostrato lo schema opposto e più drammatico. A livelli di sale da bassi a moderati, la sua rigidità alla piegatura aumentava: il duplex di RNA diventava più dritto e più rigido. Ma a concentrazioni molto elevate, la rigidità alla piegatura dell'RNA è calata di oltre la metà, e altre proprietà come la sua elasticità all'allungamento e il comportamento torsione–allungamento sono cambiate in modi inaspettati.
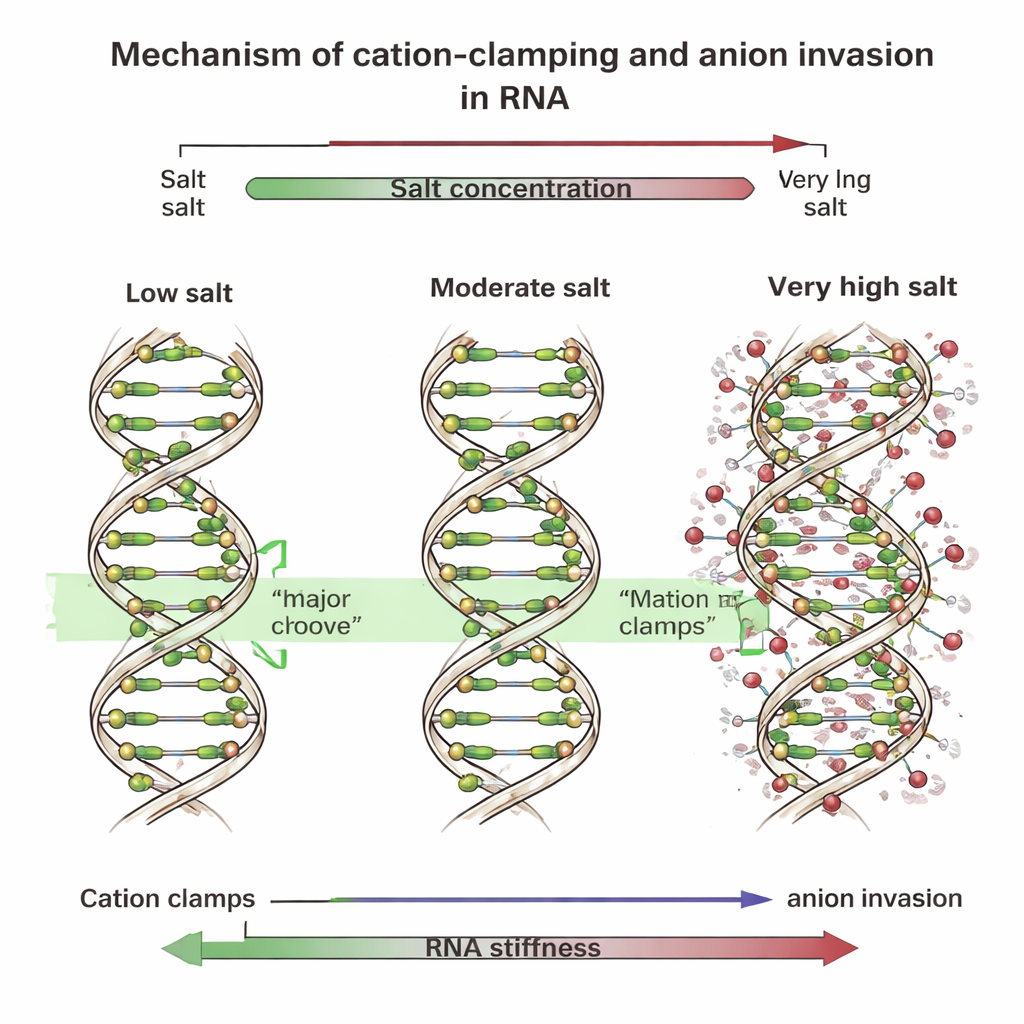
Morsetti, solchi e ioni invasivi
Per scoprirne la causa, il team ha eseguito dettagliate simulazioni al computer che tracciavano ogni atomo di brevi frammenti di DNA e RNA in acqua salina. Queste simulazioni hanno rivelato che a concentrazioni basse e moderate gli ioni positivi multivalenti si sistemano in una vasta superficie dell'RNA chiamata solco maggiore. Lì formano “morsetti di cationi” che fanno da ponte attraverso il solco, avvicinando i suoi lati, raddrizzando l'elica e rendendola più rigida. Il DNA, i cui solchi hanno forma diversa, lega principalmente questi ioni lungo la spina dorsale esterna. Tuttavia, a livelli di sale molto elevati, molti ioni negativi — come il cloruro — si avvicinano strettamente alla spina dorsale dell'RNA e perfino all'interno del solco maggiore. La loro presenza interrompe i morsetti ordinati, spezzandoli in “morsetti locali” irregolari e a chiazze che deformano l'elica. Quando i ricercatori hanno riprodotto questo effetto aggiungendo molle artificiali o bloccando ioni negativi extra vicino all'RNA nelle simulazioni, la spina dorsale dell'RNA si è incurvata di più e la rigidità complessiva è crollata, proprio come osservato negli esperimenti.
Cosa significa per le future tecnologie basate sull'RNA
In termini semplici, lo studio mostra che l'RNA può essere reso o più dritto e rigido o più piegato e flessibile semplicemente cambiando il tipo e la concentrazione dei sali circostanti. A livelli moderati di ioni multivalenti, le cariche positive bloccano ordinatamente la superficie dell'RNA e lo rinforzano; a livelli estremi, gli ioni negativi invasivi rompono quel rinforzo uniforme e creano regioni deformate e più morbide. Il DNA non mostra questo netto ammorbidimento perché lega gli ioni in modo diverso e invece subisce un'inversione netta di carica. Queste intuizioni sottolineano che non sono importanti solo gli ioni positivi ma anche i loro partner negativi per controllare la forma dell'RNA. Questa conoscenza aiuterà i ricercatori a sintonizzare deliberatamente la meccanica dell'RNA in laboratorio — per esempio, per stabilizzare farmaci a base di RNA, controllare come l'RNA si ripiega in biosensori o progettare nanostrutture a base di RNA più affidabili.
Citazione: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Parole chiave: Meccanica dell'RNA, ioni multivalenti, bloccaggio di cationi, DNA versus RNA, effetti del sale