Clear Sky Science · it
CISH, un importante checkpoint intracellulare, a confronto e in combinazione con i checkpoint immunitari antitumorali esistenti ed emergenti
Rilasciare i freni delle cellule che combattono il cancro
Le immunoterapie oncologiche hanno cambiato le prospettive per molti pazienti, ma una larga parte delle persone ottiene ancora poco o nessun beneficio. Questo studio esplora un nuovo modo per potenziare le cellule T—i sicari del sistema immunitario—disattivando un “freno” interno chiamato CISH. A differenza dei farmaci attuali che agiscono su interruttori sulla superficie cellulare, questa strategia prende di mira un sistema di controllo sepolto all’interno della cellula, con l’obiettivo di rendere le cellule T ingegnerizzate molto più efficaci nel localizzare e distruggere i tumori, anche quando i tumori cercano di nascondersi.
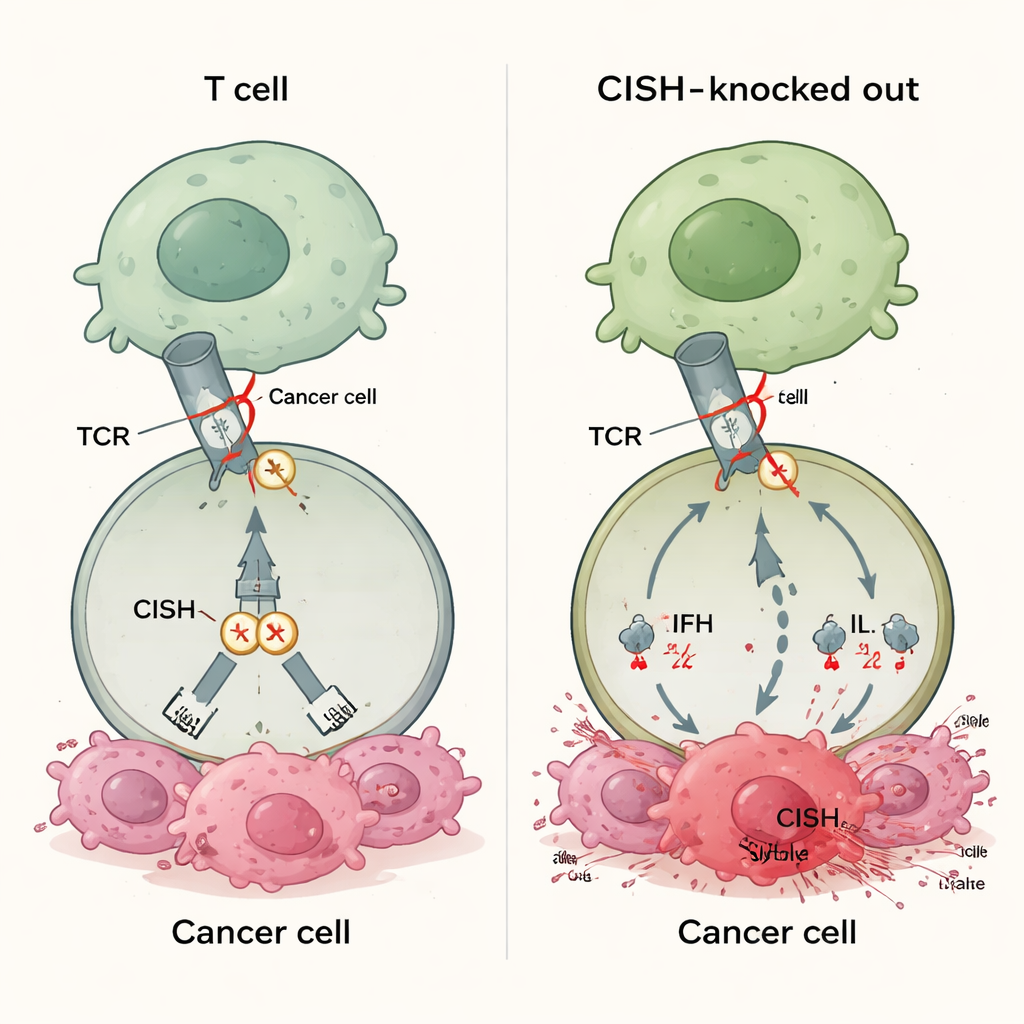
Un nuovo tipo di freno immunitario
La maggior parte dei farmaci immunoterapici approvati blocca proteine come PD-1 sulla superficie delle cellule T. Questi farmaci funzionano solo quando i tumori esprimono molecole partner corrispondenti come PD-L1, e molti tumori o non esprimono mai quantità sufficienti di questi partner o le perdono col tempo. Ciò contribuisce a spiegare perché il 30–60% dei pazienti non risponde alle terapie basate sui checkpoint attuali. CISH appartiene a una classe diversa di freni che si trovano all’interno della cellula T. Viene attivato quando il recettore della cellula T percepisce un bersaglio, quindi attenua il segnale promuovendo la degradazione di una proteina chiave della segnalazione. Poiché questa azione non dipende dai ligandi espressi dal tumore, spegnere CISH potrebbe, in linea di principio, potenziare le risposte delle cellule T attraverso molti tipi di cancro, indipendentemente dallo stato di PD-L1 o da altri biomarcatori.
Faccia a faccia con i checkpoint esistenti
I ricercatori hanno usato l’editing genico CRISPR per rimuovere CISH e hanno confrontato le cellule T risultanti con cellule prive di PD-1 o di diversi altri freni intracellulari. Quando hanno stimolato debolmente le cellule T—una condizione pensata per imitare i tumori che mostrano solo basse quantità di antigene—le cellule con CISH eliminato hanno prodotto molte più molecole immunitarie chiave, inclusi interferone-gamma, TNF-alfa e IL-2. Queste cellule erano anche più “polifunzionali”, cioè singole cellule T potevano svolgere diversi compiti contemporaneamente, una caratteristica dell’attività antitumorale potente. Al contrario, la semplice rimozione di PD-1 non ha fornito vantaggi in queste condizioni a basso segnale. In numerosi test, la perdita di CISH ha aumentato in modo più marcato l’attivazione, la capacità di uccisione e la formazione di cellule T a memoria durevole rispetto all’abbattimento di altri checkpoint intracellulari candidati come RASA2, CBLB, SOCS1, REGNASE1, HPK1 o PTPN1/2.
Lavorare insieme ad altri interruttori interni
Poiché la segnalazione delle cellule T è controllata da molte vie sovrapposte, il gruppo ha chiesto se combinare la delezione di CISH con la rimozione di altri freni potesse dare benefici additivi. Utilizzando l’editing CRISPR multiplex, hanno scoperto che eliminare CISH insieme a SOCS1, HPK1 o RASA2 aumentava ulteriormente la produzione di citochine utili sotto stimolazione debole. In un modello tumorale basato su una comune mutazione di KRAS, le cellule T ingegnerizzate con un recettore specifico per KRAS erano più efficaci nell’uccidere le cellule cancerose quando CISH era rimosso, e questo effetto diventava più forte quando la perdita di CISH era associata alla delezione di SOCS1 o RASA2. Questi risultati suggeriscono che CISH controlla un nodo non ridondante nella biologia delle cellule T e può cooperare con partner selezionati per affinare l’uccisione tumorale specifica.
Rendere le cellule CAR-T più resistenti ai tumori sfuggenti
Gli autori si sono poi concentrati su un contesto clinicamente rilevante: le cellule CAR-T dirette contro il marcatore delle cellule B CD19. Hanno creato cellule leucemiche che esprimevano diversi livelli di CD19 per imitare tumori che perdono o riducono i loro bersagli per sfuggire alla terapia. Le cellule CAR-T prive di CISH erano marcantemente migliori nel distruggere le cellule tumorali, anche quando il CD19 era scarso, e secernevano più segnali di attivazione e reclutamento. Allo stesso tempo, rilasciavano quantità inferiori di molecole note per indebolire le cellule T o promuovere la crescita tumorale, come Galectina-1, Galectina-3, 4-1BB solubile, IL-1α e la glicoproteina EMMPRIN/CD147. Nel loro insieme, questi cambiamenti indicano una cellula CAR-T più aggressiva e meno facilmente sopprimibile, particolarmente adatta ad ambienti tumorali ostili e poveri di antigene.
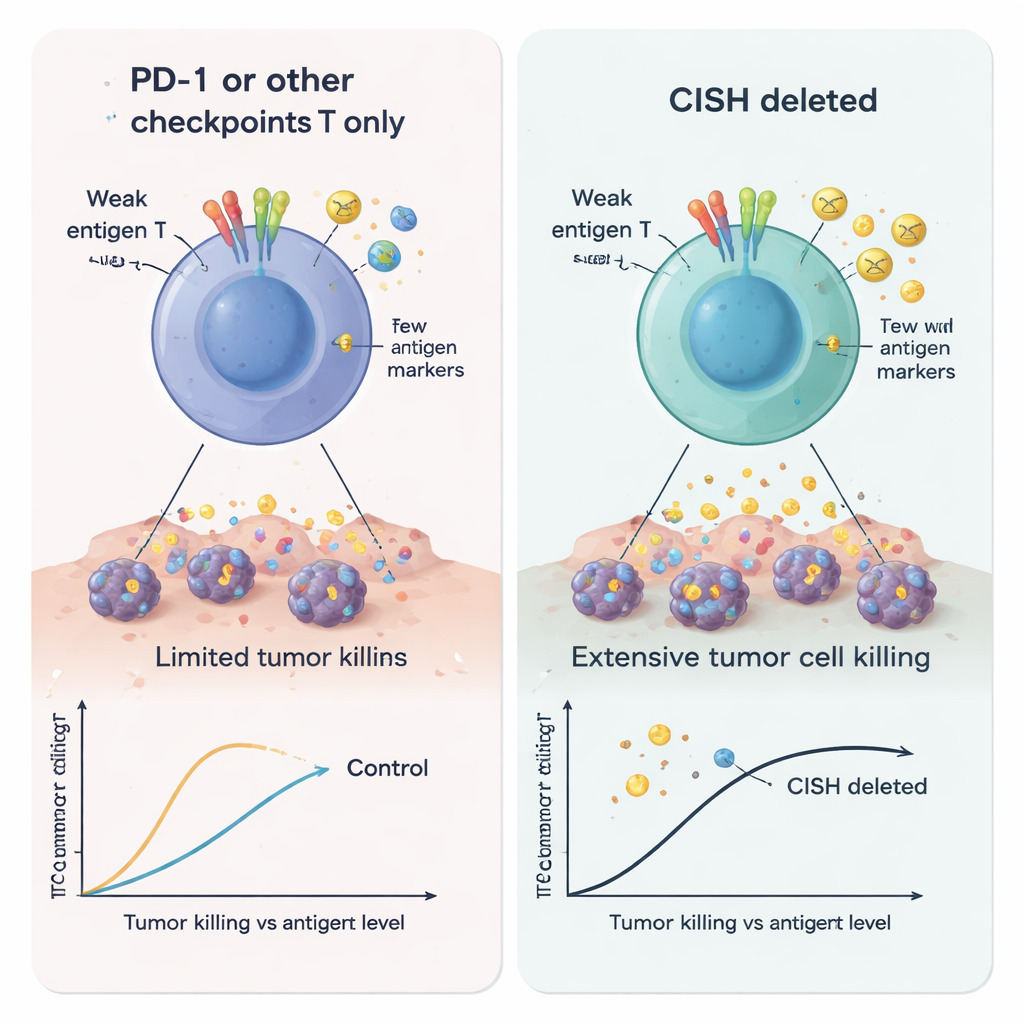
Dalla piastra di laboratorio ai pazienti
Oltre ai provette e alle colture cellulari, l’idea di mirare a CISH ha già raggiunto i pazienti. Un primo trial umano che ha utilizzato linfociti infiltranti il tumore modificati per rimuovere CISH in una persona con cancro colorettale avanzato ha prodotto una risposta completa che è durata per più di due anni, nonostante la resistenza del cancro a molte terapie precedenti. Dimostrando che CISH è un checkpoint intracellulare potente e farmacologicamente aggredibile che aumenta la sensibilità delle cellule T anche a segnali tumorali deboli, questo studio aiuta a spiegare quell’eccezionale risultato clinico e sostiene gli sforzi per sviluppare terapie future—sia cellule editate geneticamente sia farmaci orali—that allentino in modo sicuro questo freno interno e amplino la portata dell’immunoterapia oncologica.
Citazione: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Parole chiave: immunoterapia del cancro, cellule T, terapia CAR-T, checkpoint immunitari, editing genico CRISPR