Clear Sky Science · it
Sviluppo di ligandi per Prohibitin derivati dalla capsaicina per modulare l’interazione Aurora kinase A/PHB2 e la mitofagia nelle cellule tumorali
Perché una molecola del peperoncino conta per il cancro
I peperoncini devono il loro bruciore alla capsaicina, una piccola molecola che si lega alle proteine nelle nostre cellule. Questo studio esplora un risvolto sorprendente di quella spezia familiare: i ricercatori hanno riprogettato la capsaicina per creare nuove molecole simili a farmaci che si dirigono verso le “centrali energetiche” delle cellule tumorali — i mitocondri — e modulano un processo che quelle cellule usano per mantenere in efficienza le loro fabbriche di energia. Poiché le cellule tumorali dipendono fortemente da mitocondri efficienti per alimentare la crescita incontrollata, riuscire a interrompere selettivamente questo sistema di supporto potrebbe aprire una nuova strada per terapie antitumorali.
Le centrali cellulari e la loro squadra di pulizia interna
I mitocondri bilanciano costantemente la produzione di nuove unità con il riciclo di quelle danneggiate. Il lato del riciclo, chiamato mitofagia, funziona come un sistema di controllo qualità: i mitocondri usurati vengono etichettati e degradati, mentre quelli più sani restano. Molte cellule tumorali dirottano questo equilibrio, usando la mitofagia per eliminare i mitocondri deboli e arricchire quelli “super-performanti” che producono grandi quantità di ATP, la moneta energetica della cellula. Una proteina chiamata Aurora kinase A (AURKA), spesso sovraespressa nei tumori, è stata recentemente trovata all’interno dei mitocondri dove si associa con un’altra proteina, Prohibitin‑2 (PHB2), e con l’adattatore dell’autofagia LC3. Insieme formano un complesso che promuove la mitofagia e sostiene un’elevata produzione energetica nelle cellule tumorali.
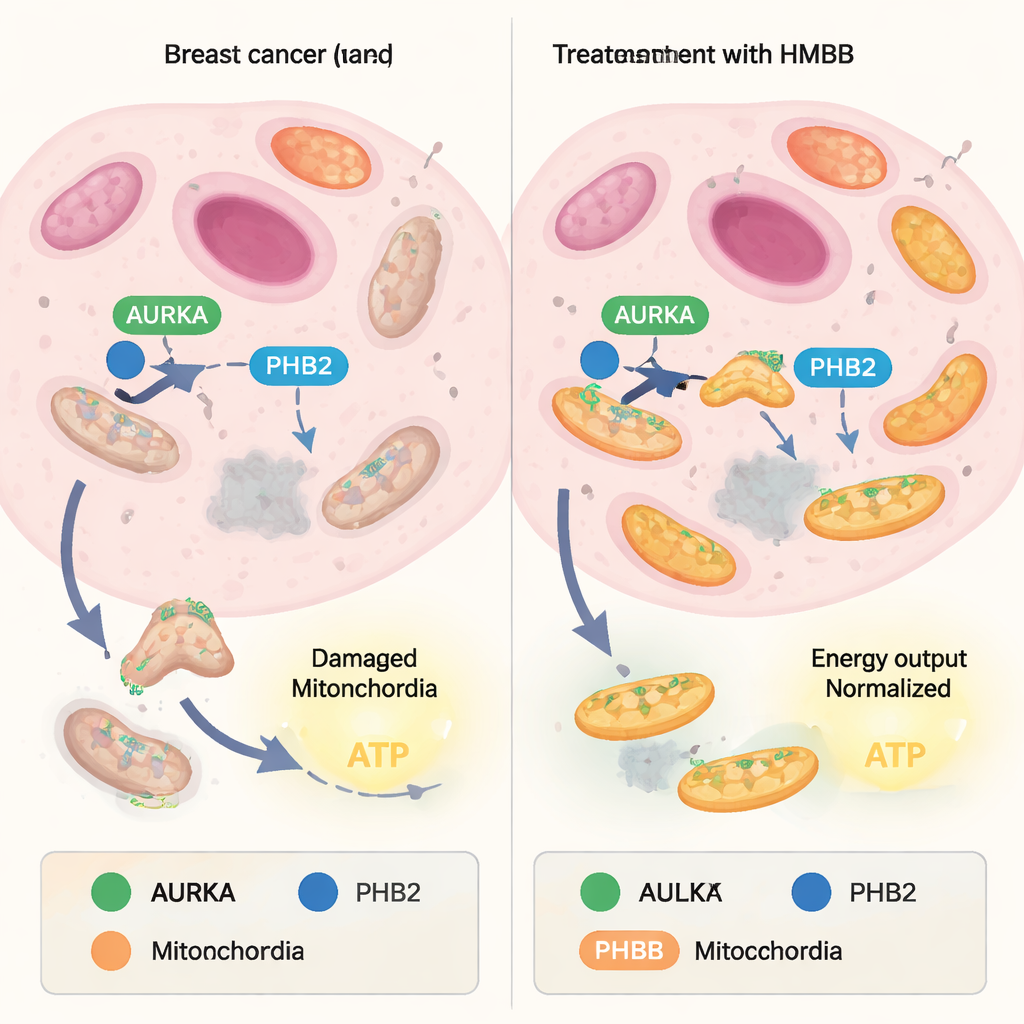
Dalla capsaicina piccante a strumenti molecolari su misura
Lavori precedenti avevano mostrato che un composto naturale chiamato xantumolo può legarsi a PHB2 e disturbare il complesso AURKA–PHB2–LC3, bloccando la mitofagia e riducendo la produzione di ATP mitocondriale. Tuttavia, la struttura chimica dello xantumolo non è ideale per lo sviluppo di farmaci. In questo studio, gli autori si sono rivolti alla capsaicina, un altro ligando naturale di PHB, e hanno chiesto se potesse essere rimodellata in strumenti più pratici. Hanno prima confermato che la capsaicina indebolisce leggermente l’interazione tra AURKA e PHB2 in cellule di cancro al seno vive, usando una tecnica di imaging (FRET/FLIM) che misura quanto due proteine marcate siano vicine tra loro. Hanno poi sintetizzato 16 molecole ispirate alla capsaicina modificando la “coda” e la “testa” aromatica della struttura originale e testato sistematicamente come ogni versione influenzasse la partnership AURKA–PHB2 all’interno dei mitocondri.
La scoperta di una “colla” molecolare che blocca le proteine insieme
Le molecole modificate hanno mostrato effetti sorprendentemente diversi. Alcune, come la stessa capsaicina o un derivato chiamato composto 5, hanno favorito la separazione di AURKA e PHB2. Altre hanno fatto quasi nulla. Un sottoinsieme, tuttavia — in particolare una molecola denominata composto 13, poi chiamata HMBB — ha avuto l’effetto opposto e ha significativamente rafforzato il legame tra AURKA e PHB2. Simulazioni di docking basate al calcolatore hanno aiutato a spiegare questo comportamento. La capsaicina e il composto 5 tendevano a inserirsi nel sito attivo di AURKA in modi che provocavano clash fisici con PHB2, spingendo le due proteine ad allontanarsi. Al contrario, i composti 12 e 13 si accomodavano nel sito attivo di AURKA e contemporaneamente entravano in contatto con una tasca inibitoria nota su PHB2 senza causare collisioni. Le loro forme consentivano loro di agire come una “colla molecolare”, facendo da ponte tra AURKA e PHB2 e stabilizzando il complesso.
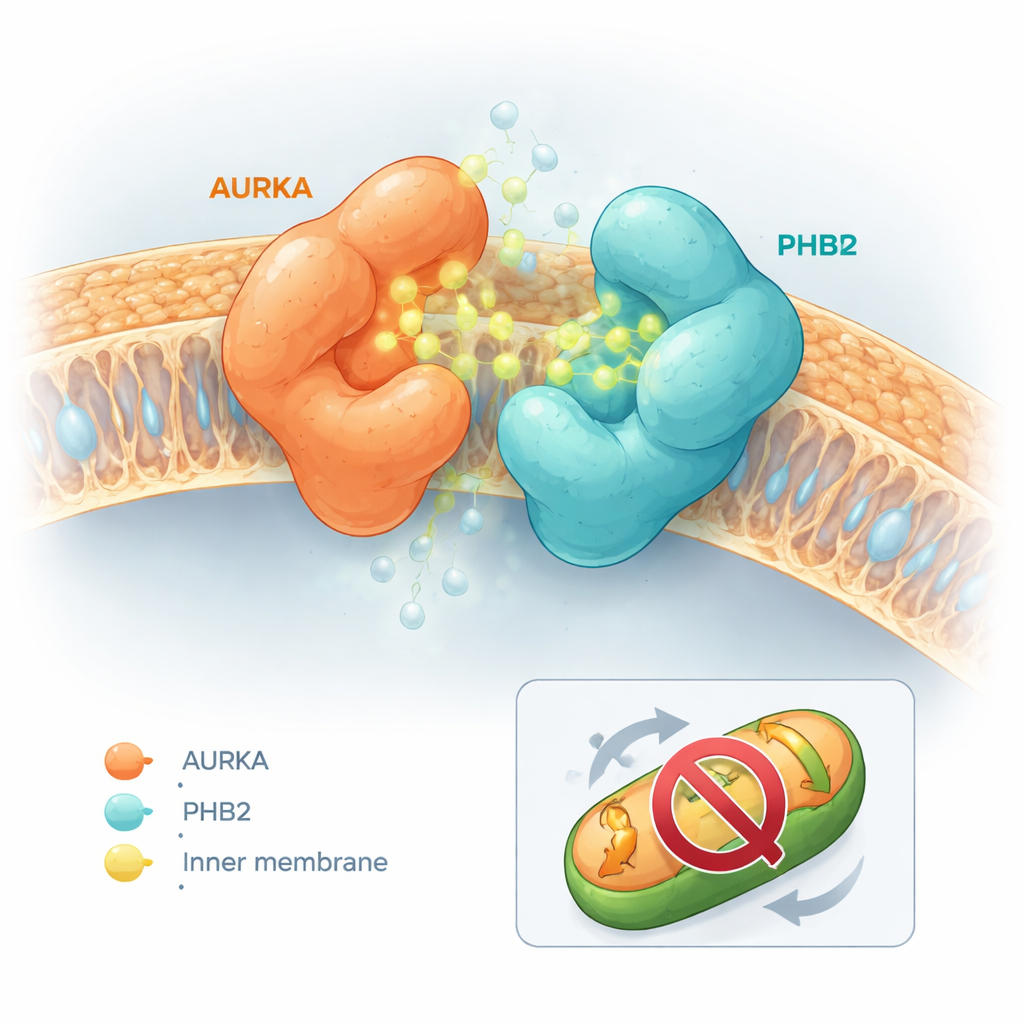
Bloccare la pulizia mitocondriale senza spegnere il centro di controllo della cellula
Una questione cruciale era se questo comportamento da colla molecolare disattivasse semplicemente AURKA ovunque nella cellula, rischiando effetti collaterali diffusi, o se agisse in modo più selettivo. Usando un biosensore fluorescente separato che segnala l’attivazione di AURKA ai centrioli — le strutture che organizzano il macchinario della divisione cellulare — il team ha osservato che HMBB non attenuava l’attività di AURKA in questi siti. Tuttavia, negli esperimenti mitocondriali, HMBB ha invertito la perdita di massa mitocondriale normalmente causata dalla sovraespressione di AURKA nelle cellule di cancro al seno. In cellule che naturalmente esprimono alti livelli di AURKA, HMBB ha aumentato il contenuto mitocondriale, indicando che la mitofagia guidata da AURKA era bloccata. In cellule con bassi livelli di AURKA, HMBB ha avuto scarso impatto, sottolineando la sua dipendenza dalla via AURKA–PHB2.
Cosa potrebbe significare per futuri trattamenti oncologici
Nel complesso, i risultati mostrano che derivati della capsaicina progettati con cura possono modulare finemente l’interazione tra AURKA e PHB2 nei mitocondri. Agendo come colla molecolare, HMBB e composti affini bloccano AURKA e PHB2 in una configurazione che impedisce il normale programma di mitofagia, senza spegnere i ruoli essenziali di AURKA altrove nella cellula. Per il lettore non specialista, l’idea chiave è che gli autori hanno creato molecole prototipo che interferiscono selettivamente con il modo in cui le cellule tumorali mantengono in efficienza le loro centrali energetiche, potenzialmente indebolendo la loro riserva energetica pur risparmiando le funzioni delle cellule normali. Sebbene questi composti siano ancora in una fase iniziale, in laboratorio, essi illustrano una strategia promettente: usare piccole molecole simili a farmaci per colpire partnership proteiche specifiche all’interno dei mitocondri e, così facendo, compromettere i vantaggi metabolici di cui molte neoplasie dipendono.
Citazione: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Parole chiave: mitocondri, mitofagia, Aurora kinase A, derivati della capsaicina, metabolismo del cancro