Clear Sky Science · it
Rivalutare la specificità tra proteine Gα e elementi di risposta nel segnalamento GPCR
Perché piccoli interruttori cellulari contano per la medicina
Molti dei farmaci odierni agiscono attivando o disattivando dei «comandi» molecolari sulla superficie delle nostre cellule chiamati recettori accoppiati a proteine G, o GPCR. Questi interruttori trasmettono messaggi all’interno della cellula tramite proteine ausiliarie note come proteine G e alla fine attivano o sopprimono geni. Per decenni i ricercatori si sono affidati a semplici test che producono luce per vedere quali proteine G usa un dato farmaco o recettore. Questo studio pone una domanda fondamentale ma cruciale: quei test ci stanno davvero dicendo quello che pensiamo—e possiamo ancora fidarci di essi nella progettazione della prossima generazione di farmaci di precisione?
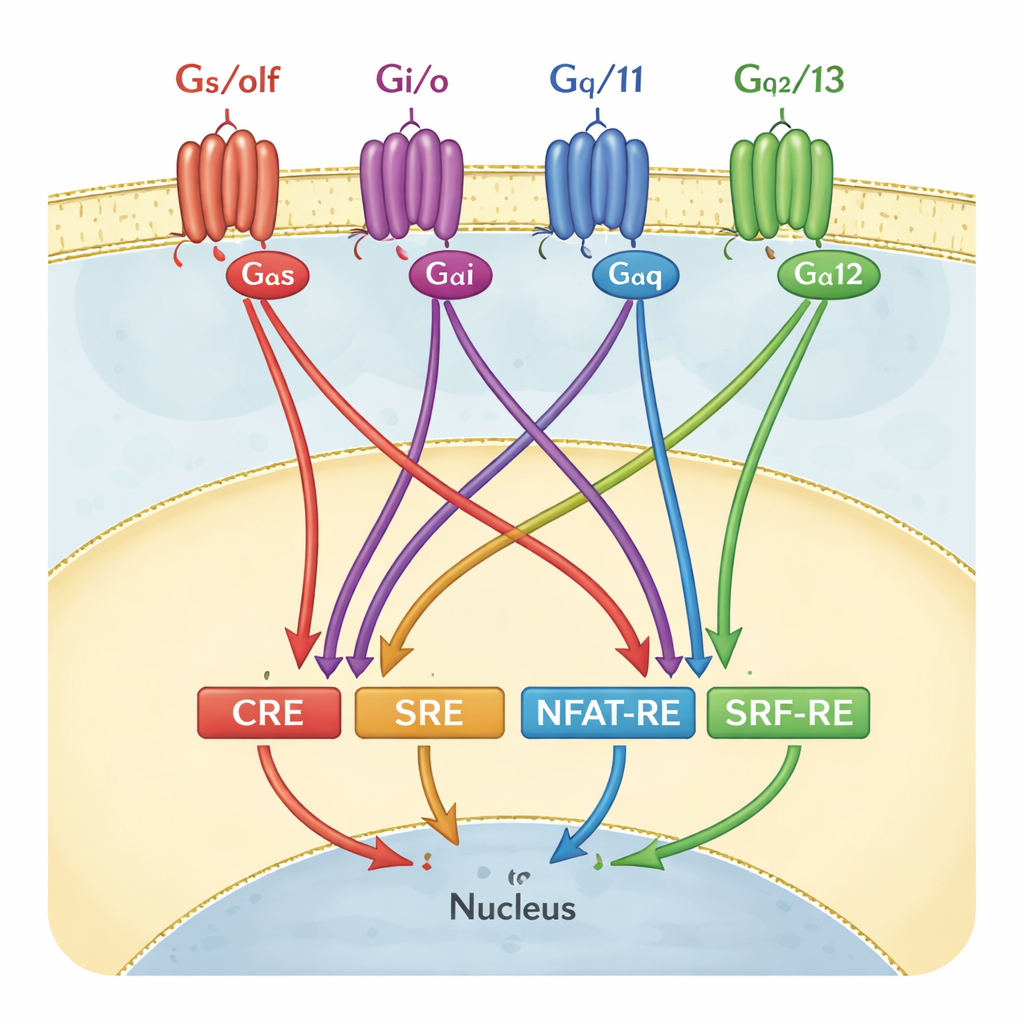
Come gli scienziati leggono solitamente i segnali GPCR
Per monitorare l’attività dei GPCR molti laboratori usano saggi di reporter genici. In questi test, le cellule sono ingegnerizzate in modo che quando un particolare interruttore genico, o «elemento di risposta», viene attivato, le cellule si illuminano. Quattro di questi interruttori sono particolarmente popolari: CRE, SRE, NFAT‑RE e SRF‑RE. Ognuno è stato a lungo trattato come un sostituto per un ramo della segnalazione mediata dalle proteine G—per esempio, CRE per la famiglia Gαs/olf, o SRF‑RE per Gα12/13. Nei libri di testo e nelle pipeline di screening queste associazioni vengono spesso disegnate quasi come diagrammi di cablaggio uno‑a‑uno: attivi una specifica proteina G e si accende solo un reporter.
Mettere alla prova il vecchio diagramma di cablaggio
Gli autori hanno sfidato sistematicamente questa rappresentazione usando cellule HEK293 umane in cui specifiche famiglie di proteine G—o persino tutte le proteine G—sono state rimosse tramite editing genomico. Hanno poi reintrodotto singoli tipi di proteine G uno per uno. In queste cellule hanno espresso nove diversi GPCR, scelti per rappresentare recettori che segnalano in modo molto selettivo oppure attraverso molti partner proteici G. Misurando quanto intensamente ciascuno dei quattro reporter si illuminava attraverso molte concentrazioni di farmaco, hanno potuto vedere quali proteine G erano realmente necessarie per ciascun elemento di risposta e quali potevano contribuire indirettamente.
Percorsi sovrapposti invece di canali puliti
I risultati ribaltano il modello semplice del «un recettore‑un reporter». Mentre CRE dipendeva ancora principalmente dalle proteine Gαs/olf—il classico percorso che aumenta il cAMP—altre famiglie di proteine G potevano influenzare in modo netto l’attività di CRE, ma solo quando Gαs/olf era presente. Per gli altri tre reporter, SRE, NFAT‑RE e SRF‑RE, la famiglia Gαq/11 è emersa come il principale motore, anche se tradizionalmente SRE e SRF‑RE erano collegati ad altri rami delle proteine G. SRE e SRF‑RE si sono comportati in modo particolarmente simile, suggerendo che attingono a macchinari a valle condivisi piuttosto che a percorsi distinti e isolati. In molti casi proteine G aggiuntive come Gα12/13 e Gαi/o fornivano una spinta extra o un’attività di fondo, evidenziando una rete di crosstalk piuttosto che canali separati.
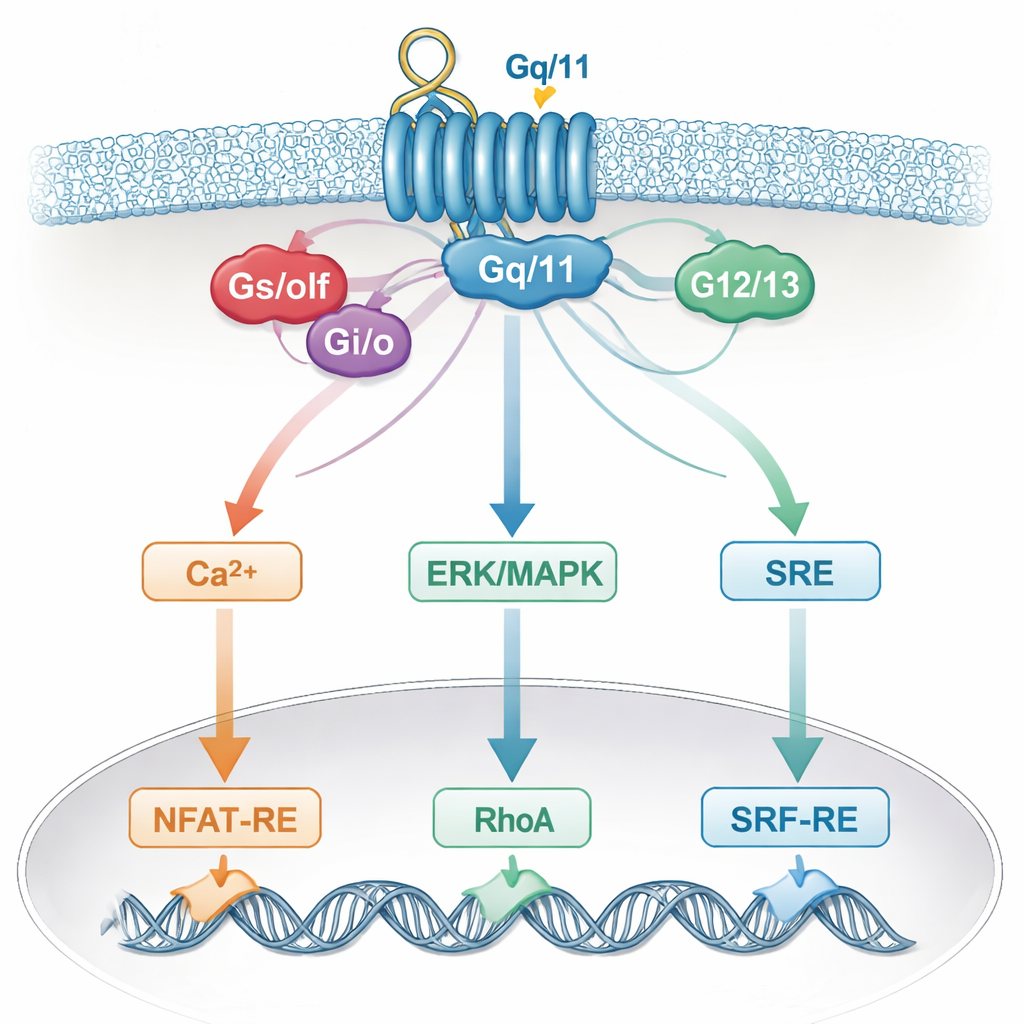
Perché la rete cellulare sfuma i nostri rilevamenti
Questa specificità sfocata probabilmente riflette come le cellule reali integrano i segnali. Un singolo recettore può attivare più proteine G, che poi convergono su messaggeri comuni come calcio, ERK/MAPK, RhoA o cAMP, e su aiutanti condivisi come le subunità Gβγ. Questi percorsi condivisi, a loro volta, alimentano gli stessi interruttori genici nel nucleo. Di conseguenza, un reporter che si pensava rispondesse a una sola famiglia di proteine G in realtà «ascolta» più famiglie. Fattori specifici del tipo cellulare e l’insieme esatto di recettori presenti aggiungono ulteriore complessità, il che significa che le conclusioni tratte da un sistema cellulare potrebbero non valere in un altro.
Cosa significa per la scoperta di farmaci
Per i non specialisti, la conclusione principale è che molti test GPCR basati sulla luminescenza comunemente usati sono meno specifici di quanto i loro nomi suggeriscano. Possono comunque dirci che un recettore è attivo e indicare grossolanamente quali vie ampie sono coinvolte, ma non costituiscono una prova affidabile che una particolare famiglia di proteine G—e solo quella—sia responsabile. Gli autori sostengono che ricercatori e sviluppatori di farmaci dovrebbero trattare questi reporter come indicatori approssimativi e abbinarli a metodi più diretti che osservano le interazioni tra proteine in tempo reale. Così facendo si otterrà un quadro più veritiero di come i potenziali farmaci indirizzano la segnalazione cellulare e si eviteranno scorciatoie fuorvianti nella ricerca di terapie più sicure e mirate.
Citazione: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Parole chiave: Segnalazione GPCR, Proteine G, saggi reporter, Reti di segnalazione cellulare, Scoperta di farmaci