Clear Sky Science · it
Test basati su cellule e selettivi per isoforma delle chinasi accoppiate a proteine G per una valutazione completa degli inibitori
Perché abbassare i “manopole del volume” cellulari è importante
Molti dei nostri farmaci agiscono modulando l'attività dei recettori di superficie cellulare che rilevano ormoni, neurotrasmettitori e farmaci. Questi recettori devono essere spenti con attenzione affinché le cellule non rimangano iperattivate, processo parzialmente controllato da enzimi chiamati GRK. Quando le GRK sono troppo attive, come avviene nell’insufficienza cardiaca e in alcuni tumori, la segnalazione viene compromessa. Questo studio sviluppa test pratici basati su cellule per misurare quanto efficacemente molecole sperimentali possono bloccare specifiche GRK, aiutando gli scienziati a progettare farmaci più intelligenti che regolano con precisione questi cruciali «manopole del volume» cellulari.
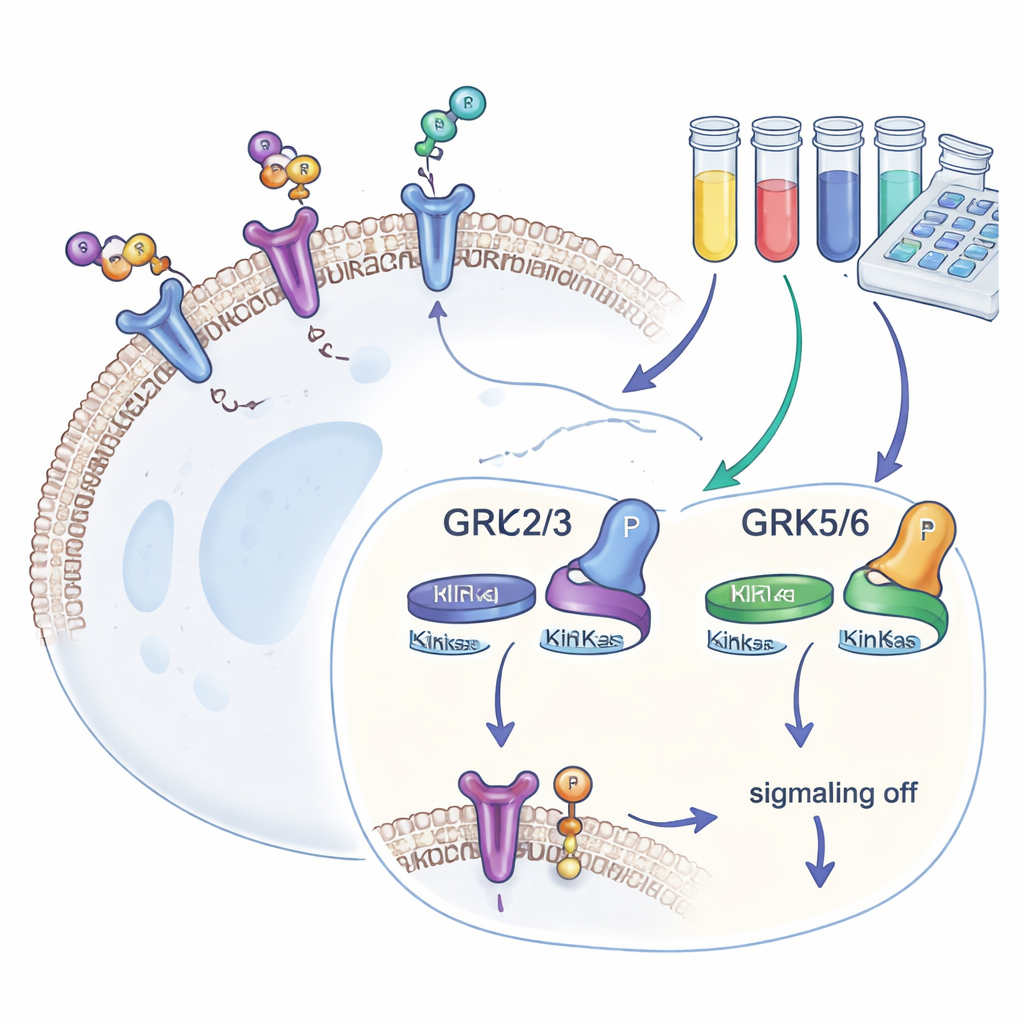
Guardiani sulla superficie cellulare
Le nostre cellule possiedono centinaia di tipi di recettori accoppiati a proteine G (GPCR), che rilevano segnali esterni e li traducono in risposte intracellulari. Dopo l’attivazione di un GPCR, le GRK aggiungono piccole “etichette” di fosfato alla sua coda. Queste etichette attirano un’altra proteina, la beta-arrestina, che interrompe l’ulteriore segnalazione e spesso internalizza il recettore. Quattro isoforme GRK—GRK2, GRK3, GRK5 e GRK6—sono presenti in molti tessuti. Poiché influenzano l’intensità della risposta dei GPCR e i loro livelli sono alterati in malattie come insufficienza cardiaca, cancro e dipendenze, gli sviluppatori di farmaci sono interessati a trovare inibitori delle GRK potenti e selettivi.
Costruire un banco di prova pulito all’interno delle cellule
La maggior parte degli studi precedenti sulle GRK si basava su modellizzazione al computer o su esperimenti in provetta, che rivelano quanto strettamente un inibitore si leghi ma non come si comporti nel caotico interno di una cellula vivente. Per colmare questa lacuna, gli autori hanno ingegnerizzato cellule umane HEK293 private di tutte e quattro le GRK comuni e poi hanno reintrodotto una sola isoforma alla volta. Ciascuna linea cellulare portava anche un recettore ben caratterizzato, il recettore beta-2 adrenergico, marcato in modo che la sua fosforilazione in un sito specifico della coda (chiamato T360/S364) potesse essere rilevata mediante un saggio sensibile basato su anticorpi. Poiché questo sito è modificato solo dalle GRK, la quantità di fosfato presente funge da misura diretta e quantitativa dell’attività di ciascuna isoforma GRK nelle cellule viventi.
Distinguere i buoni, i deboli e i non specifici
Utilizzando questo kit di strumenti, il gruppo ha testato una serie di inibitori GRK commercialmente disponibili. Hanno prima raggruppato i composti che prendono di mira principalmente GRK2 e GRK3, e un altro insieme diretto contro GRK5 e GRK6. Confrontando quanto ciascuna molecola riduceva la fosforilazione del recettore in cellule che esprimevano una sola sottoprefosforma GRK, hanno potuto mappare la selettività nel contesto cellulare. Un composto, denominato 8h, è emerso come il più potente inibitore di GRK2/3, mentre il composto 18 si è distinto per l’inibizione selettiva di GRK5/6. Alcune molecole largamente utilizzate hanno mostrato scarso effetto alle dosi testate, probabilmente perché entravano poco nelle cellule, e un inibitore covalente molto potente ha compromesso la salute cellulare, rendendolo inadatto per esperimenti di imaging.
Dalle impronte chimiche al comportamento dei recettori
Per dimostrare che questi inibitori influenzano non solo un recettore di prova ma la biologia dei GPCR in senso più ampio, gli autori hanno esaminato diversi recettori di rilievo medico, inclusi il recettore mu-oppiaceo e il recettore della vasopressina V2. Hanno misurato sia la fosforilazione sia l’internalizzazione dei recettori mediante microscopia. Il composto 8h o il 18 da soli riducevano parzialmente la fosforilazione e il movimento verso l’interno dei recettori per molti bersagli, ma la combinazione di 8h e 18 previene quasi completamente questi cambiamenti e mantiene i recettori sulla superficie cellulare. Esperimenti aggiuntivi che monitoravano il reclutamento della beta-arrestina hanno confermato che gli stessi composti possono modulare la segnalazione anche in altri recettori regolati da insiemi sovrapposti di GRK.
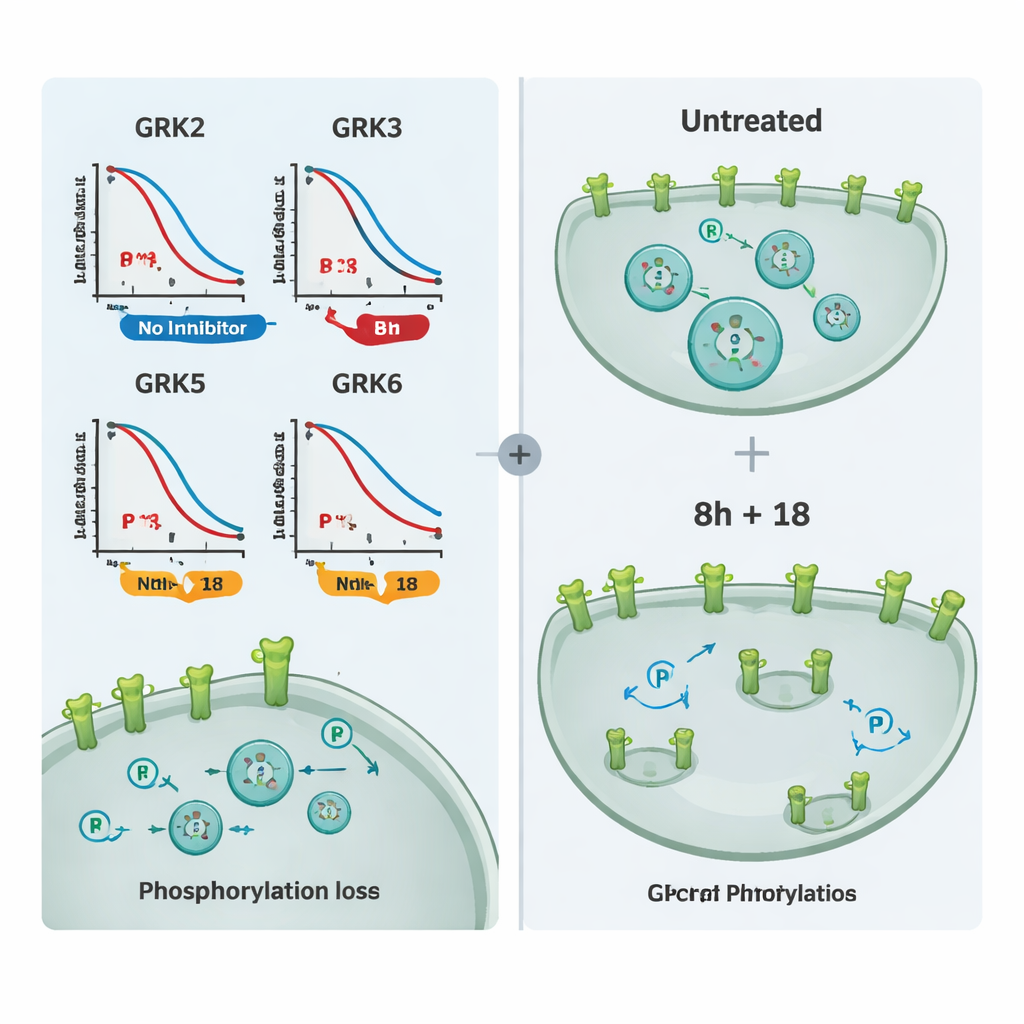
Cosa significa per i farmaci futuri
Per non specialisti, il messaggio chiave è che lo studio fornisce un set affidabile di test basati su cellule—and due composti strumentali particolarmente utili, 8h e 18—that consentono ai ricercatori di vedere, nelle cellule viventi, esattamente come vengono attenuate diverse isoforme di GRK. Piuttosto che dedurre dalle semplificate misurazioni in provetta, gli scienziati possono ora confrontare fianco a fianco gli inibitori candidati e decidere se agiscono principalmente su GRK2/3, GRK5/6 o su tutte e quattro contemporaneamente. Questa chiarezza dovrebbe accelerare lo sviluppo di farmaci che modulano con maggiore precisione la segnalazione GPCR, con potenziali benefici per il trattamento di malattie cardiache, cancro, disturbi del dolore e altre condizioni in cui l’equilibrio della segnalazione è alterato.
Citazione: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Parole chiave: segnalazione GPCR, inibitori GRK, recettore beta-adrenergico, saggio basato su cellule, scoperta di farmaci