Clear Sky Science · it
HBP1 potenzia l’attività del recettore del progesterone e l’espressione di IGFBP1 promuovendo la decidualizzazione endometriale
Perché questo conta per la fertilità
Quando inizia una gravidanza, l’embrione può impiantarsi nell’utero solo se il rivestimento uterino ha subito una trasformazione cruciale chiamata decidualizzazione. Molti casi di infertilità e insuccessi ripetuti nel trasferimento di embrioni restano senza spiegazione, e prove crescenti suggeriscono che il problema risiede in questa trasformazione piuttosto che nell’embrione stesso. Questo studio individua un «interruttore» molecolare finora sottovalutato, un fattore di trascrizione chiamato HBP1, che contribuisce a preparare il rivestimento uterino per l’impianto e potrebbe offrire nuove vie per diagnosticare e trattare i problemi di impianto.
Un interruttore nascosto nel rivestimento uterino
Il rivestimento interno dell’utero, l’endometrio, cambia ritmicamente a ogni ciclo mestruale. Sotto l’influsso degli estrogeni cresce, e sotto il progesterone matura in un letto ricettivo per l’embrione. In questo lavoro i ricercatori si sono concentrati sulle cellule stromali endometriali umane, le cellule strutturali che si trasformano in cellule deciduali più grandi e più secernenti al momento dell’impianto. Analizzando dati di espressione genica esistenti e svolgendo nuovi esperimenti, hanno osservato che i livelli di HBP1 aumentano bruscamente quando queste cellule stromali iniziano la decidualizzazione, suggerendo che HBP1 fa parte del sistema temporale intrinseco che prepara l’utero.
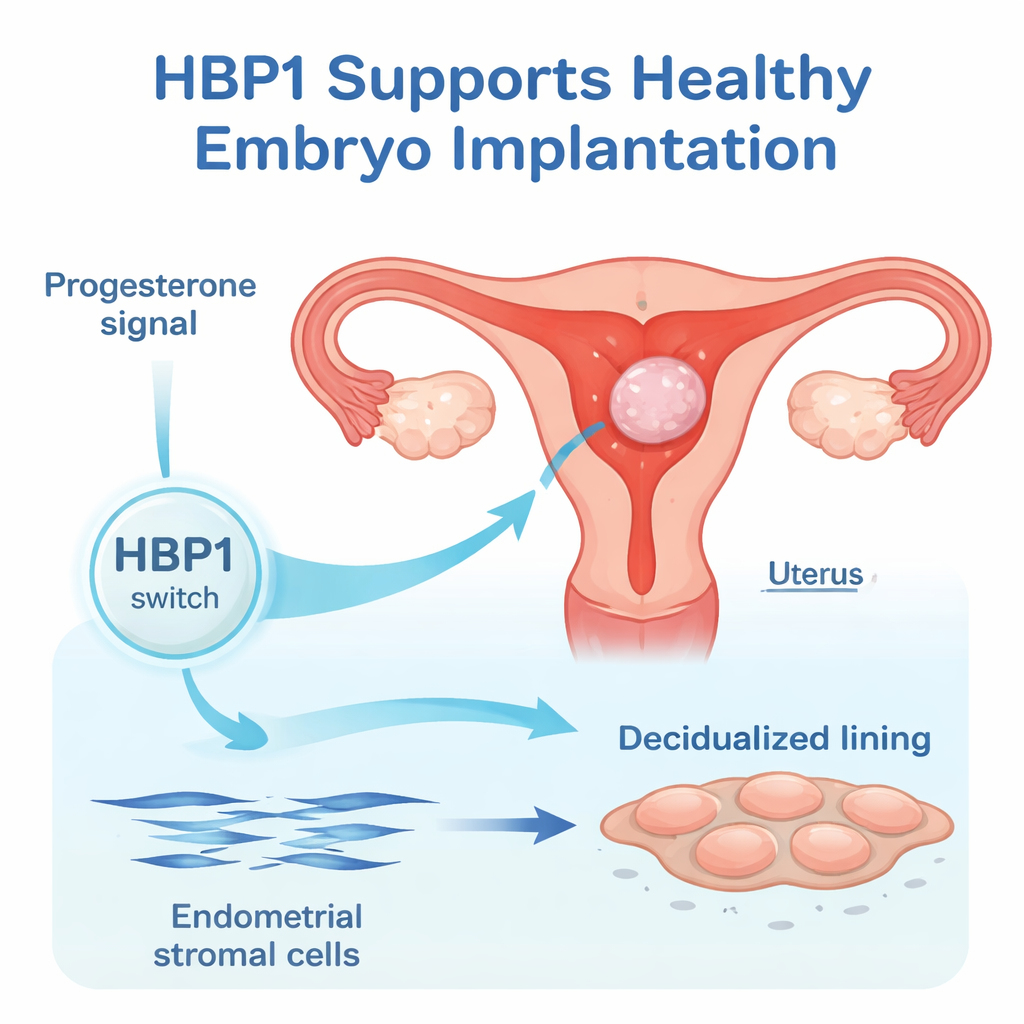
Aiutare le cellule a cambiare forma e rallentare
Per verificare se HBP1 è solo presente o effettivamente necessario, il gruppo ha modulato i suoi livelli in cellule stromali endometriali umane in coltura. Quando HBP1 è stato ridotto, marcatori classici della decidualizzazione come IGFBP1, FOXO1 e prolattina sono diminuiti sia a livello di RNA sia di proteina. Le cellule non hanno inoltre effettuato il tipico cambiamento morfologico da cellule sottili e fusiformi a cellule più larghe e poligonali e hanno continuato a proliferare. Quando HBP1 è stato aumentato, i livelli di IGFBP1 sono saliti e la divisione cellulare si è rallentata. Complessivamente questi risultati mostrano che HBP1 aiuta le cellule a uscire dalla modalità di crescita ed entrare nello stato deciduale specializzato che supporta le prime fasi della gravidanza.
Affinare i segnali ormonali all’interno della cellula
Il progesterone e il suo recettore sono centrali per la preparazione dell’utero, ma non tutti i tessuti rispondono ugualmente all’ormone. I ricercatori hanno scoperto che la segnalazione del progesterone stessa aumenta i livelli di HBP1, creando un circuito di feedback positivo. Sorprendentemente, l’abbassamento di HBP1 non ha cambiato la quantità di recettore del progesterone prodotta dalle cellule, ma ha attenuato l’attività di geni importanti rispondenti al progesterone, inclusi FKBP4, FKBP5, FOSL2 e il coattivatore SRC1. Con approcci a livello genomico hanno mostrato che HBP1 si lega vicino a molti di questi geni ed è associato a un aumento di una specifica marcatura istonica, H3K4me3, che segnala DNA attivo. In sostanza, HBP1 non accende o spegne il recettore; rende più leggibili i geni bersaglio del recettore.
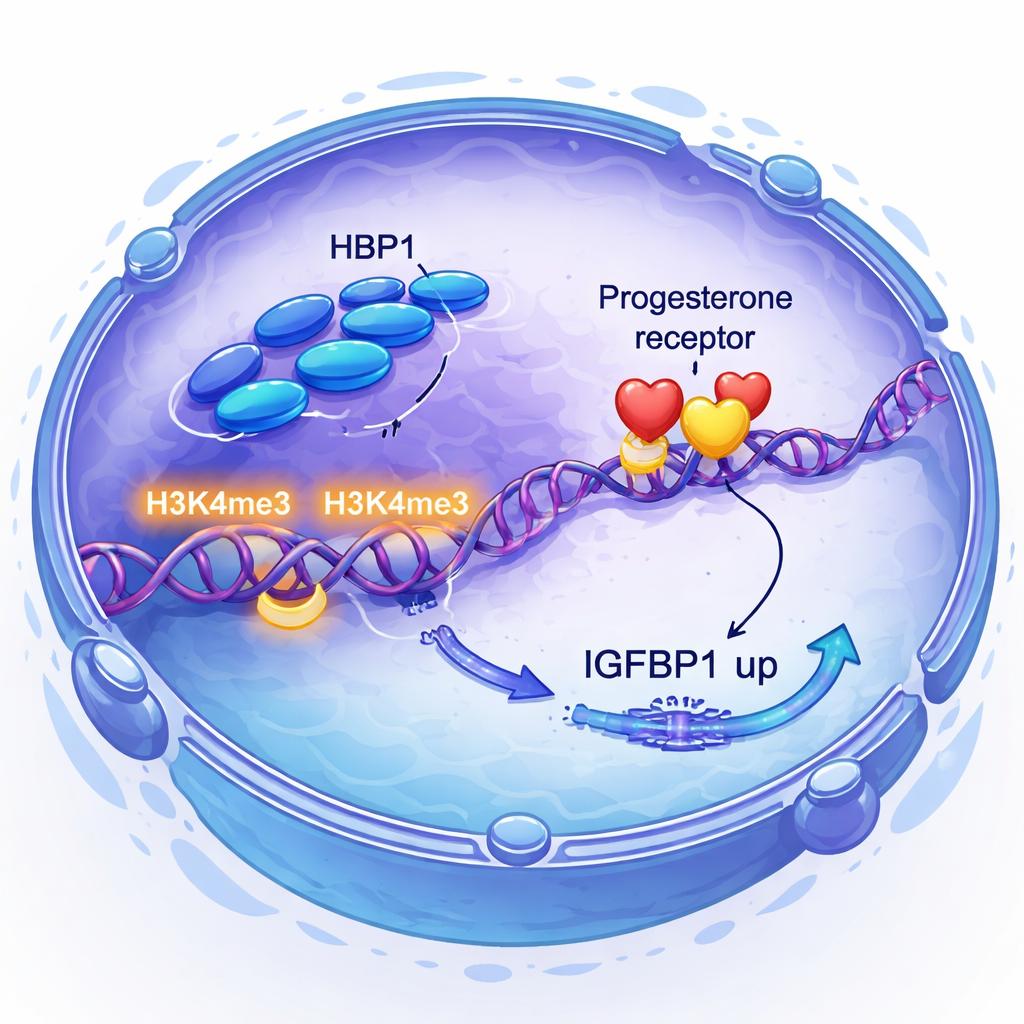
Controllo diretto di un segnale chiave per l’impianto
Il gruppo ha poi indagato come HBP1 si collega a IGFBP1, una proteina da tempo utilizzata come marcatore di una buona decidualizzazione e nota per influenzare la comunicazione embrione–utero. Combinando RNA-seq con ChIP-seq, hanno mostrato che HBP1 si trova direttamente sulla regione promotrice di IGFBP1 e aumenta lì l’H3K4me3, promuovendo una maggiore produzione di IGFBP1. Hanno anche riscontrato che la riduzione di HBP1 attivava la via PI3K–AKT, un segnale legato alla crescita che, quando iperattivo, sopprime IGFBP1. Il blocco di questa via ha ripristinato i livelli di IGFBP1. Dunque HBP1 sostiene la decidualizzazione in due modi: attivando direttamente IGFBP1 e smorzando un segnale di crescita che altrimenti inibirebbe i geni deciduali.
Collegare un difetto molecolare all’impianto fallito
Infine, i ricercatori hanno analizzato campioni endometriali di donne con fallimento ricorrente dell’impianto e li hanno confrontati con tessuti di controlli fertili nella fase mid-secretoria, pronta all’impianto. Le donne con fallimenti ripetuti mostravano livelli nettamente più bassi di HBP1 e dei suoi partner a valle IGFBP1, FKBP5 e FOSL2, nonostante i livelli del recettore del progesterone fossero simili tra i gruppi. Questo quadro è coerente con l’idea di «resistenza al progesterone»: l’ormone è presente, ma il tessuto non riesce a montare una risposta completa perché mancano fattori di supporto chiave come HBP1.
Cosa significa per le pazienti
In termini accessibili, questo studio suggerisce che HBP1 agisce come un’impostazione principale sul pannello di controllo del rivestimento uterino. Quando è adeguatamente attivato, aiuta a far funzionare i segnali del progesterone, incoraggia le cellule a interrompere la proliferazione e a specializzarsi, e aumenta la produzione di molecole favorevoli all’impianto come IGFBP1. Quando HBP1 è troppo basso, il rivestimento può apparire normale al microscopio ma funzionare male, portando a embrioni che semplicemente non riescono a impiantarsi. Comprendere e misurare HBP1 e la sua rete potrebbe, in futuro, aiutare i medici a identificare le donne a rischio di problemi di impianto e ispirare nuovi trattamenti che ripristinino la ricettività dell’utero.
Citazione: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Parole chiave: decidualizzazione endometriale, impianto dell’embrione, segnalazione del progesterone, infertilità, HBP1