Clear Sky Science · it
L'indolo-3-acido acetico, un metabolita intestinale, aggrava il lupus neuropsichiatrico tramite la via AHR/STAT3 nelle microglia
Come i microbi intestinali possono influenzare la mente
Le persone con lupus, una malattia autoimmune, sviluppano talvolta problemi gravi di pensiero, umore e memoria—una condizione chiamata lupus neuropsichiatrico. Questi sintomi cerebrali possono essere invalidanti, eppure i medici fanno ancora fatica a spiegare esattamente perché compaiono o come trattarli. Questo studio esplora un colpevole inaspettato: alcuni batteri intestinali e i composti che producono, che possono spostarsi dall'intestino al cervello e alimentare lì l'infiammazione.
Dai microbi intestinali ai comportamenti alterati
I ricercatori hanno iniziato chiedendosi se i microbi intestinali dei pazienti con lupus neuropsichiatrico avessero effetti diversi rispetto a quelli di pazienti con lupus privi di sintomi cerebrali. Hanno trasferito i batteri fecali di ciascun gruppo di pazienti in topi sani che erano stati prima privati dei loro microbi intestinali. I topi che hanno ricevuto microbi da pazienti con lupus neuropsichiatrico hanno sviluppato comportamenti più simili all'ansia, segni di depressione e deficit di apprendimento e memoria rispetto ai topi che avevano ricevuto microbi da altri pazienti con lupus. I loro cervelli mostravano una maggiore attivazione delle microglia—le cellule immunitarie del cervello—e livelli più alti di molecole infiammatorie. Anche la guaina protettiva intorno al cervello, nota come barriera emato‑encefalica, era più permeabile in questi animali, suggerendo che qualcosa nel microbiota trapiantato stesse danneggiando questa barriera critica.
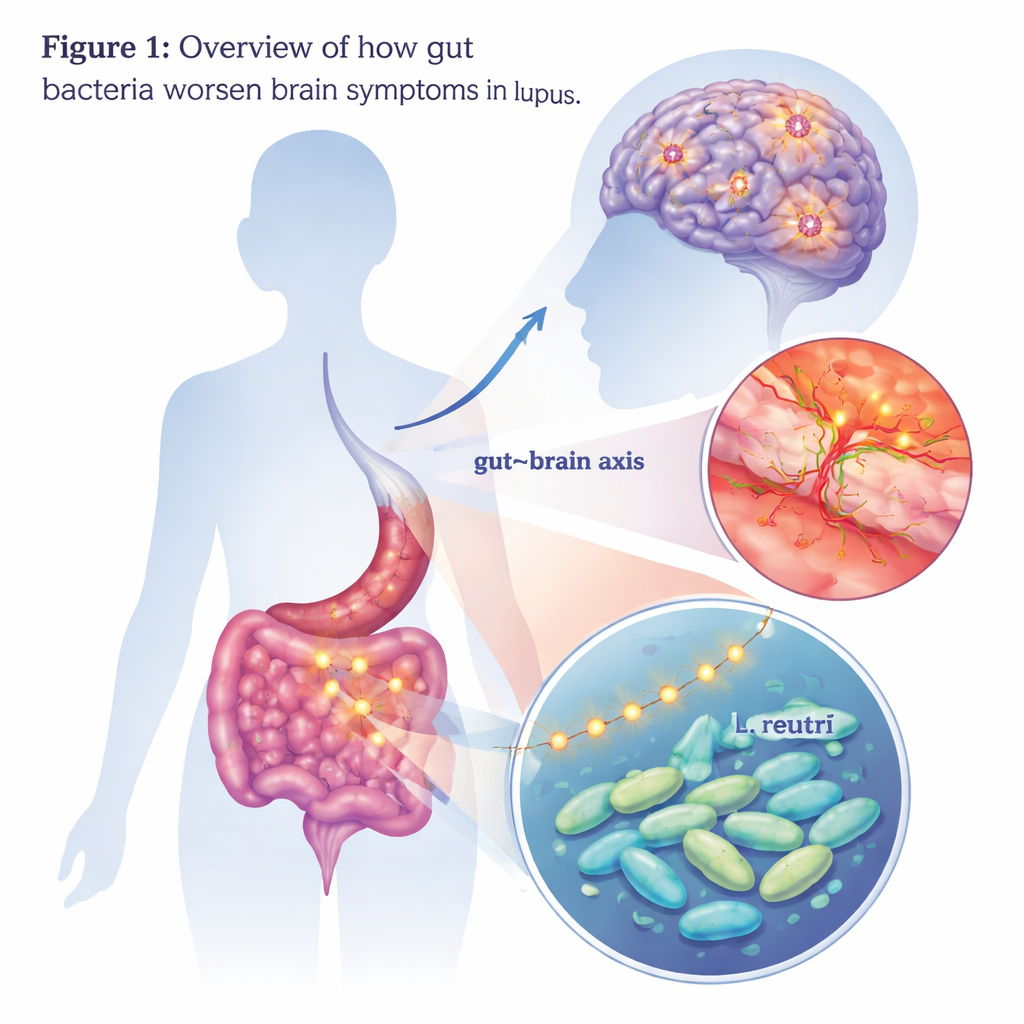
Focalizzarsi su un singolo batterio
Per identificare quali microbi potessero essere responsabili, il gruppo ha confrontato le comunità batteriche intestinali di pazienti e topi. Un genere è emerso in particolare: Lactobacillus, e in particolare una specie chiamata Lactobacillus reuteri, era più abbondante nei pazienti con lupus neuropsichiatrico e nei topi che mostravano alterazioni cerebrali. Quando gli scienziati hanno somministrato L. reuteri da solo a topi inclini al lupus, gli animali hanno sviluppato comportamenti ansiosi e depressivi più marcati e hanno ottenuto risultati peggiori nei test di memoria. I loro cervelli mostravano microglia più attivate, una maggiore perdita di neuroni e un'ulteriore compromissione della barriera emato‑encefalica. Questi risultati suggeriscono che, almeno nel contesto del lupus, questo batterio normalmente percepito come probiotico può assumere un ruolo più dannoso.
Una piccola molecola con grandi effetti
L. reuteri è noto per produrre una sostanza chimica chiamata indolo‑3‑acido acetico (IAA) dal triptofano alimentare. Tramite test chimici sensibili, il team ha trovato livelli più elevati di IAA nelle feci dei pazienti con lupus neuropsichiatrico rispetto ad altri pazienti con lupus, e ha confermato che colture di L. reuteri producono molto più IAA rispetto a batteri intestinali comuni come Escherichia coli. Nei pazienti con lupus neuropsichiatrico, i livelli di IAA nel liquido che circonda cervello e midollo spinale erano correlati a livelli più alti di citochine infiammatorie, suggerendo che questa molecola possa raggiungere il sistema nervoso centrale e promuovere l'infiammazione. In topi inclini al lupus, l'alimentazione con L. reuteri ha aumentato i livelli di IAA nell'intestino, nel sangue e nel cervello. La somministrazione di IAA da sola a questi topi ha riprodotto molte delle stesse alterazioni: comportamenti anomali, attivazione delle microglia, aumento dei segnali infiammatori e indebolimento delle barriere emato‑encefalica e intestinale.
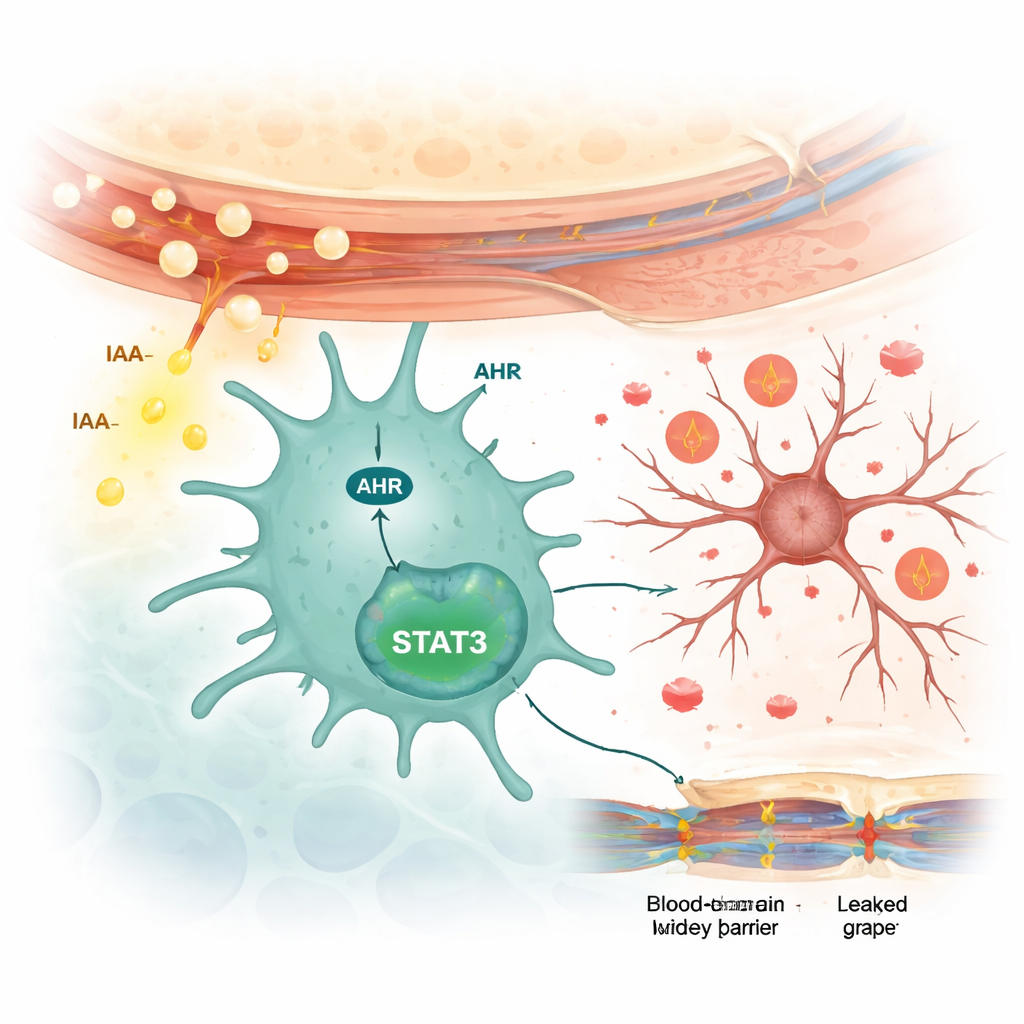
Come le cellule immunitarie del cervello vengono attivate
Gli scienziati hanno quindi esaminato come l'IAA comunichi con le cellule cerebrali. Hanno scoperto che l'IAA aumentava l'attività di una proteina sensore chiamata recettore degli idrocarburi arilici (AHR) specificamente nelle microglia, non nei neuroni o nelle cellule di supporto stellate chiamate astrociti. In microglia coltivate, l'IAA ha aumentato i livelli di AHR e ha attivato una proteina di segnalazione a valle denominata STAT3, che a sua volta ha guidato la produzione di citochine infiammatorie. Il blocco dell'AHR con un farmaco ha impedito l'attivazione di STAT3 e ha ridotto il rilascio di questi segnali infiammatori. Quando i topi inclini al lupus sono stati trattati con il farmaco che blocca l'AHR, i loro comportamenti ansiosi e depressivi sono migliorati, l'attivazione delle microglia è diminuita, le molecole infiammatorie sono calate e la barriera emato‑encefalica è diventata meno permeabile.
Cosa significa per i pazienti
Nel complesso, lo studio delinea una catena di eventi che collega l'intestino al cervello nel lupus neuropsichiatrico. Un'eccessiva abbondanza di L. reuteri nell'intestino produce IAA in eccesso, che indebolisce la barriera intestinale ed entra nel circolo sanguigno. L'IAA raggiunge poi il cervello, dove attiva il segnale AHR/STAT3 nelle microglia, scatenando un'infiammazione che danneggia i neuroni e rende più permeabile la barriera emato‑encefalica. Per i pazienti, questi risultati suggeriscono che modificare i batteri intestinali, ridurre metaboliti dannosi come l'IAA o bloccare la via AHR/STAT3 nelle microglia potrebbe un giorno aiutare a proteggere il cervello dagli effetti devastanti del lupus neuropsichiatrico.
Citazione: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Parole chiave: lupus neuropsichiatrico, microbiota intestinale, Lactobacillus reuteri, infiammazione delle microglia, barriera emato‑encefalica