Clear Sky Science · it
La terapia dinamica stimolata da radionuclidi induce percorsi complementari di necroptosi e apoptosi immunogenica nella morte cellulare tumorale
Trasformare i trucchi del cancro contro se stesso
Il cancro è noto per eludere i nostri migliori trattamenti, soprattutto nei tumori mammari aggressivi che si diffondono in tutto il corpo. Questo studio esplora un approccio ingegnoso chiamato terapia dinamica stimolata da radionuclidi (RaST), che utilizza traccianti per imaging medico e nanoparticelle attivate dalla luce per uccidere le cellule tumorali in modi che risvegliano anche il sistema immunitario. Per i lettori, questo lavoro è importante perché suggerisce come strumenti di imaging già esistenti e materiali intelligenti possano essere riproposti per creare un controllo del cancro più duraturo e guidato dal sistema immunitario, anziché un semplice e temporaneo restringimento del tumore.
Un nuovo modo per illuminare i tumori dall’interno
I trattamenti tradizionali basati sulla luce funzionano solo dove un fascio esterno può arrivare, come sulla pelle o sui tumori superficiali. RaST supera questo limite utilizzando uno zucchero radioattivo, simile al tracciante già impiegato nelle PET, che si accumula naturalmente nelle cellule tumorali a rapida crescita. Mentre questo tracciante percorre il tumore, emette un debole bagliore blu noto come radiazione di Cherenkov. I ricercatori hanno progettato piccolissime nanoparticelle di biossido di titanio rivestite con una proteina che mira il cancro, in modo che anch’esse si concentrino sul tumore. Quando il tracciante e le nanoparticelle si incontrano, la luce interna accende le particelle che a loro volta generano raffiche di specie reattive dell’ossigeno—molecole altamente reattive che danneggiano le cellule tumorali dall’interno.
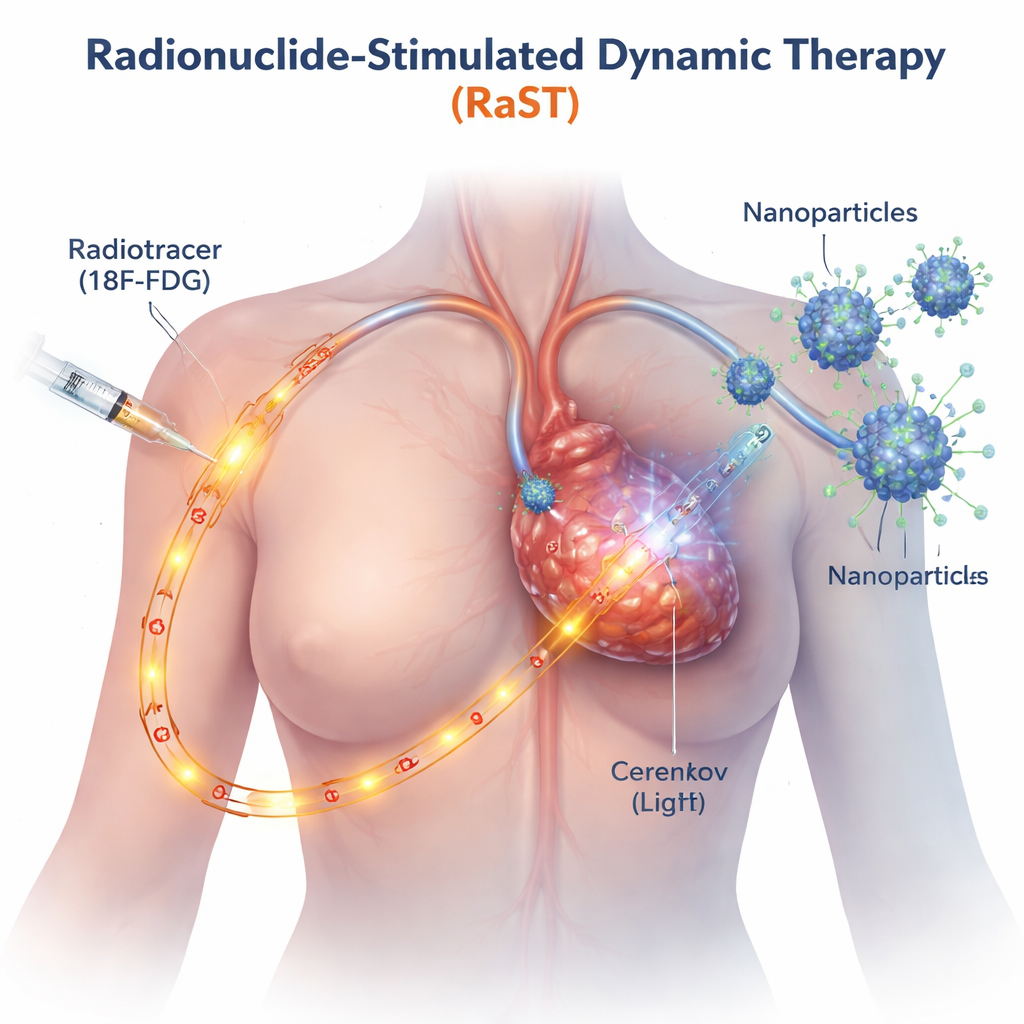
Attivare due percorsi distinti di morte cellulare
Il gruppo voleva capire non solo se RaST uccidesse le cellule tumorali, ma anche come. Utilizzando diverse linee cellulari di cancro al seno aggressive in laboratorio, hanno scoperto che dosi calibrate di tracciante radioattivo e nanoparticelle lavoravano insieme per danneggiare le cellule tumorali più efficacemente di ciascun componente da solo, anche in tipi noti per resistere alla chemioterapia standard. Imaging dettagliato e misurazioni delle proteine hanno rivelato che RaST attivava due programmi regolati di morte cellulare contemporaneamente. Uno era l’apoptosi, spesso descritta come “suicidio” cellulare, in cui le cellule si smantellano in modo ordinato. L’altro era la necroptosi, una forma più esplosiva di morte cellulare in cui le cellule si gonfiano, si rompono e riversano segnali molecolari di sofferenza nell’ambiente circostante. Questi segnali, noti come molecole associate a danno e citochine infiammatorie, possono funzionare come segnali luminosi che attraggono e attivano le cellule immunitarie.
Arruolare il sistema immunitario per un controllo duraturo
Per verificare se questo stile infiammatorio di uccisione tumorale fosse rilevante negli organismi viventi, i ricercatori hanno testato RaST in modelli murini di cancro al seno. Nei topi privi di difese immunitarie chiave, RaST fece poco per arrestare la crescita tumorale o la diffusione ai polmoni, nonostante generasse molta morte cellulare locale. Ma nei topi con sistemi immunitari integri, lo stesso trattamento ha prodotto risposte tumorali parziali e complete e ha impedito la metastasi ai polmoni. I tumori esposti a RaST sono diventati pieni di cellule immunitarie—specialmente cellule mieloidi come macrofagi e cellule dendritiche—abituate a inglobare materiale morto e presentare frammenti tumorali alle cellule T. Gli esami del sangue hanno mostrato ondate nel tempo di segnali che stimolano e regolano l’immunità, suggerendo che RaST prima innesca un attacco contro il cancro e successivamente tende verso uno stato più bilanciato man mano che i tumori si riducono o si stabilizzano.
Alla ricerca dei residui nascosti e protezione contro le recidive
Anche nei topi in cui i tumori sembravano completamente curati da RaST, un colorante per imaging altamente sensibile rivelò in seguito piccole sacche di cellule tumorali residue nascoste all’interno dei linfonodi. In modo notevole, questi animali non svilupparono comunque nuovi tumori o metastasi a distanza per molti mesi. Analisi chimiche mostrarono che le nanoparticelle di biossido di titanio, inizialmente abbondanti in ossa e fegato, si ridistribuirono gradualmente alla milza e ai linfonodi—proprio i nodi in cui pattugliano le cellule immunitarie. Questa lenta migrazione probabilmente mantiene una fonte locale di ossigeno reattivo disponibile per le cellule immunitarie, aiutandole a riconoscere e controllare questi residui tumorali nascosti prima che possano ricrescere o diffondersi.
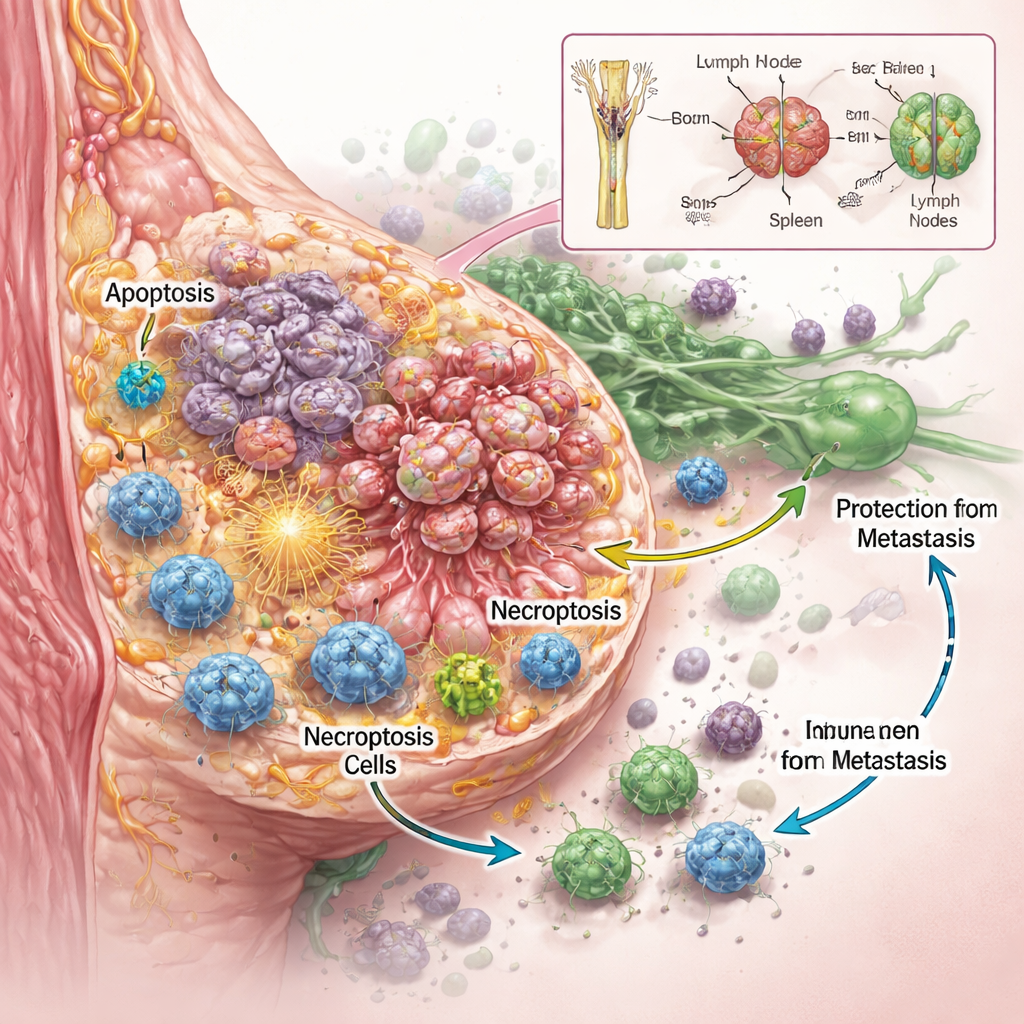
Cosa potrebbe significare per la cura futura del cancro
In termini semplici, questo lavoro mostra che RaST è più di un altro metodo per avvelenare le cellule tumorali. Combinando traccianti radioattivi, nanoparticelle sensibili alla luce e le difese naturali del corpo, spinge le cellule tumorali verso due forme di morte programmata che avvertono rumorosamente il sistema immunitario. Negli animali immunocompetenti, questo porta a un controllo duraturo dei tumori mammari aggressivi e blocca le metastasi, anche quando alcune cellule tumorali permangono nei linfonodi. Pur restando molto da fare prima che questo approccio possa essere ampiamente testato nell’uomo, lo studio indica la strada verso trattamenti futuri che non mirano semplicemente a ridurre le dimensioni dei tumori, ma a rimodellare il rapporto tra cancro, morte cellulare e immunità in modo che il corpo stesso contribuisca a mantenere la malattia sotto controllo nel lungo periodo.
Citazione: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Parole chiave: cancro al seno, nanoparticelle, immunoterapia, terapia con radionuclidi, necroptosi