Clear Sky Science · it
La glicofagia è una via bilateriana antica che sostiene l’adattamento metabolico attraverso l’evoluzione strutturale di STBD1
Come le ostriche rivelano trucchi nascosti per l’energia
Gli animali sopravvivono ai periodi difficili attingendo alle riserve di combustibile immagazzinate, ma non tutti si affidano allo stesso tipo di “batteria”. Questo studio esamina l’ostrica del Pacifico e mostra che, a differenza di molti altri animali che fanno affidamento sui grassi, le ostriche dipendono fortemente dallo zucchero immagazzinato sotto forma di glicogeno. Il lavoro mette in luce una via cellulare poco nota — chiamata glicofagia — che aiuta le ostriche a svuotare e riempire rapidamente le loro riserve di zucchero, e traccia come questo sistema si sia evoluto nel regno animale.
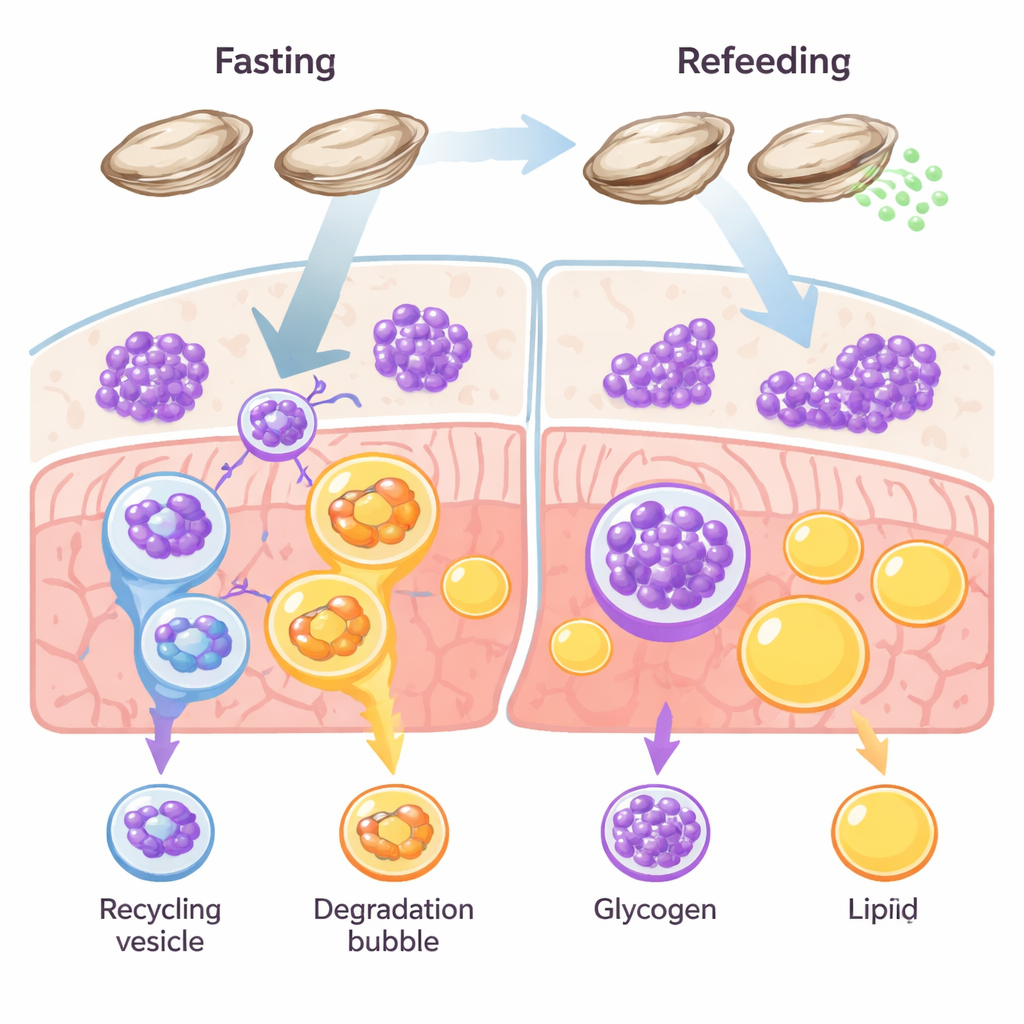
Una strategia di sopravvivenza centrata sullo zucchero
La maggior parte degli animali gestisce diverse riserve energetiche, principalmente grasso e glicogeno. Nei vertebrati come pesci e mammiferi, il grasso di solito domina come riserva a lungo termine. Le ostriche infrangono questa regola. I loro tessuti sono pieni di glicogeno, e ricerche precedenti suggerivano che questi molluschi consumino zucchero, piuttosto che grasso, quando il cibo scarseggia o durante la produzione di uova e spermatozoi. Gli autori hanno voluto verificare se la glicofagia — una degradazione mirata del glicogeno all’interno delle cellule — agisca come via principale di sopravvivenza nelle ostriche durante digiuno e recupero.
Osservare le cellule che passano dallo stoccaggio alla spesa
Il team ha tenuto le ostriche del Pacifico a digiuno per due settimane per poi rifocillarle, monitorando nel tempo la risposta dei loro tessuti. Durante il digiuno, colorazioni microscopiche hanno mostrato un aumento dei marcatori dell’autofagia — segnali di “pulizia” cellulare — esattamente nei punti dove era immagazzinato il glicogeno, mentre il glicogeno stesso diminuiva. Le riserve di grasso, al contrario, sono cambiate molto poco. Quando le ostriche sono state nutrite di nuovo, il glicogeno è tornato rapidamente e i segnali di autofagia sono diminuiti. Allo stesso tempo, i livelli di una proteina recettore chiave chiamata STBD1, che collega specificamente il glicogeno alla macchina dell’autofagia, sono aumentati e diminuiti in sincronia con l’uso del glicogeno. Un altro recettore collegato al riciclo dei grassi, p62, è rimasto per lo più stabile. Nel loro insieme, questi schemi indicano una via di riciclo dedicata e focalizzata sullo zucchero: la glicofagia, non la lipofagia dei grassi, è quella che sostiene l’equilibrio energetico delle ostriche.
Il gancio molecolare che afferra il glicogeno
La glicofagia dipende da STBD1 che agisce come un gancio molecolare: si lega al glicogeno e lo consegna a piccoli adattatori che costruiscono vescicole di riciclo. Nelle ostriche, STBD1 è risultato cablato in modo diverso rispetto al suo omologo nei vertebrati. La proteina dell’ostrica porta la sua regione che cattura il glicogeno, nota come dominio CBM20, nella parte anteriore (N-terminale), mentre lo STBD1 dei vertebrati piazza lo stesso modulo nella parte posteriore (C-terminale) e include una coda grassa aggiuntiva che lo ancora alle membrane cellulari. Modelli e simulazioni al computer hanno suggerito che la disposizione N-terminale dell’ostrica conferisce al CBM20 una presa più forte e più versatile sulle catene zuccherine ramificate. Esperimenti di laboratorio hanno confermato questo risultato: lo STBD1 purificato dell’ostrica legava il glicogeno più saldamente rispetto a STBD1 di pesce o topo, e quando tutte le versioni sono state espresse in cellule umane, la proteina dell’ostrica ha determinato un calo più netto del glicogeno durante l’autofagia indotta.
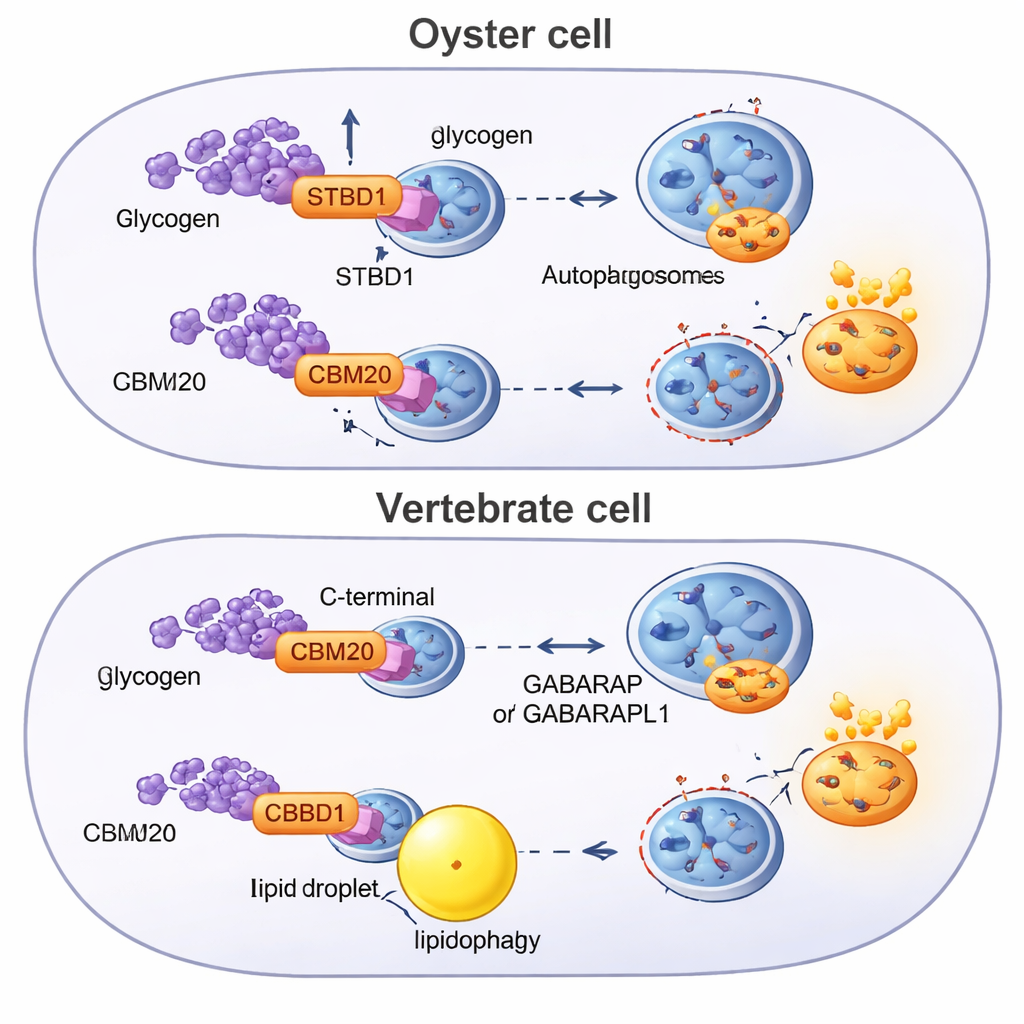
Riprogettare una via antica attraverso gli animali
Per capire da dove provenga questo sistema, i ricercatori hanno scandagliato i genomi di dozzine di animali alla ricerca di proteine contenenti CBM20 e hanno costruito alberi evolutivi. Hanno scoperto che STBD1 è un’invenzione dei bilateri — comparsa nell’antenato comune degli animali con piani corporei bilaterali — ma la sua struttura è stata rimescolata in diversi lignaggi. Le ostriche e altri lophotrocozoa tendono a mantenere il disegno ancestrale con CBM20 N-terminale, talvolta duplicando persino il modulo legante gli zuccheri. I cordati, il gruppo che include i vertebrati, mostrano una versione distinta in cui il CBM20 è stato spostato nella coda della proteina. Questo rimaneggiamento si correla con un legame meno forte al glicogeno e con una strategia metabolica che fa più affidamento sulla degradazione dei grassi tramite la lipofagia, supportata da altri recettori dell’autofagia e proteine adattatrici assenti nelle ostriche.
Cosa significa per le scelte energetiche della vita
Per i non specialisti, il messaggio principale è che gli animali hanno evoluto più di un modo per superare le carenze energetiche. Le ostriche mostrano una strategia antica centrata sullo zucchero: una versione ad alta affinità di STBD1 cattura rapidamente il glicogeno e lo convoglia nelle unità di riciclo cellulare, rendendo la glicofagia una fonte primaria di energia durante lo stress. I vertebrati, al contrario, sembrano aver scambiato parte di quella presa forte sullo zucchero per un approccio più bilanciato o orientato ai grassi, supportato da diversi partner proteici e disposizioni di domini. Collegando la struttura dettagliata delle proteine alle scelte di combustibile dell’organismo nel suo complesso, questo studio illustra come piccole “ricablaggi” molecolari possano aiutare diversi rami dell’albero animale ad adattarsi ai propri ambienti e stili di vita.
Citazione: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Parole chiave: glicofagia, metabolismo del glicogeno, biologia delle ostriche, autofagia, evoluzione del metabolismo