Clear Sky Science · it
Rimodellamento epigenetico e metabolico nei feocromocitomi e paragangliomi metastatici guidato da mutazioni SDHB
Perché questi tumori rari sono importanti
I feocromocitomi e i paragangliomi sono tumori rari che originano da cellule nervose produttrici di ormoni, spesso in prossimità delle ghiandole surrenali. La maggior parte cresce lentamente e può essere curata con la chirurgia, ma circa uno su cinque finisce per diffondersi in altri organi diventando potenzialmente letale. Questo studio pone una domanda semplice ma cruciale: cosa rende alcuni di questi tumori pericolosi? Analizzando in profondità come questi tumori attivano o disattivano i geni e come si alimentano, i ricercatori scoprono una vulnerabilità nascosta che un giorno potrebbe essere bersaglio di nuovi trattamenti.
Dalla crescita silenziosa alla diffusione letale
Il gruppo si è concentrato sui tumori che portano alterazioni in un gene chiamato SDHB. SDHB aiuta i mitocondri—le centrali energetiche della cellula—a eseguire una parte del ciclo di Krebs, una via fondamentale per la produzione di energia. Quando SDHB è danneggiato, si accumula una molecola chiamata succinato e le cellule cominciano a comportarsi come se vivessero in condizioni di bassa ossigenazione, anche quando non è così. I ricercatori hanno studiato campioni tissutali di 34 pazienti, confrontando tumori rimasti localizzati con quelli già metastatizzati. Usando una mappa ad alta risoluzione della “metilazione” del DNA, che mostra come le etichette chimiche modulano l’attività dei geni, hanno scoperto che i tumori metastatici presentavano un pattern più marcato di silenziamento genico rispetto a quelli benigni, soprattutto quando era presente la mutazione SDHB.
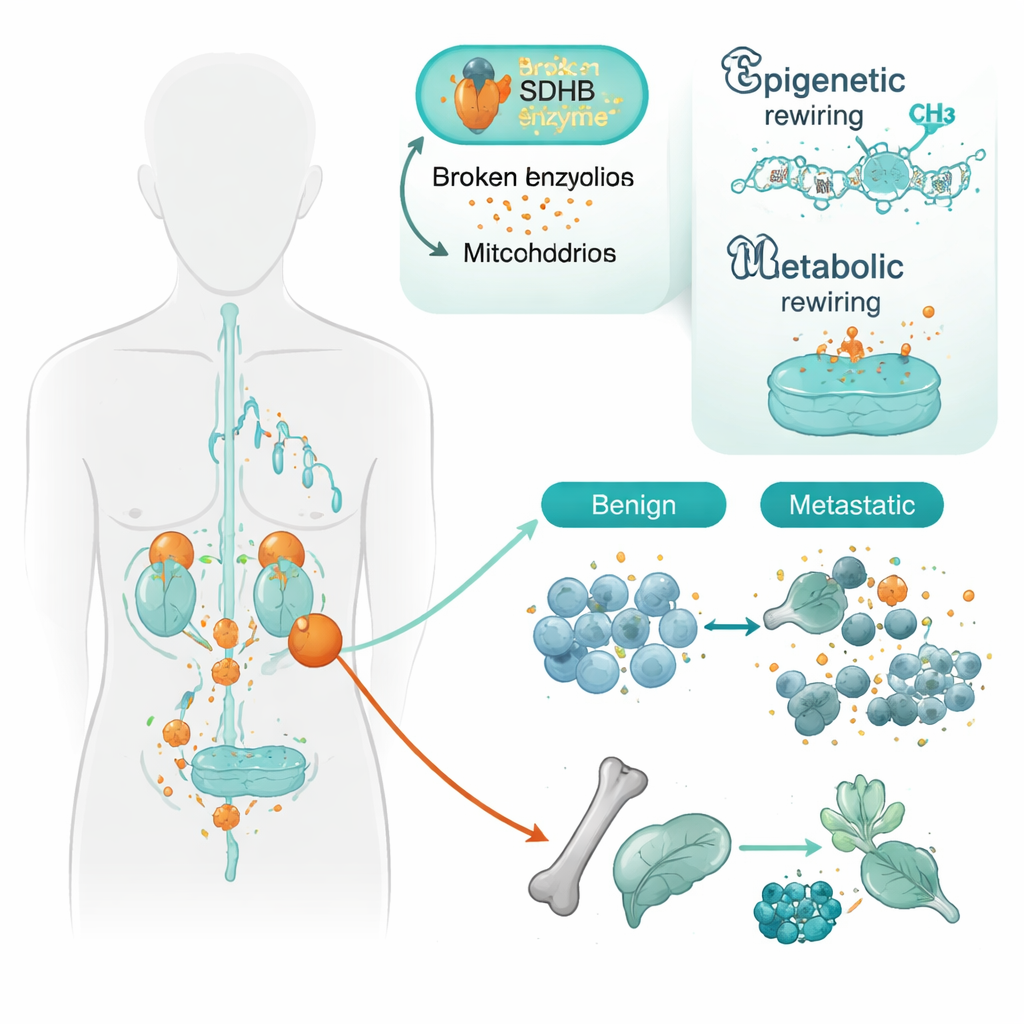
Riprogrammare l’identità cellulare
Molti dei geni silenziati nei tumori aggressivi erano quelli che aiutano le cellule nervose a maturare e a mantenere la loro identità specializzata. Tra questi vi sono famiglie di geni che guidano l’adesione cellulare, l’organizzazione del DNA e la determinazione del tipo cellulare. Un esempio di rilievo è stato il gene di adesione cellulare PCDHGC3. Anche in tumori SDHB‑mutanti non metastatici, la regione di controllo di questo gene era già in parte spenta; nei tumori metastatizzati il silenziamento era ancora più pronunciato. Un altro gene, SATB2, coinvolto nell’organizzazione di ampi tratti di DNA, risultava silenziato solo nei tumori metastatici, indipendentemente dallo stato di SDHB. Nel complesso, questi pattern suggeriscono che la perdita di SDHB “prepara” le cellule a uno stato meno maturo e più mobile, e cambiamenti epigenetici ulteriori le aiutano poi a staccarsi e a diffondersi.
Rimodellamento del modo in cui i tumori consumano zuccheri
Con sorpresa, non tutte le modificazioni riguardavano il silenziamento genico. Un insieme più ridotto di geni diventava meno metilato e più attivo, e questi erano fortemente coinvolti nel trasporto degli zuccheri nelle cellule. Tra questi, è emerso particolarmente il gene trasportatore del fruttosio SLC2A5. Il suo prodotto, noto come GLUT5, trasporta il fruttosio—uno zucchero comune nella frutta e in molti alimenti lavorati—all’interno delle cellule. In modelli di laboratorio di cellule simili a tumori esposte a bassa ossigenazione, SLC2A5 si attivava progressivamente, mentre altri trasportatori di zuccheri rispondevano in modo meno coerente. Gli autori hanno poi creato colture cellulari derivate da pazienti con PPGL e hanno mostrato che quando il glucosio era scarso, l’aggiunta di fruttosio aiutava queste cellule a continuare a proliferare, specialmente in condizioni di bassa ossigenazione che imitano l’ambiente tumorale.
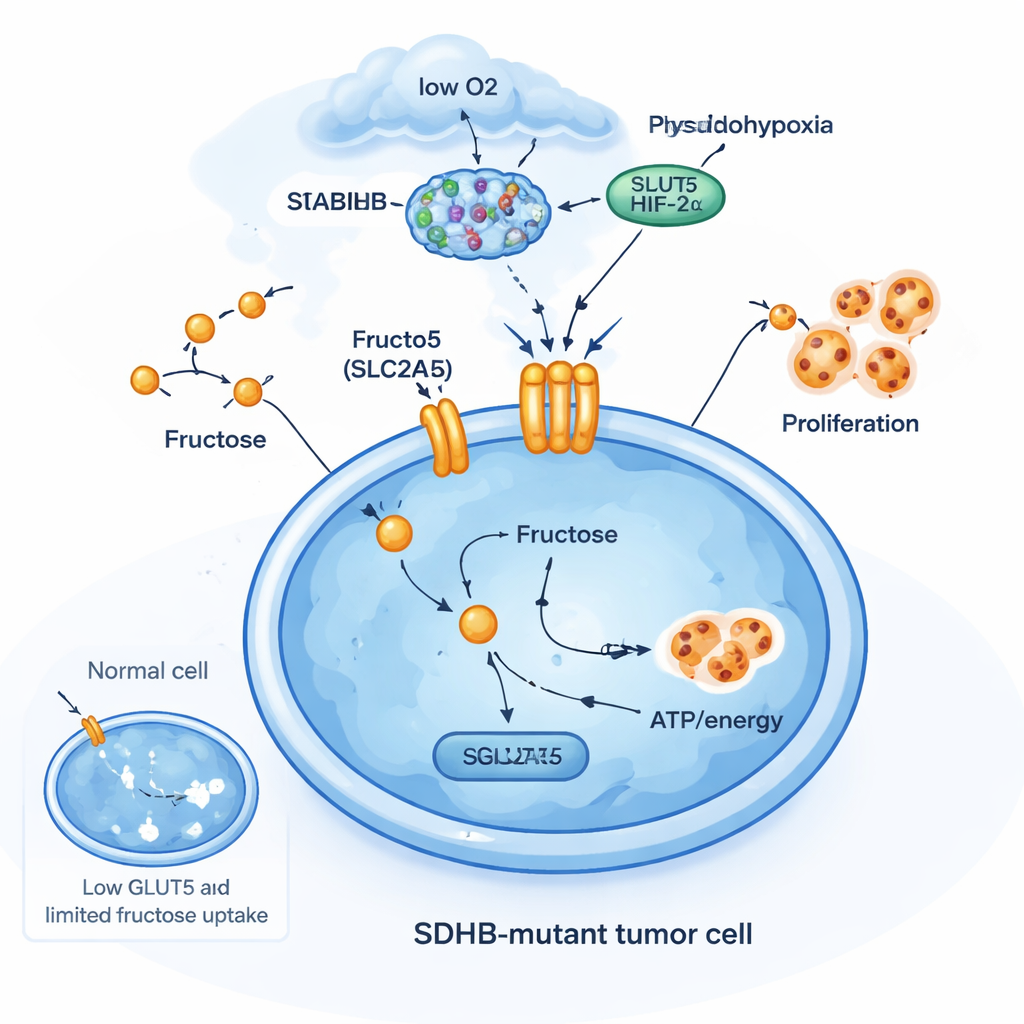
Un trucco di sopravvivenza alimentato dal fruttosio
Per capire perché le mutazioni SDHB contano in questo contesto, il team ha modificato diversi tipi cellulari rimuovendo SDHB. In cellule di tipo cromaffine della ghiandola surrenale e in una linea di carcinoma renale con attivazione costitutiva del fattore sensibile all’ossigeno HIF2α, la perdita di SDHB ha aumentato i livelli di SLC2A5. Ma in linee cellulari tumorali più comuni, che non presentavano queste caratteristiche neuroendocrine o di HIF2α, lo stesso knockout di SDHB non induceva SLC2A5. Questo dimostra che il trasportatore di fruttosio non fa parte di una risposta allo stress generica; è un adattamento altamente specifico in certi tipi cellulari che vivono già in uno stato di “pseudo‑ipossia”. In queste cellule, la perdita di SDHB, l’accumulo di succinato e l’attività di HIF2α cooperano per aprire una nuova porta metabolica: l’assorbimento di fruttosio per alimentare la crescita quando ossigeno e glucosio sono limitati.
Cosa significa per i pazienti
In termini semplici, lo studio rivela un doppio cambiamento nei PPGL metastatici con mutazione SDHB. Primo, il loro sistema di controllo del DNA è rimodellato per spingere le cellule verso uno stato meno specializzato e più plastico, incline all’invasione. Secondo, il loro sistema energetico è riconfigurato per sfruttare il fruttosio come combustibile alternativo in nicchie difficili, povere di ossigeno e di glucosio. Identificando il trasportatore del fruttosio SLC2A5/GLUT5 come un attore chiave in questo processo, il lavoro indica un possibile tallone d’Achille: bloccare l’assorbimento o il metabolismo del fruttosio potrebbe affamare selettivamente questi tumori risparmiando la maggior parte dei tessuti normali. Sebbene tali terapie non siano ancora disponibili, mappare questo paesaggio epigenetico e metabolico è un passo cruciale verso trattamenti più precisi, focalizzati sul metabolismo, per i pazienti con PPGL SDHB‑mutanti ad alto rischio.
Citazione: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Parole chiave: feocromocitoma, paraganglioma, mutazione SDHB, epigenetica, metabolismo del fruttosio