Clear Sky Science · it
Analisi multi-omica delle reti di segnalazione umane di PHACTR1
Perché questo gene dei vasi sanguigni conta per te
Infarti, ictus e ipertensione riconducono tutti alla salute dei nostri vasi sanguigni. Un singolo gene chiamato PHACTR1 è emerso ripetutamente negli studi genetici su larga scala di queste condizioni, ma i ricercatori non avevano capito il perché. Questo studio ha adottato uno sguardo ampio e «a tutti i livelli» all’interno delle cellule umane per mappare ciò che PHACTR1 fa realmente, rivelando come possa influenzare crescita cellulare, uso di energia e gestione del ferro—processi che in ultima analisi plasmano la salute delle arterie.
Una scansione d’insieme all’interno delle cellule
Invece di concentrarsi su una molecola alla volta, i ricercatori hanno utilizzato una strategia chiamata multi-omica—misurando simultaneamente migliaia di RNA, proteine, piccoli metaboliti e lipidi nelle cellule. Hanno modificato geneticamente cellule umane per produrre PHACTR1 in eccesso oppure con il gene attenuato, riproducendo differenze genetiche naturali riscontrate nelle persone. Confrontando queste cellule alterate con controlli normali attraverso quattro livelli molecolari e immettendo poi i dati in software di analisi dei percorsi, hanno costruito una mappa globale di come la variazione di PHACTR1 riverbera nella macchina cellulare interna. 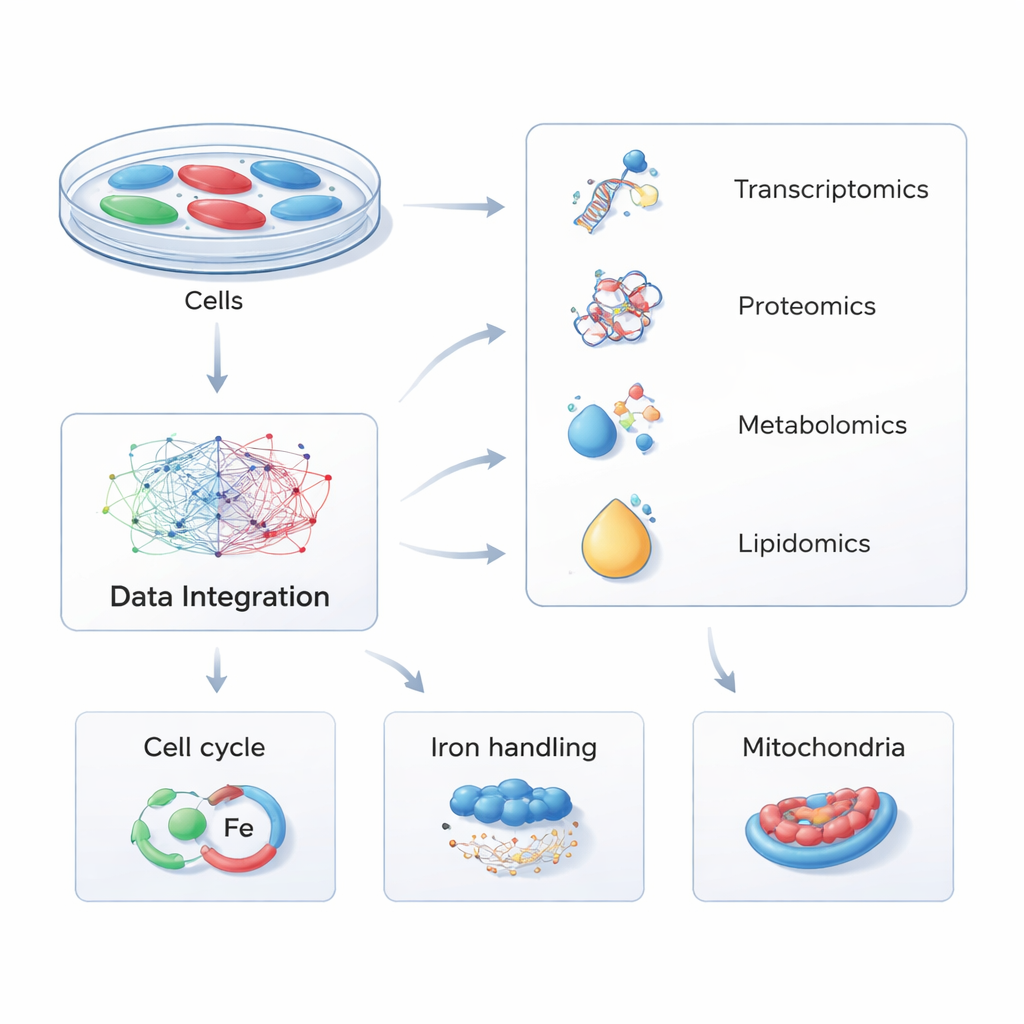
Oltre lo scheletro cellulare: controllo dei cicli di crescita
PHACTR1 era conosciuto principalmente per il suo ruolo nell’organizzazione dell’impalcatura interna di filamenti di actina. I nuovi dati hanno mostrato che ha anche un ruolo significativo nel controllo del ciclo cellulare—la coreografia con cui le cellule copiano il DNA e si dividono. Le cellule con PHACTR1 in eccesso sono uscite dalla fase di riposo G1 e si sono accumulate nelle fasi di copia del DNA e pre-divisione, con meno cellule che entravano con successo nella mitosi completa. Sono risultati alterati regolatori chiave come Ciclin B1, Cdt1 e altre proteine del ciclo cellulare. Quando il team ha ripetuto gli esperimenti in cellule endoteliali primarie umane—le cellule che rivestono i vasi sanguigni—ha nuovamente osservato cambiamenti nei regolatori fondamentali del ciclo cellulare. Ciò suggerisce che PHACTR1 contribuisca a decidere quando le cellule vascolari riposano, si dividono o si bloccano, un equilibrio cruciale sia nella riparazione delle pareti vascolari sia nella formazione di crescite tissutali pericolose.
Gestire il ferro e proteggere dai danni
L’integrazione multi-omica ha indicato anche percorsi legati al ferro e una forma specializzata di morte cellulare guidata dal ferro chiamata ferroptosi. Sebbene le cellule non fossero in fase attiva di ferroptosi, l’aumento di PHACTR1 ha ridotto i livelli di importanti proteine di gestione del ferro, inclusa la catena pesante della ferritina (l’involucro principale di immagazzinamento del ferro) e l’eme ossigenasi 1 (che ricicla il ferro dall’eme). Nelle cellule endoteliali primarie, PHACTR1 ha alterato similmente queste proteine e i principali difensori contro il danno ossidativo. Poiché un cattivo controllo del ferro può alimentare infiammazione, stress ossidativo e placche arteriose instabili, questi risultati suggeriscono che PHACTR1 possa modulare come le cellule vascolari immagazzinano e detossificano il ferro, influenzando potenzialmente la suscettibilità a determinate malattie vascolari.
Mitocondri, energia e salute delle arterie
Un’altra sorpresa è stato il ruolo di PHACTR1 nei mitocondri, le centrali energetiche della cellula. Il team ha trovato la proteina PHACTR1 all’interno di mitocondri isolati e ha osservato che modificarne i livelli rimodellava la rete mitocondriale. Quando PHACTR1 era elevato, i mitocondri risultavano più allungati, e una proteina chiamata Drp1 mostrava una modifica chimica in un sito che riduce la scissione mitocondriale. I livelli di una proteina impalcatura, AKAP1, che aiuta a organizzare la segnalazione sulla superficie mitocondriale, aumentavano e diminuivano in sincronia con PHACTR1. Questi cambiamenti strutturali corrispondevano a variazioni nella produzione di energia: PHACTR1 alto riduceva la produzione mitocondriale di ATP ed era associato all’accumulo di alcuni metaboliti derivati dagli acidi grassi che segnalano un rallentamento nella combustione dei lipidi, mentre PHACTR1 basso spingeva le cellule a dipendere maggiormente dalla glicolisi, la degradazione degli zuccheri. Analisi di campioni di arterie umane hanno mostrato che PHACTR1 e AKAP1 tendono a essere attivati insieme, collegando direttamente questo circuito di controllo mitocondriale ai vasi sanguigni reali. 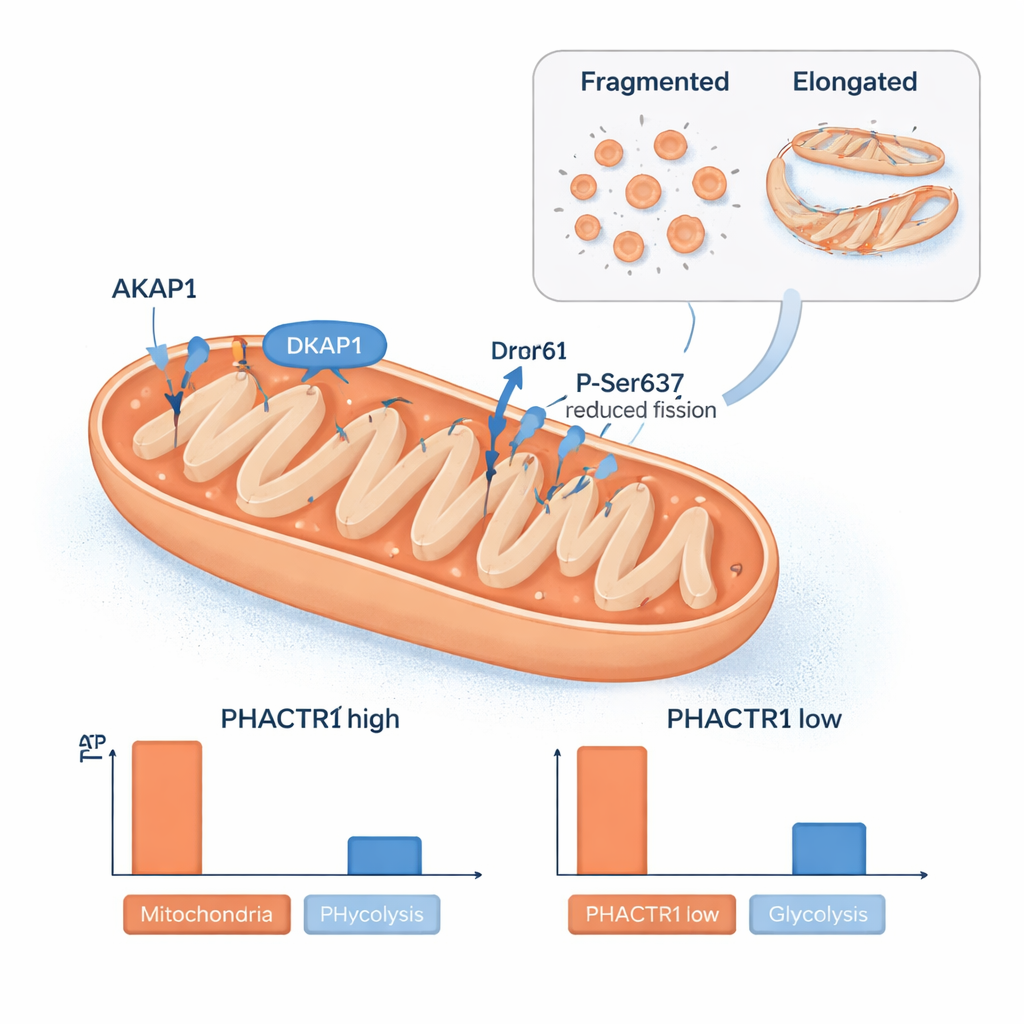
Cosa significa tutto questo per i vasi sanguigni
Nel complesso, questo lavoro dimostra che PHACTR1 non è un gene a scopo unico ma un coordinatore master che tocca i modi in cui le cellule vascolari si dividono, immagazzinano il ferro e si alimentano. Mappando queste connessioni attraverso migliaia di molecole, lo studio aiuta a spiegare perché le differenze naturali in PHACTR1 sono associate a un’ampia gamma di malattie vascolari—dalla malattia coronarica a rotture arteriose spontanee e emicrania. Per il pubblico non specialista, il messaggio è che un gene individuato dalla genetica umana ora viene ricondotto a comportamenti cellulari concreti che influenzano la crescita delle placche, la stabilità dei vasi e l’equilibrio energetico. Col tempo, comprendere queste reti controllate da PHACTR1 potrebbe aprire la strada a terapie più precise che modulino i cicli cellulari, la gestione del ferro o la funzione mitocondriale per riportare a uno stato più sano le persone a rischio di malattie cardiovascolari.
Citazione: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Parole chiave: PHACTR1, malattie vascolari, multi-omica, mitocondri, metabolismo del ferro