Clear Sky Science · it
Mirare PAK4 favorisce la piropotosi indotta da Gemcitabina nel cancro del pancreas tramite l’asse NLRP1/caspasi-3/GSDME
Perché uccidere le cellule tumorali in modo “fiammante” potrebbe fare la differenza
Il cancro del pancreas è tra i tumori più letali e anche i nostri migliori farmaci chemioterapici spesso smettono di funzionare quando i tumori sviluppano resistenza. Questo studio esplora una svolta sorprendente: lo stesso farmaco, la gemcitabina, può uccidere le cellule tumorali in modo più esplosivo e infiammatorio chiamato piropotosi—se un importante “freno” molecolare chiamato PAK4 viene spento. Comprendere e mirare a questo freno potrebbe rendere i trattamenti esistenti più efficaci per molti pazienti.
Un cancro ostinato che elude le terapie
L’adenocarcinoma duttale pancreatico viene solitamente diagnosticato in fase avanzata e risponde male alle terapie, quindi la gemcitabina resta un caposaldo nonostante i suoi limiti. La gemcitabina normalmente uccide le cellule tramite apoptosi, una forma ordinata e “silenziosa” di morte cellulare programmata. Ma più della metà dei tumori pancreatici esaminati in questo studio produceva alti livelli di una proteina chiamata GSDME, che può trasformare questa morte silenziosa in piropotosi—una forma rapida di morte cellulare che provoca danneggiamento della membrana e il rilascio di segnali infiammatori. Questo ha sollevato una domanda chiave: se i tumori possono andare incontro a piropotosi, perché così tanti resistono ancora alla gemcitabina?
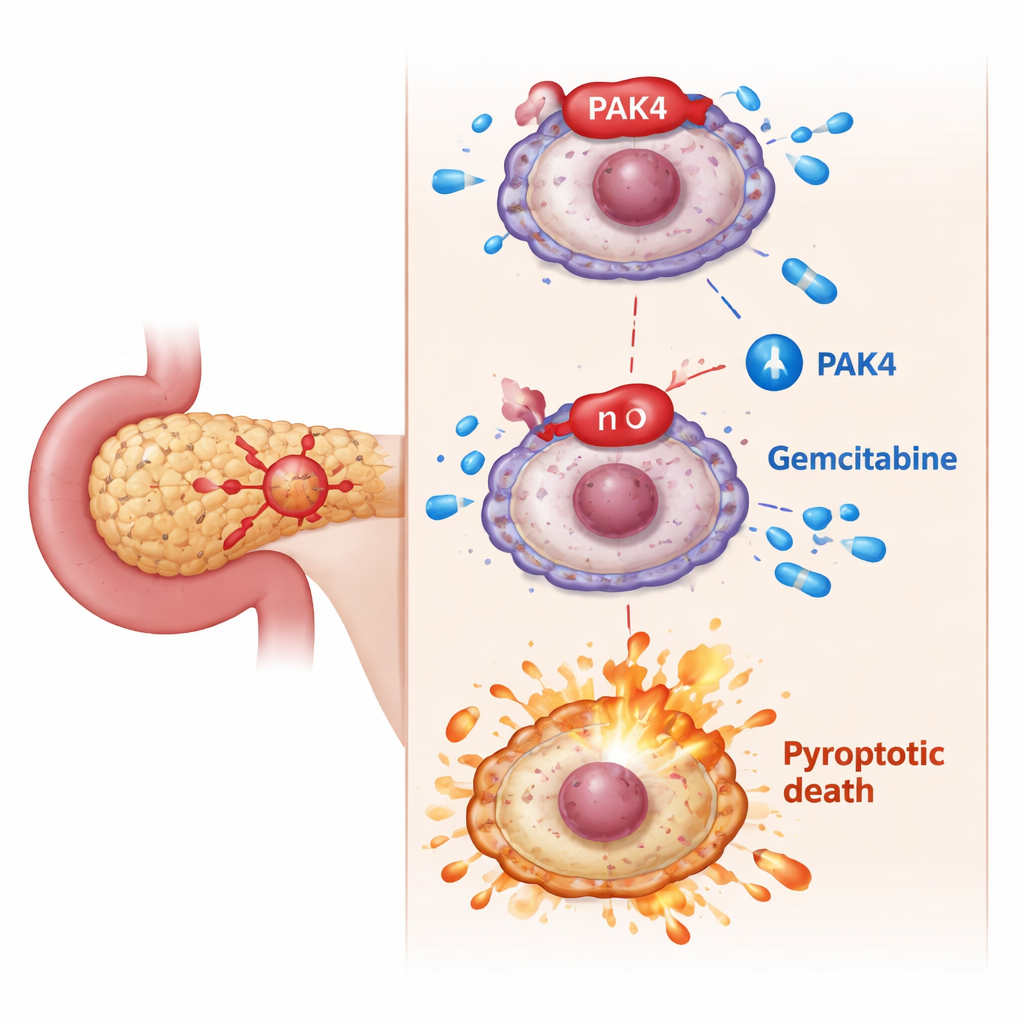
Il freno nascosto: PAK4 blocca la morte cellulare “fiammante”
I ricercatori si sono concentrati su PAK4, una proteina che promuove la crescita nota per essere iperattiva nel cancro pancreatico e collegata a una scarsa risposta alla gemcitabina. Negli esperimenti cellulari, le cellule tumorali con alti livelli di PAK4 erano più difficili da eliminare con la gemcitabina. Quando il gruppo ha ridotto PAK4, la gemcitabina è diventata improvvisamente molto più letale: le cellule hanno mostrato caratteristiche tipiche della piropotosi—rigonfiamento, bolle simili a palloni, rottura delle membrane e maggiore rilascio di contenuti intracellulari. A livello molecolare, questo cambiamento dipendeva dal fatto che GSDME venisse tagliata in un frammento attivo da un’altra proteina, la caspasi-3. Bloccare la caspasi-3 impediva a GSDME di innescare la piropotosi, confermando che PAK4 agisce normalmente come freno di questa via di morte.
Come PAK4 smantella l’allarme di morte della cellula
Approfondendo, gli scienziati hanno scoperto che PAK4 non attacca direttamente GSDME. Piuttosto, sabota un “sensore d’allarme” a monte chiamato NLRP1. Nei pazienti, livelli più alti di NLRP1 erano associati a una sopravvivenza migliore, suggerendo che aiuta l’organismo a tenere sotto controllo i tumori. Nelle cellule tumorali, quando NLRP1 veniva rimosso, la morte cellulare indotta da gemcitabina e l’attivazione di GSDME calavano nettamente, mostrando che NLRP1 alimenta la macchina della piropotosi. I livelli di PAK4 e NLRP1 erano inversamente correlati nei campioni tumorali: dove PAK4 era alto, NLRP1 era basso. Lo studio ha dimostrato che PAK4 attivo agisce tramite un’altra proteina, l’enzima E3 ligasi Mdm2, per marcare NLRP1 destinandolo alla distruzione dal sistema di smaltimento cellulare. Marcando NLRP1 in questo modo, PAK4 impedisce l’attivazione di una reazione a catena—attraverso caspasi-9 e caspasi-3—that normalmente culminerebbe nella piropotosi guidata da GSDME.
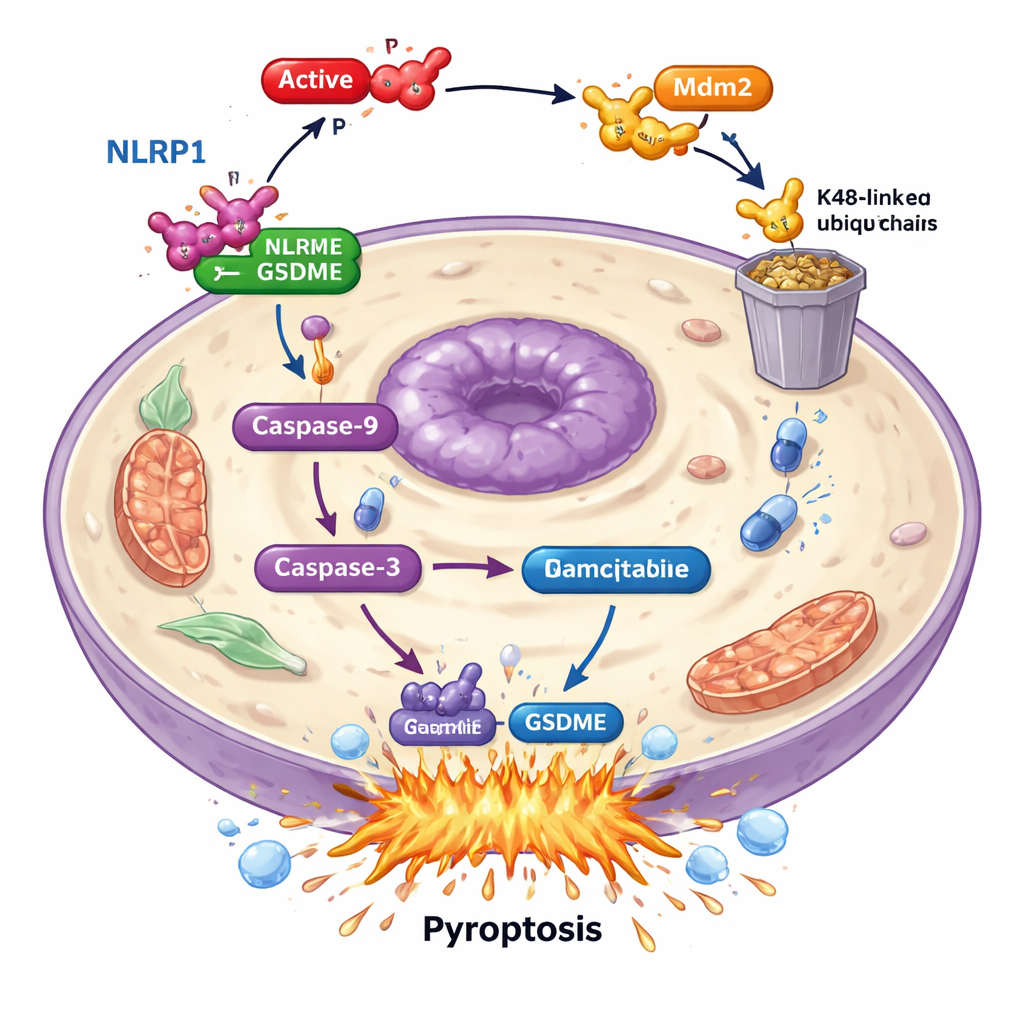
Spegnere PAK4 per potenziare la chemioterapia
Poiché PAK4 agisce da freno sulla piropotosi, il gruppo ha verificato se bloccarne l’attività potesse riattivare il potere citotossico della gemcitabina. Hanno usato un inibitore di PAK4 a piccola molecola chiamato PF-3758309. Da solo, questo inibitore spingeva già le cellule del cancro pancreatico verso la piropotosi, aumentando l’attivazione della caspasi-3, il taglio di GSDME e la rottura della membrana cellulare. In combinazione con la gemcitabina, l’effetto era ancora più marcato: più cellule morivano per piropotosi e i segnali molecolari della via di morte erano amplificati. Nei modelli murini portatori di tumori pancreatici umani, sia la riduzione di PAK4 sia il trattamento con l’inibitore di PAK4 hanno reso la gemcitabina più efficace nel ridurre i tumori e hanno aumentato i marcatori di piropotosi all’interno dei tumori.
Implicazioni per i pazienti e per le terapie future
In termini semplici, questo lavoro rivela una serratura molecolare—PAK4—that impedisce alle cellule del cancro pancreatico di morire in modo particolarmente distruttivo durante la chemioterapia. Disabilitando PAK4, i medici potrebbero essere in grado di spingere i tumori trattati con gemcitabina verso la piropotosi, rendendo il farmaco più efficace e potenzialmente stimolando il sistema immunitario contro il cancro. Pur richiedendo ulteriori studi in modelli derivati da pazienti e trial clinici, lo studio propone una strada chiara: mirare alla via PAK4–Mdm2–NLRP1–GSDME per convertire tumori resistenti in tumori sensibili, usando farmaci già disponibili in combinazioni più intelligenti.
Citazione: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Parole chiave: cancro del pancreas, resistenza alla gemcitabina, piropotosi, PAK4, terapia mirata