Clear Sky Science · it
La reversione fetale da linee diverse sostiene il pool di cellule staminali intestinali e conferisce resilienza allo stress
Come l’intestino si autoripara sotto attacco
Il rivestimento del tuo intestino è uno dei tessuti più indaffarati del corpo. Digerisce il cibo, assorbe nutrienti e protegge dai germi, il tutto mentre si rinnova ogni pochi giorni. Questo articolo esplora come quella superficie fragile sopravviva ad assalti severi — dall’infiammazione alla chemioterapia — riportando temporaneamente le cellule a uno stato più fetale e flessibile che favorisce la riparazione e la resistenza al danno.
La catena di montaggio quotidiana nell’intestino
Negli intestini sani, un gruppo specializzato di cellule chiamate cellule colonnari alla base della cripte (CBC) si trova sul fondo di piccole cavità note come cripte. Queste cellule simili a staminali si dividono continuamente e mandano i loro discendenti verso l’alto, verso i villi digitiformi che proiettano nel tubo intestinale. Durante il viaggio, le cellule maturano in ruoli diversi, come gli enterociti assorbenti che prelevano nutrienti, o le cellule secretorie che producono muco e composti antimicrobici. In condizioni normali, questo flusso dall’alto al basso mantiene il rivestimento intestinale rinnovato e ordinato.
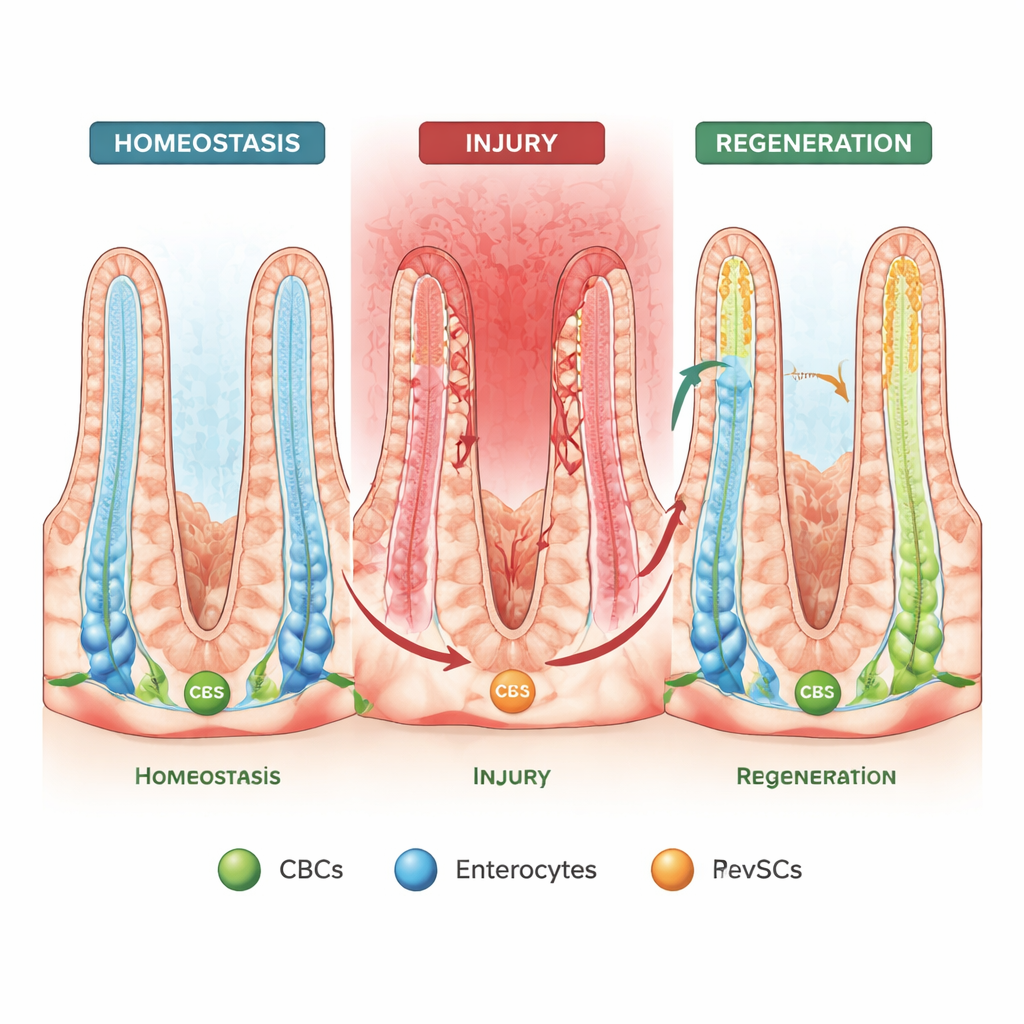
Cellule che possono invertire la catena di montaggio
Quando il rivestimento intestinale è danneggiato e le CBC vengono perse, lavori precedenti hanno mostrato che alcune cellule mature possono "camminare indietro" nella cripta e riacquisire capacità simili a quelle staminali, un comportamento chiamato plasticità spaziale. Un secondo fenomeno, più recente, è la "reversione fetale", in cui le cellule adottano un profilo di espressione genica che ricorda l’intestino in sviluppo. In questo studio, gli autori collegano queste due idee usando colture sofisticate di organoidi (mini-intestini), sequenziamento RNA a singola cellula e tracciamento delle linee cellulari nei topi. Identificano una popolazione speciale di tipo fetale chiamata cellule staminali di riviviscenza (revSCs) che può originare sia dalle CBC sia dagli enterociti assorbenti ordinari, e che poi rigenera l’intero insieme di tipi cellulari intestinali.
I mini-intestini rivelano una flessibilità nascosta
Per osservare questi cambiamenti in azione, il gruppo ha coltivato organoidi intestinali di topo e umani in due diversi gel. In Matrigel, gli organoidi si comportavano come tessuto adulto normale, ricchi di CBC e tipi cellulari maturi. In un gel di collagene, invece, gli organoidi divennero dominati da cellule simili alle revSC con una firma genica fetale. Le analisi a singola cellula mostrarono che le revSC potevano essere ricondotte lungo due percorsi principali: dalle CBC classiche e dagli enterociti assorbenti. Esperimenti di separazione confermarono che le CBC hanno la capacità maggiore di convertirsi in revSC, ma anche cellule più mature potevano farlo se collocate nell’ambiente giusto. In modo cruciale, revSC purificate potevano essere trasferite di nuovo in Matrigel e rigenerare CBC e tutte le principali linee intestinali, dimostrando che lo stato fetale è sia reversibile sia pienamente funzionale.
Cellule dei villi e danno nel mondo reale
Lo studio fa un passo avanti chiedendo se questa flessibilità appare anche fuori dal laboratorio. I ricercatori etichettarono gli enterociti nei villi dei topi e poi coltivarono frammenti di villo o esposero gli animali a un farmaco che danneggia l’intestino, il 5-fluorouracile (5-FU). In collagene, i frammenti di villo — normalmente considerati poveri di cellule staminali — formarono nuovi organoidi che adottarono caratteristiche da revSC e poi riacquisirono marcatori di CBC quando riportati alle condizioni standard. Quando trapiantati in modelli di colite, questi organoidi "derivati dai villi" ricostruirono un rivestimento intestinale sano. In topi vivi trattati con 5-FU, gli enterociti etichettati iniziarono a esprimere marcatori revSC, per poi riapparire come lunghe strisce clonali che includevano nuove CBC alla base della cripta, confermando che cellule mature erano intervenute per rifornire il pool di cellule staminali.
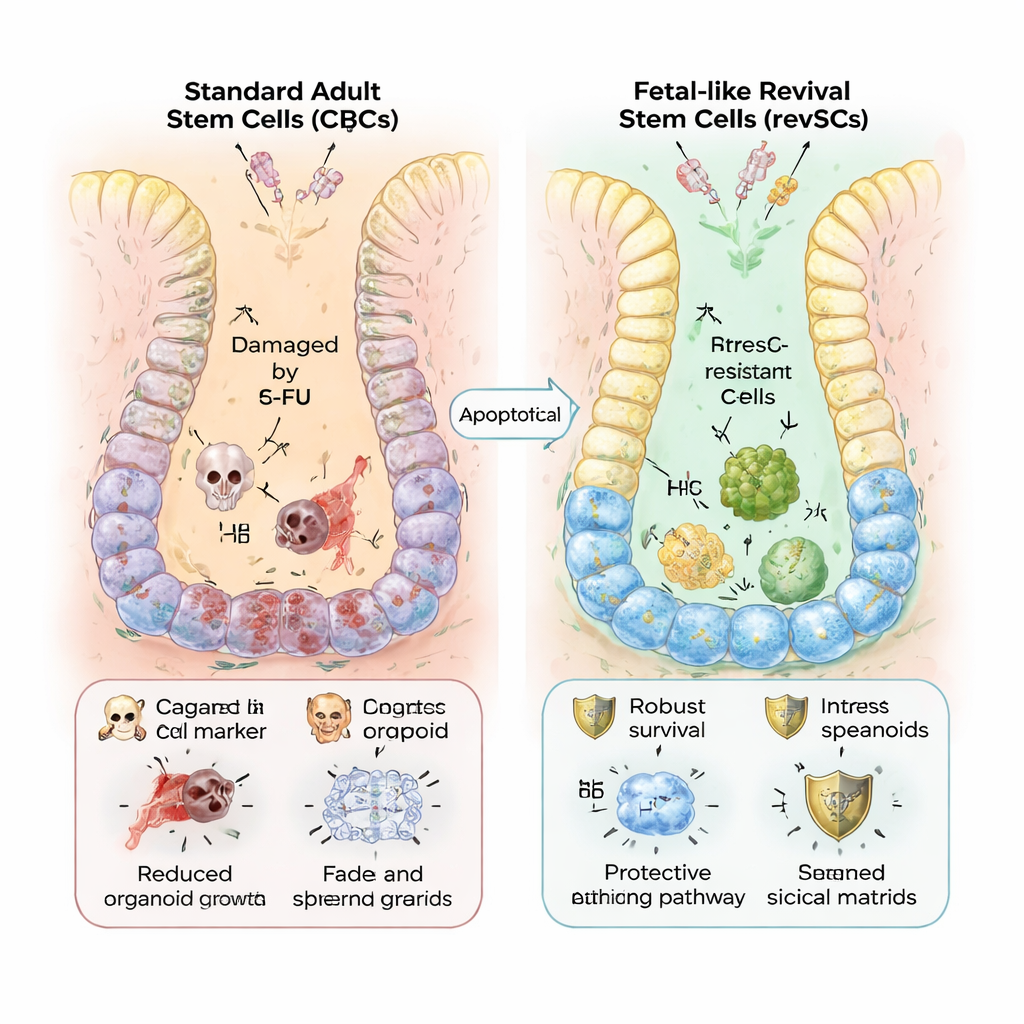
Squadre di riparazione resistenti allo stress
Perché ricorrere a questa deviazione fetale? Gli autori mostrano che le revSC sono molto più abili a sopportare lo stress. Quando gli organoidi furono messi alla prova con 5-FU, quelli in Matrigel standard si ridussero e mostrarono ampi programmi genici legati al danno al DNA e a una proliferazione frenetica. Gli organoidi coltivati in collagene, ricchi di revSC, al contrario continuarono a crescere e mostrarono una risposta più calma e mirata. Le analisi geniche rivelarono una maggiore attività dei sistemi antiossidanti, proteine anti-apoptotiche e chaperoni da shock termico — scudi molecolari che aiutano le cellule a sopravvivere a infiammazione e insulti tossici. Schemi simili furono osservati sia nelle cellule di topo sia in quelle umane, e gli stessi geni revSC risultano elevati negli intestini umani infiammati.
Che cosa significa per le malattie intestinali e la terapia
Per un non specialista, la conclusione è che il rivestimento intestinale possiede un piano di fuga d’emergenza incorporato. Quando l’infiammazione o i farmaci minacciano le sue cellule staminali abituali, sia le staminali sia le cellule assorbenti ordinarie possono temporaneamente ritornare a uno stato fetale, resistente allo stress, di tipo revSC. Da lì, possono ricreare il compartimento staminale normale e ricostruire il tessuto. Questo lavoro unifica due concetti di rigenerazione — la plasticità spaziale e la reversione fetale — in una singola gerarchia di riparazione, e suggerisce che sfruttare con attenzione questo programma flessibile e fetale potrebbe migliorare i trattamenti per condizioni come la malattia infiammatoria intestinale e il cancro colorettale, pur avvertendo che una reversione mal gestita potrebbe alimentare la crescita tumorale.
Citazione: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
Parole chiave: cellule staminali intestinali, rigenerazione tissutale, plasticità cellulare, malattia infiammatoria intestinale, organoidi