Clear Sky Science · it
La fluvastatina sopprime l’inizio e la progressione del cancro al seno tramite il targeting di CYP4Z1
Perché un farmaco per il colesterolo è rilevante nel cancro al seno
Molte donne trattate per il cancro al seno sviluppano alterazioni dei lipidi nel sangue e affrontano il rischio continuo di recidiva o di diffusione della malattia. Questo studio esplora un’idea interessante: una comune pillola per abbassare il colesterolo, la fluvastatina, potrebbe essere riproposta per rallentare o prevenire il cancro al seno neutralizzando una proteina che alimenta cellule tumorali particolarmente pericolose, simili a cellule staminali?
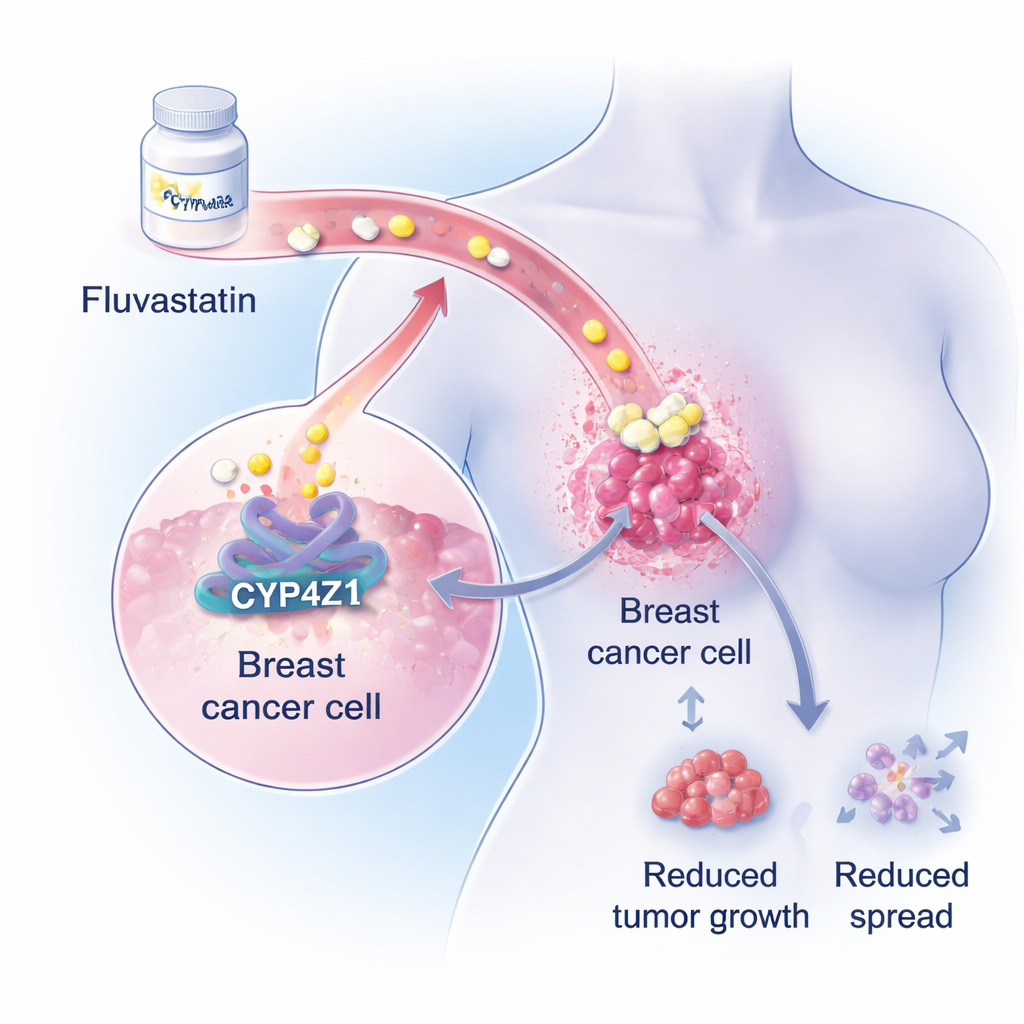
Un driver nascosto all’interno dei tumori mammari
I ricercatori si concentrano su una proteina poco nota chiamata CYP4Z1, presente a livelli elevati nelle cellule del cancro al seno ma non nel tessuto mammario sano. Lavori precedenti avevano mostrato che CYP4Z1 favorisce comportamenti simil-staminali nelle cellule tumorali — cellule in grado di auto-rinnovarsi indefinitamente, resistere alla chemioterapia e riavviare i tumori dopo il trattamento. In ampie analisi genetiche e biochimiche, il team dimostra ora che l’eccessiva attività di CYP4Z1 potenzia fortemente le vie di sintesi lipidica all’interno delle cellule del cancro al seno, in particolare la produzione di trigliceridi, un importante grasso di stoccaggio. Poiché molte pazienti con cancro al seno sviluppano già alterazioni lipidiche nel corso della chemioterapia, questo ruolo promuovente dei lipidi di CYP4Z1 ha suggerito una possibile applicazione per farmaci ipolipemizzanti esistenti.
Riproporre la fluvastatina dalla salute cardiaca alla cura del cancro
Per testare l’ipotesi, gli scienziati hanno vagliato una piccola libreria di 23 farmaci approvati dalla FDA utilizzati per abbassare i lipidi nel sangue. La fluvastatina, una statina ampiamente prescritta per il colesterolo alto, è emersa come particolarmente efficace: ha bloccato direttamente l’attività enzimatica di CYP4Z1 in modo dose-dipendente. A dosi molto meno dannose per le cellule mammarie normali rispetto a quelle tumorali, la fluvastatina ha ridotto nettamente marcatori chiave di “stemness”, la capacità delle cellule del cancro al seno di formare sfere tumorali flottanti e la loro capacità di migrare e invadere barriere simili a tessuti nei test di laboratorio. Ha anche aumentato la sensibilità delle cellule tumorali all’adriamicina, suggerendo che potrebbe potenziare i trattamenti esistenti.
Mettere alla prova il farmaco negli animali vivi
Il team ha poi valutato la fluvastatina in modelli murini. In topi impiantati con cellule umane di cancro al seno, un trattamento periodico con fluvastatina ha rallentato la crescita tumorale, ridotto i livelli di un marcatore di stemness (ALDH1A1) e del marcatore di proliferazione Ki67 nei tumori e diminuito il numero di noduli metastatici comparsi nei polmoni. È importante che i topi trattati con fluvastatina abbiano mantenuto il peso corporeo e non mostrato anomalie significative del sangue o del midollo osseo, a sostegno di un profilo di sicurezza favorevole alla dose testata. In un modello genetico più realistico — topi ingegnerizzati per sviluppare tumori mammari guidati da un gene oncogenico — i ricercatori hanno inoltre introdotto CYP4Z1 umano nel tessuto mammario. Questi topi hanno sviluppato più lesioni precancerose e cancerose, e più metastasi al fegato e ai polmoni, rispetto agli animali di controllo. Il trattamento con fluvastatina ha ridotto sostanzialmente sia il numero di lesioni mammarie sia le metastasi a distanza, in particolare nei topi che portavano il gene CYP4Z1 aggiuntivo.
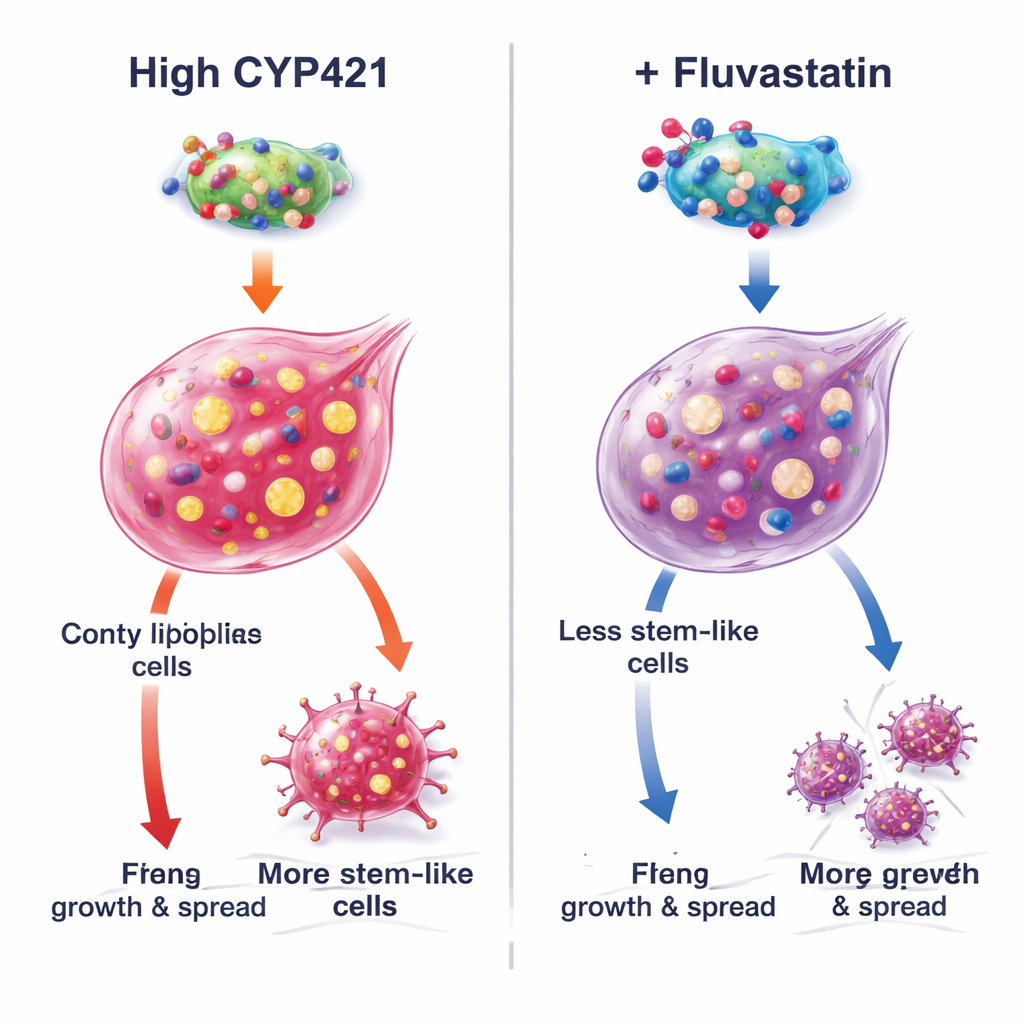
Come la fluvastatina disarma una proteina che promuove il cancro
Per comprendere il meccanismo, gli autori hanno combinato modellizzazione al computer con ingegneria proteica precisa. Hanno previsto che la fluvastatina si inserisca nel sito attivo di CYP4Z1 a tre aminoacidi critici (Lys109, Pro444 e Arg450). Quando questi siti sono stati mutati, l’attività di CYP4Z1 è diminuita e la fluvastatina non è più riuscita a inibirla ulteriormente, confermando tali posizioni come punti di ancoraggio. In cellule che naturalmente non esprimono CYP4Z1, l’introduzione della proteina normale ha aumentato la stemness e attivato la segnalazione proliferativa PI3K/AKT, mentre la fluvastatina ha invertito questi effetti. Le versioni mutanti di CYP4Z1 erano meno potenti e meno sensibili al farmaco. Esperimenti aggiuntivi hanno mostrato che l’effetto della fluvastatina si indeboliva quando la produzione di trigliceridi veniva artificialmente aumentata, o quando CYP4Z1 veniva silenziata, sottolineando che gli effetti più forti del farmaco derivano dal bloccare questa proteina specifica e le sue conseguenze nella sintesi lipidica piuttosto che dall’indurre la morte cellulare tramite ferroptosi guidata dal ferro.
Cosa significa per le pazienti
Complessivamente, lo studio suggerisce che la fluvastatina, oltre ad abbassare il colesterolo, può limitare le fasi iniziali e la diffusione successiva del cancro al seno in modelli sperimentali agendo su CYP4Z1, una proteina che guida il metabolismo dei lipidi e i comportamenti simil-staminali nei tumori. Poiché la fluvastatina è già approvata e la sua sicurezza è ben caratterizzata, questi risultati offrono una via promettente verso test clinici più rapidi come terapia aggiuntiva, in particolare nelle pazienti i cui tumori esprimono fortemente CYP4Z1. Pur richiedendo ulteriori studi per valutare l’approccio negli esseri umani e identificare eventuali bersagli aggiuntivi del farmaco, la ricerca apre la porta all’uso di un farmaco cardiologico familiare come parte di una nuova strategia contro i tumori mammari aggressivi e inclini alla recidiva.
Citazione: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Parole chiave: cancro al seno, fluvastatina, cellule staminali tumorali, metabolismo lipidico, riutilizzo di farmaci