Clear Sky Science · it
microRNA differenzialmente espressi nella corteccia temporale di pazienti con Alzheimer e la loro associazione con la patologia della tau
Perché piccoli interruttori cerebrali contano nell’Alzheimer
La malattia di Alzheimer priva lentamente le persone della memoria e dell’autonomia, eppure mancano ancora terapie in grado di arrestarla o invertirla. Questo studio esplora alcuni dei più piccoli interruttori di controllo del cervello—brevi molecole di RNA chiamate microRNA—that aiutano a decidere quali proteine le cellule producono. Analizzando tessuto cerebrale di persone affette da Alzheimer, i ricercatori hanno verificato se le variazioni in questi microRNA siano legate a un elemento chiave della malattia: l’accumulo e la diffusione della proteina tau anomala all’interno delle cellule cerebrali.
Esaminare i messaggi in una regione cerebrale vulnerabile
Il team si è concentrato sulla corteccia temporale, una regione importante per linguaggio e memoria fortemente colpita nell’Alzheimer. Dopo il decesso, sono stati raccolti campioni da 36 individui—13 senza Alzheimer e 23 con la malattia—provenienti da due banche cerebrali europee. Gli scienziati hanno estratto RNA da questi tessuti e hanno utilizzato il sequenziamento ad alto rendimento per quantificare centinaia di diversi microRNA. Poiché il tessuto cerebrale si degrada dopo la morte, hanno controllato con attenzione la qualità dell’RNA e selezionato 19 campioni con integrità accettabile per l’analisi più dettagliata, quindi hanno usato tutti i 36 campioni per confermare i risultati principali.
Scoprire una firma di microRNA dell’Alzheimer
Tra 449 microRNA rilevati, 13 si sono distinti come costantemente alterati nella corteccia temporale degli Alzheimer. Otto risultavano ridotti e cinque aumentati rispetto ai cervelli di controllo. Diversi segnali più forti coinvolgevano microRNA già sospettati di avere un ruolo nell’Alzheimer: miR-129-5p, miR-132-3p e miR-146b-5p erano tutti più bassi, mentre miR-151a-5p era aumentato. Queste molecole sono abbondanti nel cervello e sono note per regolare reti geniche coinvolte nella salute neuronale. Utilizzando una seconda tecnica più mirata (RT-qPCR), gli autori hanno convalidato che gli stessi microRNA cambiavano nella stessa direzione, anche includendo campioni di qualità inferiore, rafforzando la fiducia che il quadro sia reale.
Collegare i piccoli interruttori all’aggravarsi degli ammassi di tau
La gravità dell’Alzheimer nel cervello viene spesso classificata con lo stadio di Braak, che riflette fino a che punto gli ammassi di tau si sono diffusi nelle diverse regioni. I ricercatori hanno trovato che i livelli di miR-129-5p, miR-132-3p e miR-146b-5p diminuivano gradualmente con l’aumentare dello stadio di Braak, mentre miR-151a-5p tendeva ad aumentare. Hanno inoltre misurato direttamente nella stessa serie di campioni una forma altamente fosforilata e incline a formare grovigli della proteina tau. I cervelli con maggiore quantità di questa tau anomala mostravano lo stesso schema: meno miR-129-5p, miR-132-3p e miR-146b-5p, e più miR-151a-5p. In altre parole, le variazioni dei microRNA seguivano sia la stadiazione microscopica sia i segni biochimici della patologia della tau, suggerendo che sono strettamente connessi al processo patologico piuttosto che meri spettatori casuali.
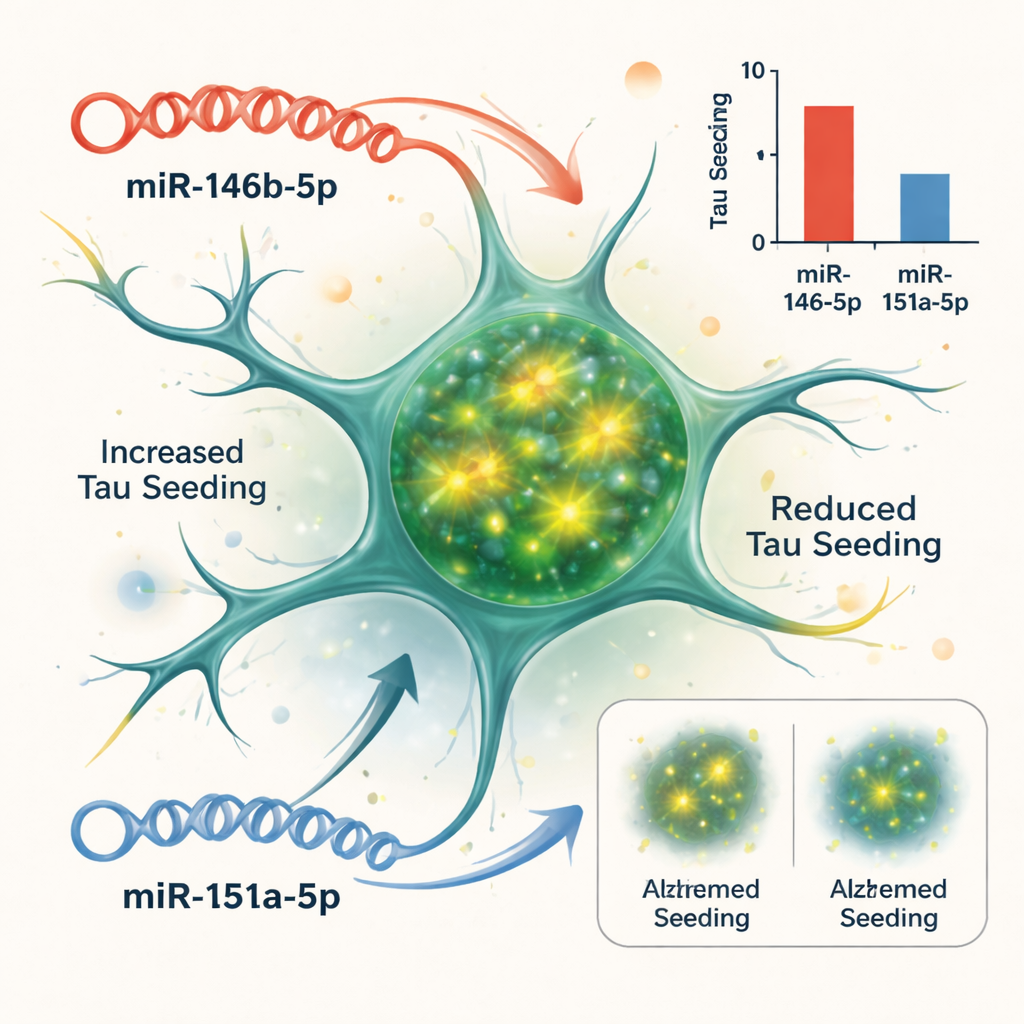
Testare causa ed effetto in un modello cellulare
La correlazione non prova che i microRNA guidino la malattia, così il team ha usato un sistema cellulare che segnala quanto facilmente la tau aggregata può “innescare” nuovi ammassi. Hanno impiegato cellule biosensori ingegnerizzate per illuminarsi quando si formano fibre di tau al loro interno. Aggiungendo materiale ricco di tau proveniente da cervelli affetti da Alzheimer, le cellule hanno prodotto un forte segnale fluorescente. Potenziando o bloccando specifici microRNA in queste cellule, gli scienziati hanno potuto vedere quali ne modificavano l’innesco della tau. Due si sono distinti: aumentare miR-146b-5p ha peggiorato l’innesco della tau, mentre bloccarlo lo ha ridotto; al contrario, aumentare miR-151a-5p ha attenuato l’innesco della tau, mentre inibirlo lo ha reso più robusto. Altri microRNA testati hanno mostrato scarso effetto in questo saggio.
Cosa potrebbe significare per diagnosi e terapie future
Per comprendere cosa potrebbero fare questi microRNA, gli autori hanno usato strumenti computazionali per mappare i loro bersagli genici predetti su vie biologiche note. I microRNA downregolati—specialmente miR-129-5p, miR-132-3p e miR-146b-5p—erano collegati a reti coinvolte nella sopravvivenza dei neuroni, nella trasmissione chimica sinaptica e in percorsi associati all’Alzheimer. Ciò suggerisce che la perdita del loro normale effetto “frenante” potrebbe compromettere contemporaneamente più sistemi protettivi, mentre l’aumento di miR-151a-5p potrebbe rappresentare un tentativo tardivo e parziale del cervello di contrastare l’aggregazione della tau. Sebbene questo lavoro si basi su tessuto post-mortem e modelli cellulari semplificati, rafforza l’idea che microRNA specifici riflettano e modulino la patologia della tau. A lungo termine, misurare queste molecole nel liquido cerebrospinale o nel sangue potrebbe aiutare a seguire la progressione della malattia, e regolare con precisione i loro livelli nel cervello potrebbe offrire una nuova strada per rallentare o prevenire la diffusione della tau tossica.
Citazione: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Parole chiave: Malattia di Alzheimer, microRNA, patologia della tau, corteccia temporale, neurodegenerazione