Clear Sky Science · it
Il blocco mirato dello splicing genico può disgregolare i microRNA primari incorporati negli introni
Messaggi nascosti all’interno dei nostri geni
Molte nuove terapie geniche agiscono modificando i messaggi di RNA delle cellule, ma quegli RNA spesso contengono «note a margine» che gli scienziati stanno solo cominciando a comprendere. Questo studio mostra che farmaci progettati per correggere lo splicing difettoso possono inavvertitamente aumentare piccole RNA regolatorie sepolte negli introni — le sequenze non codificanti tra i segmenti del gene — con effetti sorprendenti sul wiring cerebrale e sullo sviluppo.
Terapie geniche che riscrivono l’RNA
Gli oligonucleotidi antisenso, o ASO, sono brevi frammenti sintetici di materiale genetico che si legano all’RNA e ne modificano la lettura o l’elaborazione. Diversi ASO sono già in sperimentazione o in uso per malattie genetiche rare, soprattutto quelle dovute a errori nello splicing dell’RNA — il passaggio che cucisce insieme i segmenti codificanti di un gene. La maggior parte dei test di sicurezza valuta se un ASO ristabilisce la proteina corretta ed evita effetti collaterali evidenti. Ma molti geni contengono anche RNA non codificanti, inclusi i microRNA, all’interno dei loro introni. Queste piccole molecole possono modulare fortemente l’attività genica, e fino a metà dei microRNA noti nei vertebrati deriva da introni. Lo studio si domanda: che ne è di questi microRNA incorporati quando forziamo modifiche dello splicing con ASO?
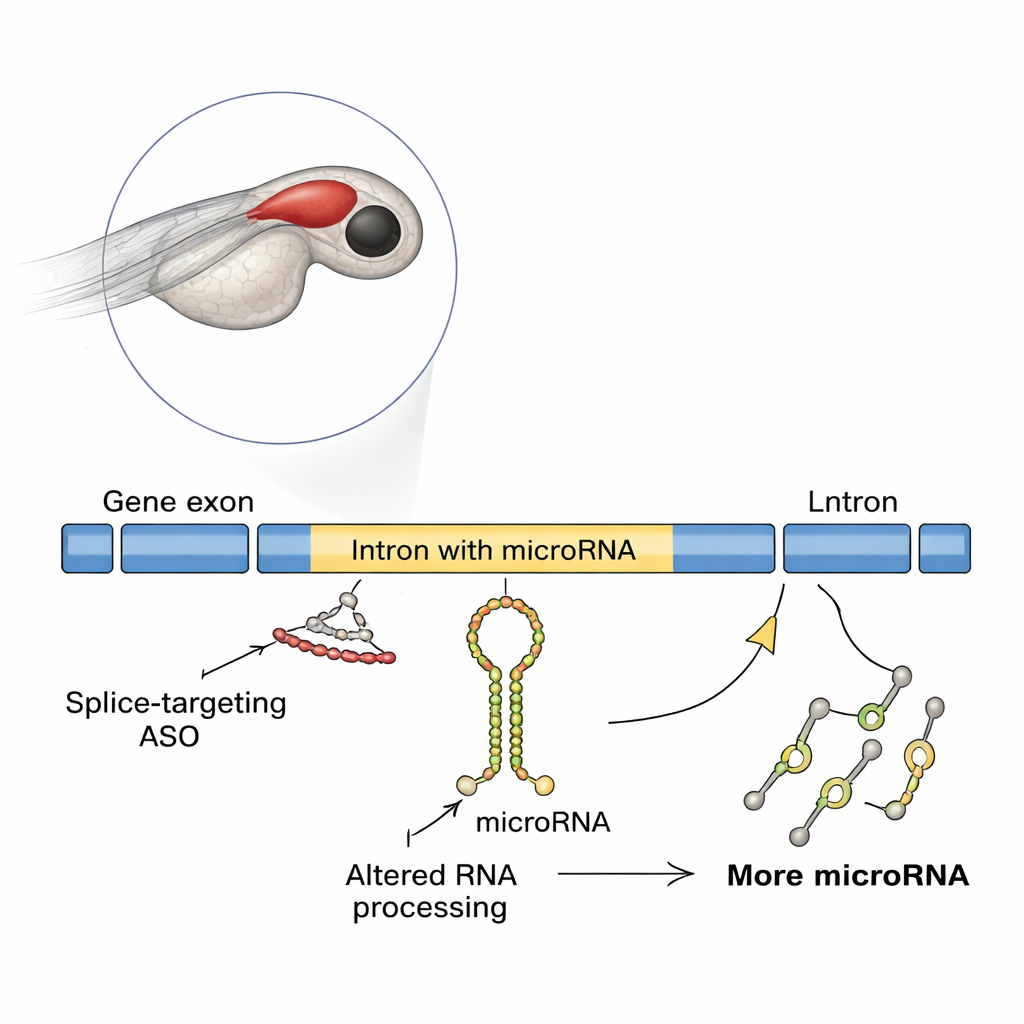
Un effetto sorprendente nei cervelli dei pesci in sviluppo
I ricercatori hanno usato la zebrafish, un modello vertebrato popolare i cui embrioni trasparenti rendono facile seguire lo sviluppo cerebrale. Si sono concentrati su un gene chiamato slit3, che guida le fibre nervose e contiene un microRNA chiamato mir-218a-1 all’interno di uno dei suoi introni. Quando il gruppo ha bloccato l’inizio della traduzione di slit3, lo sviluppo degli assoni secretori di ormoni in ipofisi sembrava normale. Ma quando hanno utilizzato un diverso ASO che bloccava lo splicing in un sito di splicing specifico di slit3, gli assoni diretti all’ipofisi posteriore risultavano drasticamente ridotti, pur non cambiando il numero di neuroni produttrici di ossitocina. Test molecolari hanno mostrato che questo ASO che blocca lo splicing causava il mantenimento dell’introne nell’RNA del gene, aumentandone inaspettatamente i livelli di trascritto di slit3, il suo introne lungo e il trascritto primario intronico di mir-218a-1.
È il microRNA, non la perdita di proteina, a causare i difetti
Per chiarire la causa del difetto assonale, gli autori hanno confrontato diversi scenari. Bloccare solo il mir-218a-1 maturo non ha modificato i livelli di slit3, e un ASO separato diretto a un diverso sito di splicing vicino al microRNA non ha prodotto difetti assonali né aumentato mir-218a-1. Crucialmente, quando l’ASO che bloccava lo splicing di slit3 è stato combinato con un ASO che neutralizza mir-218a-1, il cablaggio assonale si è in gran parte ripristinato. Allo stesso modo, in zebrafish privi geneticamente di mir-218a-1, lo stesso ASO che blocca lo splicing di slit3 non ha più causato difetti assonali, mentre l’iniezione di un analogo sintetico di mir-218a ha potuto riprodurre il fenotipo nei pesci normali. Questi esperimenti indicano che è l’aumento del microRNA intronico — piuttosto che una proteina Slit3 troncata — il principale fattore alla base del disturbo dello sviluppo.
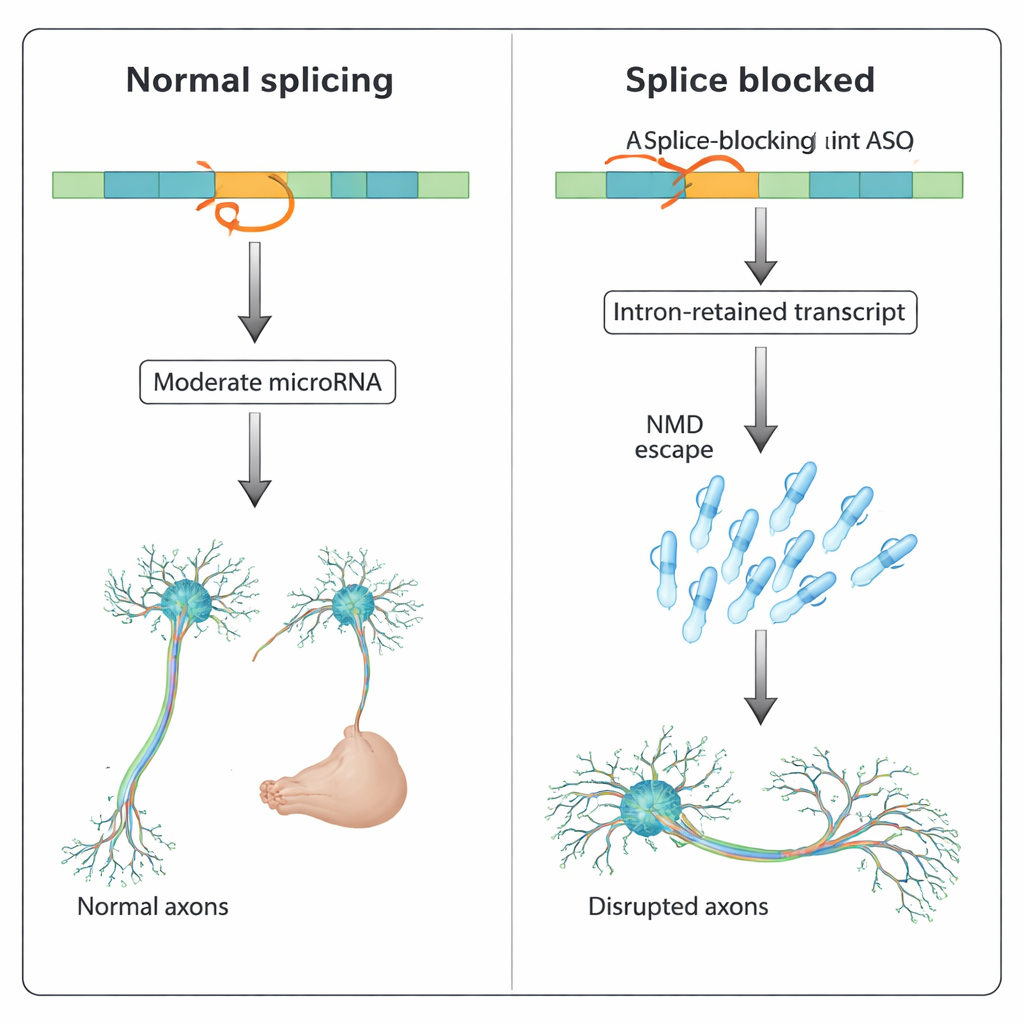
Un quadro più ampio su più geni
Il gruppo si è poi chiesto se questo effetto fosse unico di slit3. Ha esaminato il genoma della zebrafish e ha trovato dozzine di geni codificanti proteine che ospitano microRNA intronici, molti coinvolti nello sviluppo e nella segnalazione. Due di questi geni, pank2 e dnm2a, avevano precedentemente mostrato gravi problemi di sviluppo quando il loro splicing era stato bloccato da ASO, includendo accumulo di liquido cerebrale, gonfiore cardiaco e deformità corporee — problemi che gli knockout genetici degli stessi geni non avevano riprodotto. In questo studio, co-iniettare ASO che bloccavano specificamente i microRNA intronici mir-103 (in pank2) o mir-199-5p (in dnm2a) ha parzialmente risolto questi fenotipi indotti dagli ASO. In alcuni casi, il blocco del microRNA ha anche ripristinato l’espressione del gene ospite, mentre in altri no, suggerendo che un’attività microRNA elevata può essere dannosa anche quando i livelli complessivi cambiano solo modestamente.
Cosa significa per i trattamenti futuri
I risultati rivelano che gli ASO mirati allo splicing possono fare più che causare l’esclusione di esoni o il mantenimento di introni: possono stabilizzare trascritti con introni trattenuti che sfuggono al sistema di controllo qualità cellulare e aumentare i microRNA primari intronici, che poi dis-regolano reti di geni bersaglio. Nei neuroni in sviluppo, un’attività microRNA incontrollata può distorcere la crescita degli assoni e la connettività. Per gli sviluppatori di farmaci, ciò significa che fenotipi insoliti o «off-target» nei test su animali potrebbero non derivare sempre da vie di tossicità generiche come l’attivazione di p53, ma da effetti involontari su RNA intronici nascosti. Confrontare attentamente ASO che bloccano la traduzione e ASO che bloccano lo splicing, e monitorare l’espressione dei microRNA intronici, potrebbe aiutare a individuare questi rischi precocemente e a perfezionare il design degli ASO prima che raggiungano i pazienti.
Citazione: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Parole chiave: oligonucleotidi antisenso, microRNA, splicing dell'RNA, sviluppo della zebrafish, sicurezza della terapia genica