Clear Sky Science · it
Nimbolide migliora la SDRA e la colite ulcerosa interrompendo l’attivazione dell’inflammasoma NLRP3
Perché è importante frenare l’infiammazione fuori controllo
Molte malattie gravi, dalla insufficienza polmonare potenzialmente letale alle dolorose patologie intestinali, non sono causate solo da germi o traumi, ma anche dall’eccessiva reazione del sistema immunitario. Questo studio verifica se un composto naturale chiamato nimbolide, estratto dall’albero del neem, possa agire come un freno mirato su una potente macchina infiammatoria all’interno delle cellule immunitarie, aprendo potenzialmente una strada più sicura per trattare condizioni come la sindrome da distress respiratorio acuto (ARDS) e la colite ulcerosa.
Un allarme problematico all’interno delle cellule immunitarie
Al centro di questa storia c’è un sistema di allarme molecolare chiamato inflammasoma NLRP3. Quando le cellule immunitarie avvertono pericolo — segnali da infezioni, tessuti danneggiati o cristalli — questo complesso può assemblarsi come una struttura modulare composta da tre parti: il sensore NLRP3, l’adattatore ASC e l’enzima Caspasi‑1. Una volta formato, il complesso attiva potenti messaggeri come IL‑1β e IL‑18 e può scatenare una forma infiammatoria di morte cellulare chiamata piroptosi. Sebbene questa risposta aiuti a eliminare le minacce, quando è iperattivata contribuisce a malattie croniche e acute, incluse artrite, complicazioni del diabete, Alzheimer, ARDS e malattie infiammatorie intestinali. Le industrie farmaceutiche hanno cercato di domare NLRP3 con composti sintetici, ma molti candidati hanno fallito a causa di tossicità, effetti collaterali o cattivo comportamento farmacocinetico, lasciando aperta la necessità di inibitori più sicuri e selettivi.
Scoperta di un potente inibitore di origine vegetale
I ricercatori hanno scremato 126 composti naturali per identificare quali bloccassero al meglio il rilascio di IL‑1β da cellule immunitarie di topo. Il nimbolide è emerso come il più promettente, riducendo la secrezione di IL‑1β di oltre l’80% alle dosi testate. Ulteriori esperimenti hanno mostrato che il nimbolide riduce in modo marcato l’attivazione della Caspasi‑1, il rilascio di IL‑1β e la piroptosi in macrofagi derivati dal midollo osseo di topo, con una potenza simile a un farmaco di riferimento chiamato MCC950. Importante, il nimbolide non ha attenuato il rilascio di altri mediatori immunitari come IL‑6, suggerendo che agisce in modo mirato piuttosto che spegnere l’immunità in modo generale. Testato contro diversi stimoli che attivano NLRP3 — come ATP, nigericina, cristalli di allume e imiquimod — il nimbolide ha costantemente ridotto l’attività dell’inflammasoma, anche in cellule umane THP‑1. Al contrario, non ha bloccato due inflammasomi correlati, AIM2 e NLRC4, evidenziando la sua specificità per NLRP3.
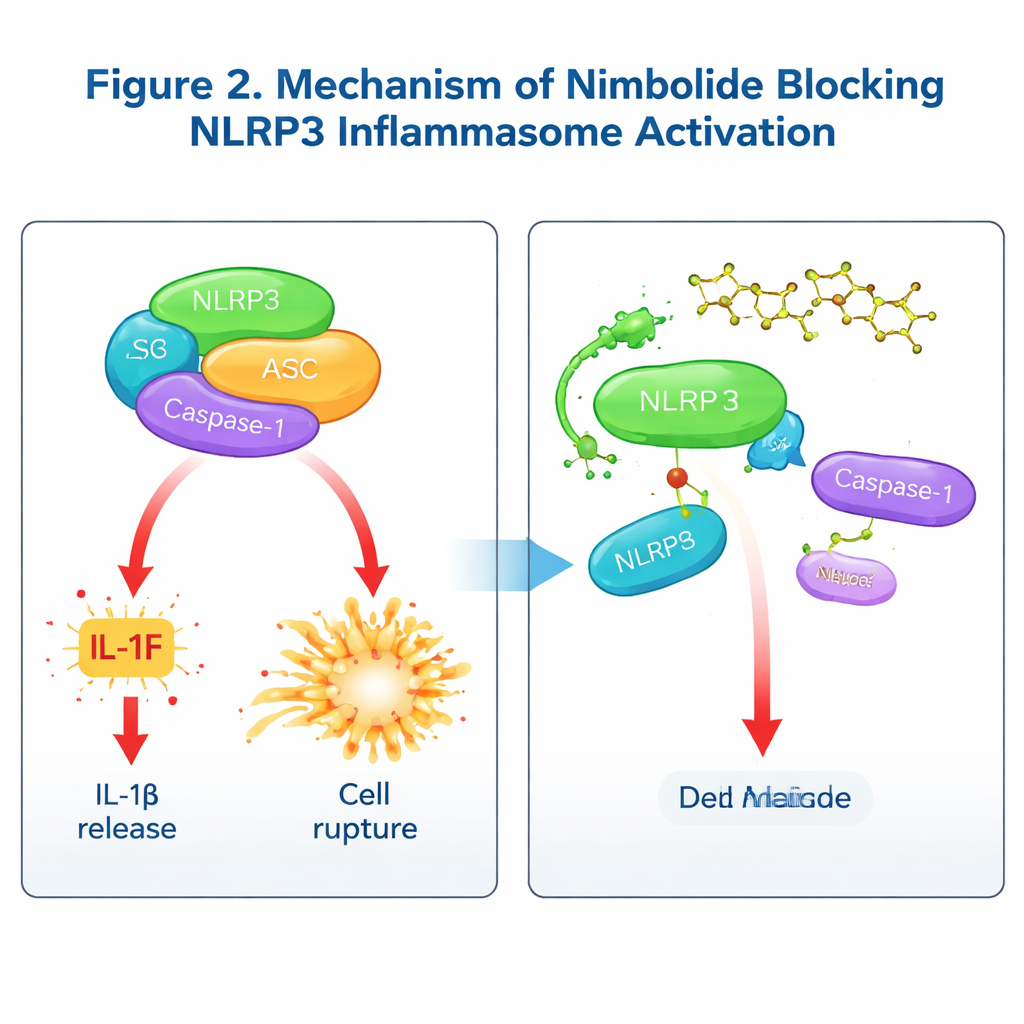
Come il nimbolide blocca la macchina infiammatoria
Per capire il meccanismo d’azione, il gruppo ha indagato se il nimbolide interferisse con le prime fasi di “priming” controllate dalla via NF‑κB, o con le fasi successive in cui l’inflammasoma si assembla fisicamente. Un trattamento a breve termine, somministrato dopo il priming, non ha alterato i segnali di priming né l’espressione genica chiave, ma ha comunque ridotto IL‑1β e l’attivazione della Caspasi‑1, indicando che il nimbolide agisce principalmente sulla fase di assemblaggio. Test biochimici dettagliati hanno rivelato che il nimbolide non modifica il flusso di potassio o calcio, il danneggiamento mitocondriale né l’interazione di NLRP3 con la proteina ausiliaria NEK7. Agisce invece interrompendo l’interazione cruciale tra NLRP3 e ASC, riducendo il raggruppamento di ASC in speck e impedendo a NLRP3 di formare oligomeri di ordine superiore. Tramite saggi di legame e modellazione molecolare, gli autori hanno mostrato che il nimbolide si lega direttamente alla regione NACHT di NLRP3 in un amminoacido specifico, la lisina 565. Quando questo sito è stato mutato, il nimbolide non è stato più in grado di proteggere NLRP3 dalla degradazione né di rompere il suo legame con ASC, confermando Lys565 come punto di ancoraggio chiave. Degno di nota, mentre altri farmaci spesso prendono di mira l’attività ATPasica di NLRP3, il nimbolide blocca l’assemblaggio senza alterare l’uso di ATP, offrendo un meccanismo d’azione distinto.
Testare il nimbolide nelle malattie polmonari e intestinali
Il gruppo ha quindi verificato se questo effetto molecolare si traducesse in protezione nei modelli di malattia. In topi trattati con una tossina batterica per indurre ARDS, la somministrazione di nimbolide prima dell’insulto ha ridotto il danno tissutale polmonare, l’accumulo di liquidi e la perdita di proteine negli spazi aerei. Si è osservata una minore infiltrazione di cellule immunitarie nei polmoni e livelli più bassi di IL‑1β sia nel tessuto polmonare che nel sangue. Benefici simili sono emersi in un modello in cui la tossina è stata somministrata direttamente nelle vie aeree. In un modello separato di colite ulcerosa, in cui i topi assumevano un agente chimico che danneggia il colon, il nimbolide ha limitato la perdita di peso, migliorato la consistenza delle feci e i punteggi di sanguinamento, preservato la lunghezza del colon e ridotto i segni microscopici di infiammazione ed erosione tissutale, abbassando contestualmente i livelli di IL‑1β nel colon. Crucialmente, in topi geneticamente privi di NLRP3 la malattia era già attenuata e il nimbolide non ha apportato benefici aggiuntivi, sottolineando che i suoi effetti protettivi dipendono dall’inibizione di NLRP3.
Cosa potrebbe significare per i trattamenti futuri
Per i non specialisti, la lezione principale è che il nimbolide funziona come un freno intelligente su uno degli interruttori infiammatori più potenti dell’organismo. Legandosi a un sito preciso su NLRP3 e impedendo all’inflammasoma di assemblarsi, attenua l’infiammazione eccessiva sia nei polmoni sia nell’intestino senza sopprimere ampiamente le difese immunitarie. Sebbene il nimbolide richiederà miglioramenti in aspetti come stabilità e somministrazione prima di poter diventare un medicinale, questo lavoro lo colloca come un promettente punto di partenza — e come modello — per progettare farmaci di nuova generazione contro le malattie guidate da NLRP3, come ARDS e colite ulcerosa.
Citazione: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Parole chiave: nimbolide, inflammasoma NLRP3, infiammazione, sindrome da distress respiratorio acuto, colite ulcerosa