Clear Sky Science · it
Studio di associazione su tutto l’epigenoma di interleuchina-6 circolante collega la metilazione del DNA alla salute immunometabolica e infiammatoria
Perché questo è importante per la salute di tutti i giorni
L’infiammazione cronica a basso livello modella in modo silenzioso il nostro rischio per malattie come il diabete di tipo 2, le malattie cardiache e le malattie infiammatorie intestinali. Un attore chiave in questo processo è una proteina di segnalazione nel sangue chiamata interleuchina‑6 (IL‑6). Questo studio pone una domanda fondamentale: come interagisce l’IL‑6 con il nostro epigenoma — i tag chimici sul DNA che aiutano a regolare l’attività genica — e cosa significa questo per la nostra salute a lungo termine?
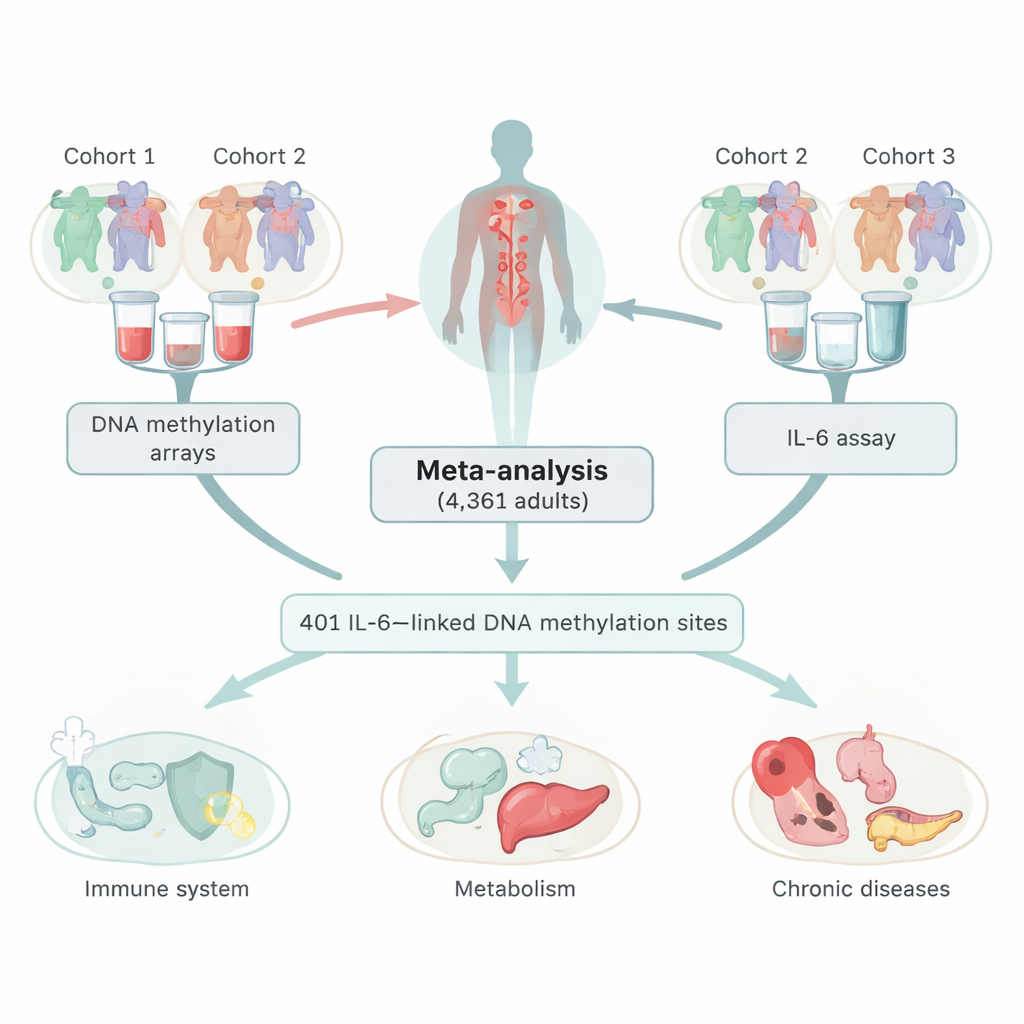
Esaminare i marker chimici sul DNA
I ricercatori hanno combinato dati provenienti da tre ampi studi europei, coprendo 4.361 adulti che hanno fornito campioni di sangue. In questi campioni hanno misurato sia i livelli di IL‑6 sia la metilazione del DNA, un comune marcatore chimico sul DNA che può aumentare o ridurre l’espressione genica senza modificare il codice genetico. Scansionando oltre 400.000 siti nel genoma, hanno identificato 401 posizioni in cui i livelli di metilazione erano correlati alla quantità di IL‑6 circolante nel sangue. La maggior parte di questi siti mostrava un andamento inverso: livelli maggiori di IL‑6 correvano paralleli a una minore metilazione in quei punti. Il team ha verificato attentamente che questi legami non fossero semplici effetti collaterali del fumo, di differenze nei tipi cellulari ematici o di un altro marcatore infiammatorio chiamato proteina C‑reattiva (CRP).
Collegare l’infiammazione al metabolismo e alle malattie
Successivamente gli autori hanno chiesto se questi siti di DNA associati all’IL‑6 sovrapponessero segnali visti in altri grandi studi epigenetici. Hanno riscontrato un forte arricchimento per tratti con una componente infiammatoria o metabolica, inclusi indice di massa corporea, lipidi ematici, pressione arteriosa, glicemia, diabete di tipo 2, malattia renale cronica e condizioni psichiatriche e correlate allo stress. Molti degli stessi siti di metilazione erano già stati collegati alla CRP, ma i pattern suggerivano che IL‑6 e CRP portino ciascuna firme epigenetiche in parte distinte. In altre parole, i segni chimici associati all’IL‑6 non sono una semplice copia carbone di quelli legati alla CRP e possono fornire informazioni aggiuntive sullo stato infiammatorio e metabolico di una persona.
Dove nel genoma avviene l’azione
Per capire cosa potrebbero fare questi siti di metilazione, il team li ha mappati su regioni regolatorie note del genoma. Hanno trovato che i siti associati all’IL‑6 erano concentrati in elementi di controllo attivi come gli enhancer — porzioni di DNA che aiutano ad attivare i geni — piuttosto che in regioni silenti. Questi siti si trovavano inoltre vicino a sequenze di legame per fattori di trascrizione che regolano direttamente l’IL‑6 e le risposte allo stress, inclusi NF‑κB, Atf4, CHOP e Nrf2. Combinando i dati di metilazione con grandi dataset di espressione genica, i ricercatori hanno collegato oltre 400 geni ai siti correlati all’IL‑6. Molti di questi geni sono al centro del controllo immunitario e metabolico, tra cui SOCS3, IL6R, AIM2, IFI16, MTOR e RORC, e partecipano a vie che guidano l’attivazione e l’uso dell’energia in un tipo specializzato di cellula T (cellule Th17) implicata nelle malattie infiammatorie croniche.
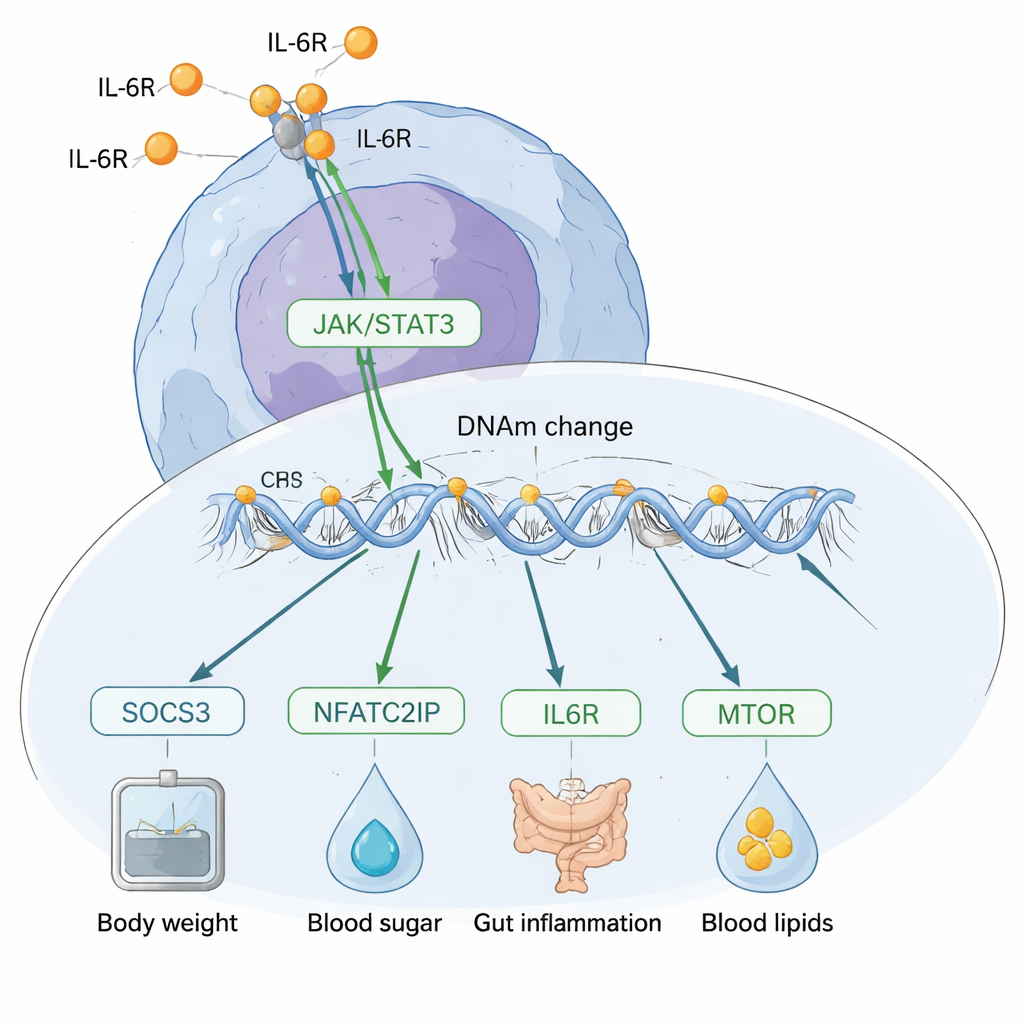
In che direzione corre la causa ed effetto?
Una sfida importante è capire se la metilazione del DNA stia causando cambiamenti nell’IL‑6, oppure se l’IL‑6 stia rimodellando la metilazione. Il team ha usato diversi approcci genetici per sondare questa direzione. A livello genomico, le loro analisi di “triangolazione” supportavano un modello in cui l’IL‑6 per lo più guida cambiamenti nella metilazione del DNA, piuttosto che il contrario. Hanno poi esaminato più in dettaglio siti specifici e hanno trovato che i cambiamenti di metilazione vicino al gene SOCS3 sembrano mediare l’impatto dell’IL‑6 su fattori di rischio come peso corporeo, colesterolo, livelli di CRP e malattia infiammatoria intestinale. Al contrario, un sito di rilievo vicino a un regolatore genico chiamato NFATC2IP mostrava segnali di influenzare la produzione di IL‑6 stessa e sembrava anche influenzare più condizioni tra cui indice di massa corporea, diabete di tipo 2 e infiammazione intestinale.
Cosa significa per la prevenzione e il trattamento futuri
Per un lettore non specialista, il messaggio centrale è che l’IL‑6 e i segni epigenetici sul DNA sono strettamente intrecciati in modi che riguardano molte malattie comuni. Nella maggior parte dei casi, l’IL‑6 sembra lasciare un “impronta” chimica sul genoma, in particolare nelle cellule immunitarie, marcando e possibilmente stabilizzando stati pro‑infiammatori. In alcuni siti chiave, tuttavia, la metilazione può contribuire a determinare quanto IL‑6 venga prodotto e quanto intensamente rispondano le vie immunitarie. Questi risultati indicano i profili di metilazione del DNA come promettenti indicatori ematici dello stato infiammatorio e metabolico, e suggeriscono che modifiche epigenetiche mirate con attenzione — in particolare attorno a geni come SOCS3 e NFATC2IP — potrebbero un giorno affiancare i farmaci che bloccano l’IL‑6 nella prevenzione o nel trattamento delle malattie croniche.
Citazione: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Parole chiave: interleuchina-6, metilazione del DNA, infiammazione, malattie metaboliche, epigenetica