Clear Sky Science · it
MAT2A aumenta la trascrizione di PARN tramite SRF per accelerare la glicolisi e guidare la progressione maligna nell’osteosarcoma
Perché questo studio sul cancro osseo è importante
L’osteosarcoma è il tumore osseo più comune nei bambini e negli adolescenti, e i trattamenti sono rimasti sostanzialmente invariati per decenni. Molti giovani pazienti affrontano ancora prognosi sfavorevoli, soprattutto se il tumore metastatizza o è resistente alla chemioterapia. Questo studio mette in luce una proteina «interruttore master» chiamata MAT2A che aiuta le cellule di osteosarcoma a proliferare, riorganizzare il loro metabolismo energetico e formare tumori aggressivi — e mostra che un farmaco mirato a MAT2A può rallentare o ridurre questi tumori in modelli di laboratorio.
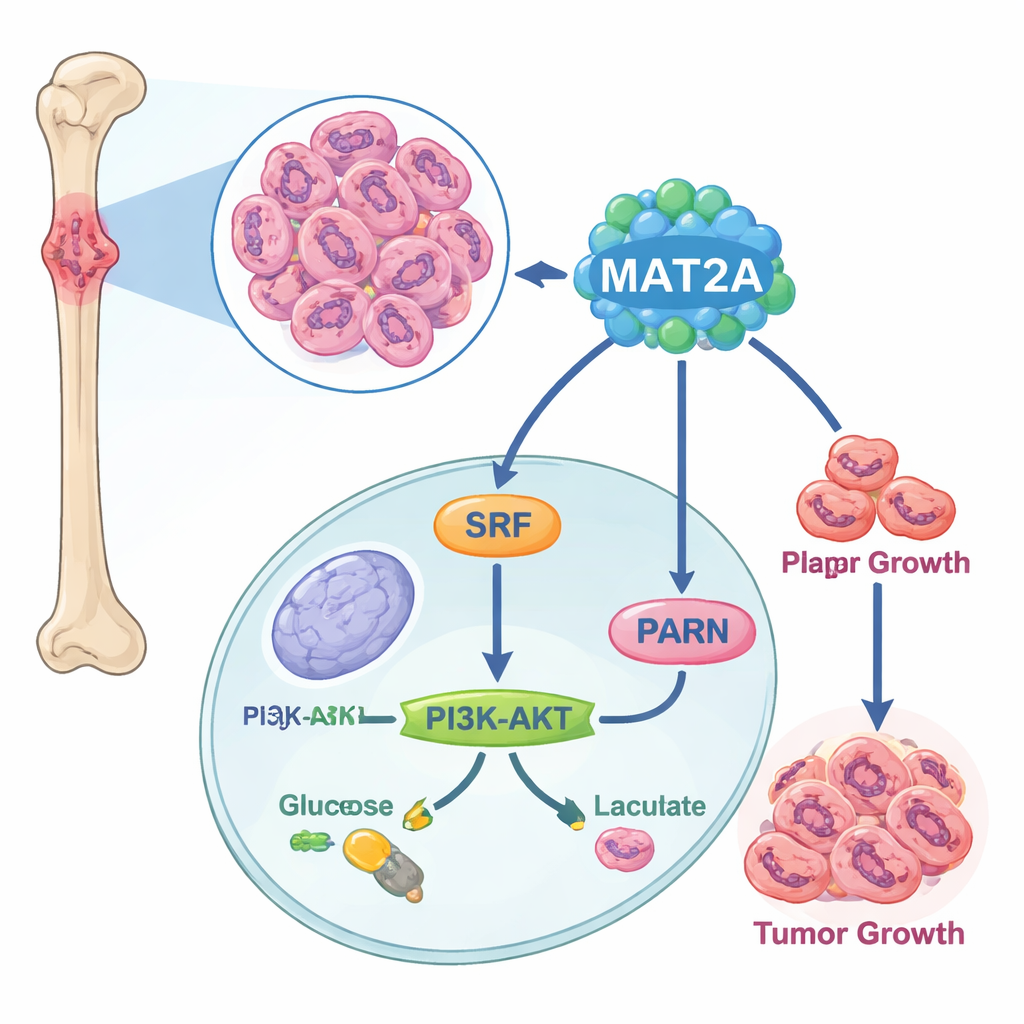
Un motore nascosto all’interno delle cellule tumorali
I ricercatori hanno iniziato confrontando campioni di tumore osseo con tessuto osseo normale a livello di singola cellula. Hanno scoperto che il tessuto di osteosarcoma contiene più cellule con funzione tumorale e meno cellule immunitarie, e che un gene in particolare — MAT2A — risultava insolitatamente attivo nelle cellule tumorali. Analisi di banche dati pubbliche sul cancro e di linee cellulari coltivate in laboratorio hanno confermato che i livelli di MAT2A erano molto più alti nell’osteosarcoma rispetto alle cellule ossee sane, e che i pazienti con maggiore espressione di MAT2A tendevano ad avere malattia più avanzata e diffusione ai linfonodi. Questo ha posto MAT2A al centro dell’attenzione come potenziale fattore guida della malattia piuttosto che come semplice spettatore.
Abbassare MAT2A rallenta la crescita tumorale
Per verificare l’importanza reale di MAT2A nel comportamento tumorale, il team ha utilizzato strumenti genetici per ridurre i livelli di MAT2A in linee cellulari di osteosarcoma. Quando MAT2A veniva silenziata, le cellule tumorali si dividevano più lentamente e mostravano una maggiore tendenza ad andare incontro ad apoptosi programmata. In topi impiantati con queste cellule modificate, i tumori crescevano molto più lentamente e risultavano significativamente più piccoli, pur senza variazioni rilevanti nel peso corporeo degli animali. Questi esperimenti hanno dimostrato che le cellule di osteosarcoma dipendono fortemente da MAT2A sia per la sopravvivenza sia per la capacità di formare tumori.
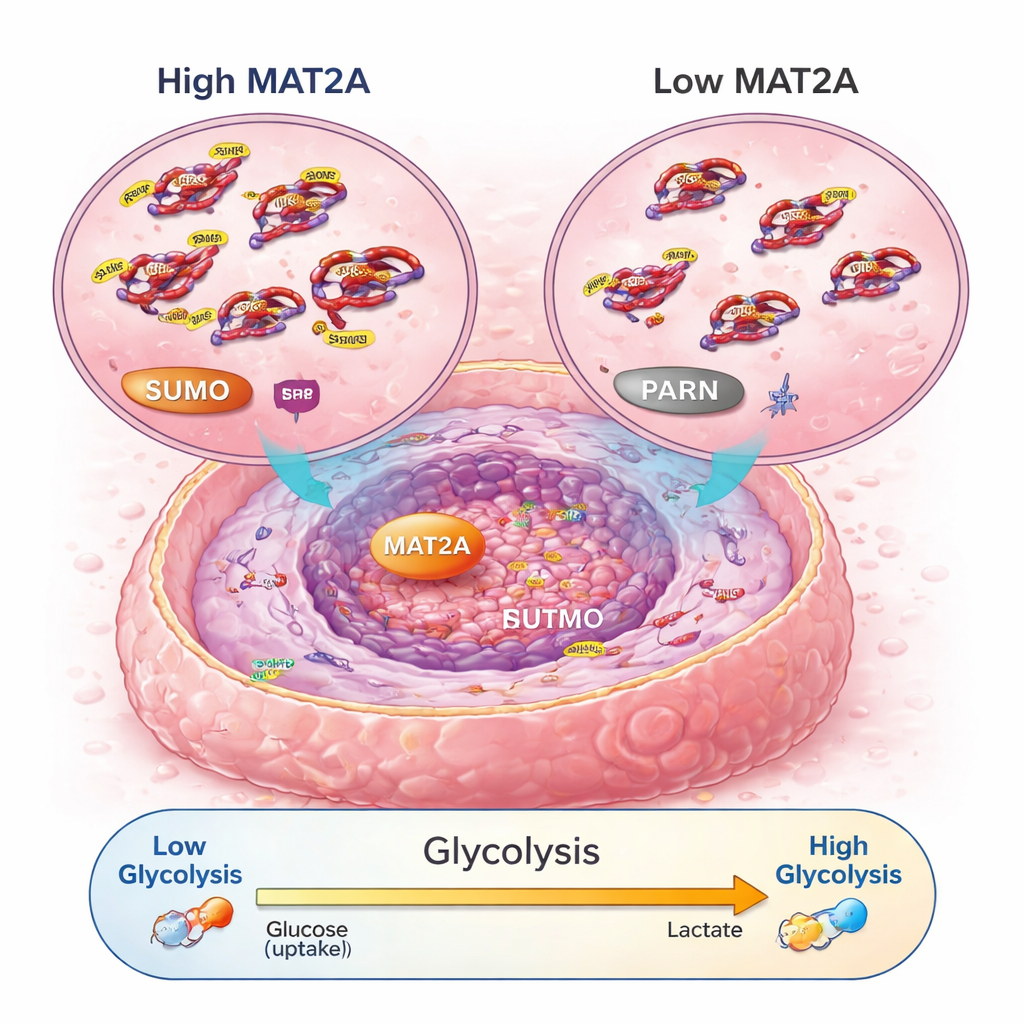
Una catena di segnali che aumenta l’uso di carburante cellulare
Approfondendo i meccanismi, gli scienziati hanno scoperto che MAT2A fa più del suo ruolo metabolico abituale. Nel nucleo si lega a un fattore di trascrizione chiamato SRF, contribuendo a mantenere SRF stabile e attivo promuovendo un marchio chimico noto come SUMO. A sua volta, SRF attiva il gene PARN, che poi stimola la nota via PI3K–AKT e aumenta i meccanismi della glicolisi aerobica — un modo rapido ma inefficiente con cui le cellule producono energia, favorito dalle cellule tumorali. Quando MAT2A veniva ridotto, le cellule tumorali producevano meno ATP (la loro moneta energetica), assumevano meno glucosio, generavano meno acido lattico e tornavano verso una respirazione ossidativa più tranquilla. Disgregare PARN o AKT poteva annullare gli effetti pro-crescita e pro-glicolisi di MAT2A, confermando che questa catena — MAT2A verso SRF verso PARN verso PI3K–AKT — funziona come un circuito chiave per energia e crescita nell’osteosarcoma.
Un ruolo non tradizionale e un bersaglio farmacologico
Colpisce che una versione di MAT2A priva della sua normale attività enzimatica continuasse a sostenere la stabilità di SRF e l’attivazione di PARN, il che significa che questo ruolo promotore del cancro non dipende dalla sua reazione chimica abituale. Invece, MAT2A agisce più come uno impalcatura che organizza altre proteine. Questo ha implicazioni pratiche: i farmaci non devono necessariamente bloccare il suo sito catalitico per indebolire i tumori. I ricercatori hanno testato un inibitore di piccola molecola chiamato FIDAS-5, progettato per colpire MAT2A, sia in colture cellulari sia in modelli murini. Il trattamento ha ridotto SRF nucleare, abbassato PARN e la segnalazione PI3K–AKT, attenuato la glicolisi, rallentato la crescita cellulare e indotto la morte delle cellule tumorali. Nei topi, FIDAS-5 ha ridotto o rallentato i tumori senza perdita di peso evidente, suggerendo effetti collaterali tollerabili in questo contesto.
Cosa significa per i pazienti e le terapie future
Per i non specialisti, il messaggio principale è che le cellule di osteosarcoma dipendono da MAT2A per mantenere i loro programmi di crescita e i motori di consumo di zucchero al massimo regime. Stabilizzando proteine di controllo chiave e potenziando una catena di segnali, MAT2A aiuta i tumori a crescere più rapidamente e a diventare più aggressivi. Bloccare questa proteina — sia con metodi basati sul gene sia con un farmaco come FIDAS-5 — interrompe questo supporto, costringendo le cellule tumorali a rallentare, a consumare energia meno frenetica e infine a morire. Sebbene resti molto lavoro prima che tali terapie arrivino in clinica, questo studio pone MAT2A come un nuovo obiettivo promettente nella lotta contro il cancro osseo, aprendo una possibile strada verso terapie più precise e meno tossiche per i pazienti giovani.
Citazione: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Parole chiave: osteosarcoma, MAT2A, metabolismo del cancro, via PI3K AKT, terapia mirata