Clear Sky Science · it
Analisi computazionale dell'eterogeneità degli epitopi nelle immunomarcature da serie di diluizione degli anticorpi
Perché conta la qualità della colorazione con anticorpi
Dal tracciamento delle cellule tumorali alla diagnosi delle infezioni, la biologia moderna fa ampio uso di anticorpi che «illuminano» molecole specifiche all'interno delle cellule. Eppure molti laboratori convivono con un problema fastidioso: colorazioni troppo deboli, troppo rumorose o semplicemente fuorvianti. Questo articolo presenta un metodo pratico, basato su calcolo, per ricavare più informazioni da una routine di serie di diluizione degli anticorpi, aiutando i ricercatori a ottimizzare la colorazione per immagini più pulite, misure più affidabili e persino nuovi modi di marcare più bersagli in un singolo canale di colore. 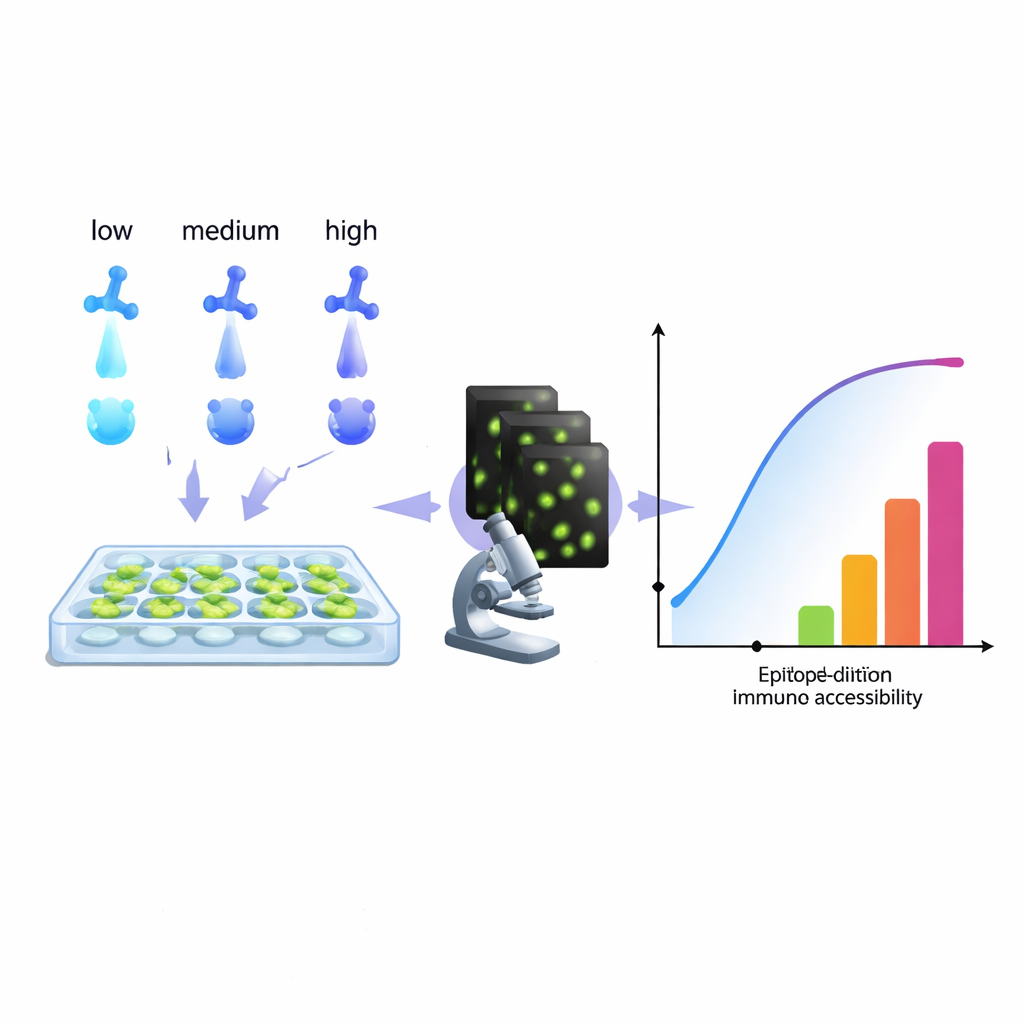
Come gli scienziati normalmente tarano le colorazioni con anticorpi
Quando i ricercatori impostano un esperimento di immunomarcatura, in genere stimano una concentrazione dell'anticorpo dal datasheet, provano alcune diluizioni e scelgono quella che «sembra buona». Dietro le quinte, però, innumerevoli fattori minuti—la conformazione proteica, l'affollamento all'interno delle cellule, il pH e la capacità dell'anticorpo di inserirsi—decidono se un anticorpo resta legato o viene lavato via. Gli strumenti tradizionali che misurano il legame degli anticorpi, come la risonanza plasmonica di superficie, funzionano meglio con proteine purificate su superfici artificiali, non su cellule o tessuti densamente impacchettati. Ciò significa che i valori forniti possono non corrispondere al vero sistema biologico in cui l'anticorpo viene usato. Di conseguenza, i laboratori possono inconsapevolmente scegliere concentrazioni che aumentano un fondo sfocato o nascondono bersagli importanti ma meno accessibili.
Trasformare semplici serie di diluizione in «mappe di accessibilità»
Gli autori propongono un approccio diverso: trattare una serie standard di diluizione degli anticorpi come un set di dati ricco e adattarla con un modello che rifletta ciò che il microscopio vede realmente—anticorpi che restano legati anche dopo ripetuti lavaggi. Analizzando come il segnale cresce al variare della concentrazione, il loro algoritmo ricostruisce un «istogramma di accessibilità». Invece di cercare di isolare costanti chimiche di legame pure, questo istogramma raggruppa i siti bersaglio in classi tecniche di «epitopo» in base alla facilità con cui si colorano nelle condizioni reali. Un singolo epitopo biologico può comparire in più classi se, per esempio, è facile da raggiungere in una regione della cellula e più difficile in una zona affollata. Fondamentale, questo metodo lavora direttamente con il segnale del microscopio, senza necessità di proteine purificate o hardware aggiuntivo, quindi qualsiasi laboratorio in grado di eseguire una serie di diluizioni e quantificare la fluorescenza può, in principio, costruire tali istogrammi. 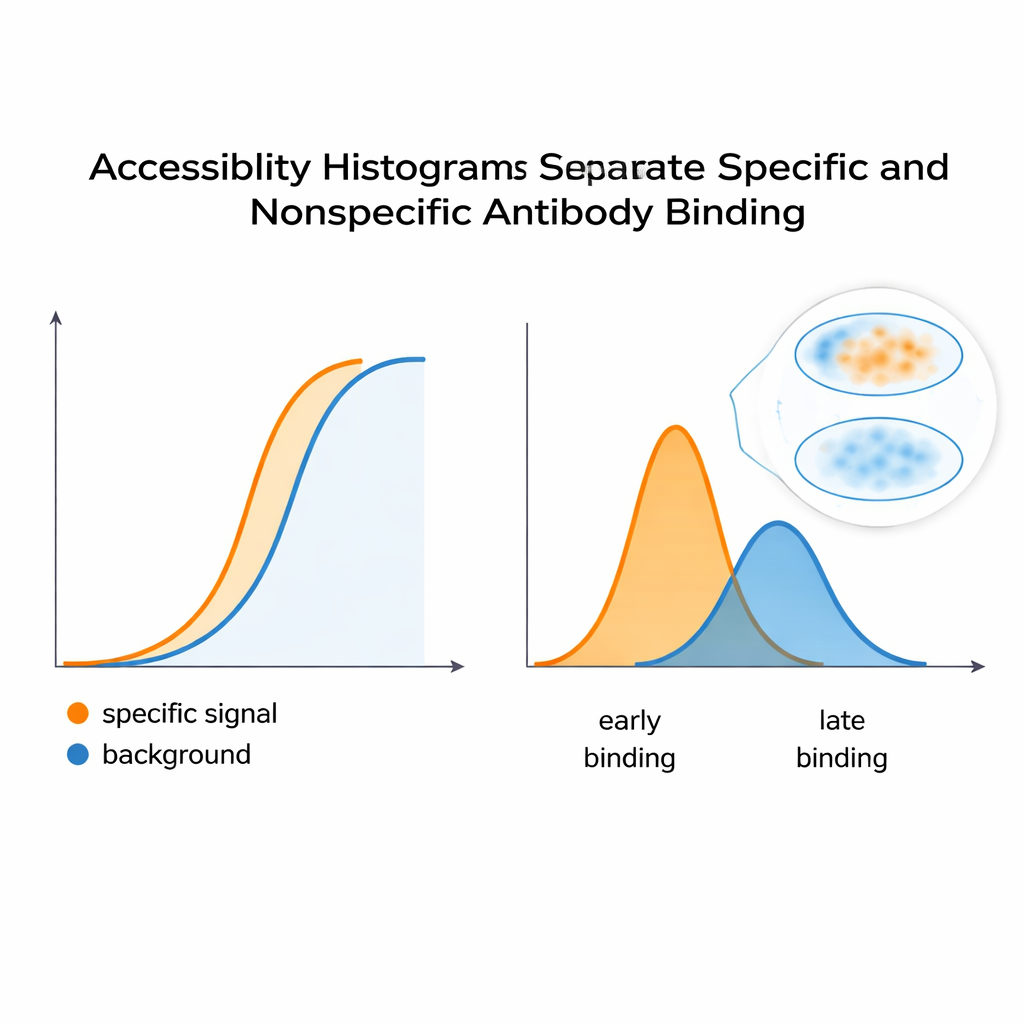
Separare il segnale reale dal fondo
Per verificare se questi istogrammi catturano davvero il comportamento della colorazione, il gruppo ha costruito un sistema controllato usando cellule HeLa e due anticorpi monoclonali: uno che imita un segnale specifico desiderato e un altro che funge da fondo indesiderato. Quando miscelati, la curva di fluorescenza combinata sembrava una singola risposta liscia—nulla di ovvio suggeriva due contributori distinti. Ma l'analisi computazionale ha suddiviso quella curva in picchi separati nell'istogramma di accessibilità, rivelando almeno due classi di epitopi sottostanti. Una strategia simile applicata a un anticorpo che riconosce un sito sensibile alla forma su una subunità regolatoria della PKA ha mostrato che cambiamenti nella conformazione proteica—indotti da una molecola chiamata cAMP—spostavano la distribuzione di epitopi accessibili. Ciò suggerisce che il metodo può segnalare quando le strutture proteiche si aprono o si chiudono, alterando la facilità con cui gli anticorpi si legano all'interno delle cellule.
Scegliere diluizioni migliori e marcare di più con un solo colore
Poiché ogni picco nell'istogramma di accessibilità contribuisce principalmente in un certo intervallo di concentrazione, gli autori usano questi picchi come guida per scegliere le diluizioni «ottimali». I picchi a bassa accessibilità che emergono solo a livelli molto alti di anticorpo sono probabilmente associati a legami non specifici, mentre i picchi precoci spesso riflettono il bersaglio voluto. Modellando come i singoli picchi costruiscono la curva dose–risposta complessiva, il gruppo può suggerire diluizioni che massimizzano il segnale specifico prima che compaiano i picchi problematici—talvolta molto più diluite rispetto alle raccomandazioni del produttore. Estendono inoltre questa idea in una forma ingegnosa di «multiplexing computazionale». Colorando lo stesso campione fissato ripetutamente con concentrazioni scelte con cura, acquisendo immagini dopo ogni passaggio e sottraendo immagini precedenti da quelle successive, isolano segnali legati a diverse classi di accessibilità, separando di fatto più bersagli all'interno di un singolo canale di fluorescenza.
Cosa significa per il lavoro di laboratorio di tutti i giorni
In termini semplici, questo lavoro trasforma un passaggio di risoluzione dei problemi di routine—eseguire una serie di diluizione degli anticorpi—in uno strumento quantitativo. Gli istogrammi di accessibilità aiutano gli scienziati a individuare complessità nascoste nelle loro colorazioni, scegliere diluizioni che riducono il fondo fuorviante e, in alcuni casi, separare segnali sovrapposti senza bisogno di etichette fluorescenti aggiuntive. Sebbene il modello alla base sia intenzionalmente semplice e non catturi ogni dettaglio molecolare, è progettato per essere facile da usare e sufficientemente robusto per dati reali. Se adottato ampiamente, questo approccio potrebbe rendere le tecniche basate su anticorpi—dall'imaging di base ai saggi diagnostici—più affidabili, più informative e meno basate sul tentativo ed errore.
Citazione: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Parole chiave: colorazione con anticorpi, immunofluorescenza, accessibilità dell'epitopo, risposta alla dose, multiplexing computazionale