Clear Sky Science · it
Progressi strategici per studi strutturali cryo‑EM di piccoli GPCR (<100 kDa)
Perché i piccoli interruttori cellulari sono importanti per la medicina
Gran parte della medicina moderna agisce spostando delicatamente piccoli interruttori presenti nelle membrane cellulari, chiamati recettori accoppiati a proteine G (GPCR). Questi interruttori percepiscono ormoni, odori e farmaci, e circa un terzo di tutti i farmaci approvati agisce su di essi. Per progettare terapie più sicure e intelligenti, gli scienziati hanno bisogno di immagini 3D dettagliate di questi recettori, in particolare nelle loro forme «spente» o inattive, che sono il bersaglio di molti farmaci. Questo articolo spiega come i ricercatori stiano imparando a osservare alcuni dei GPCR più piccoli con la crio‑microscopia elettronica (cryo‑EM), una potente tecnica di imaging che può visualizzare le molecole congelate in uno stato vicino al naturale.
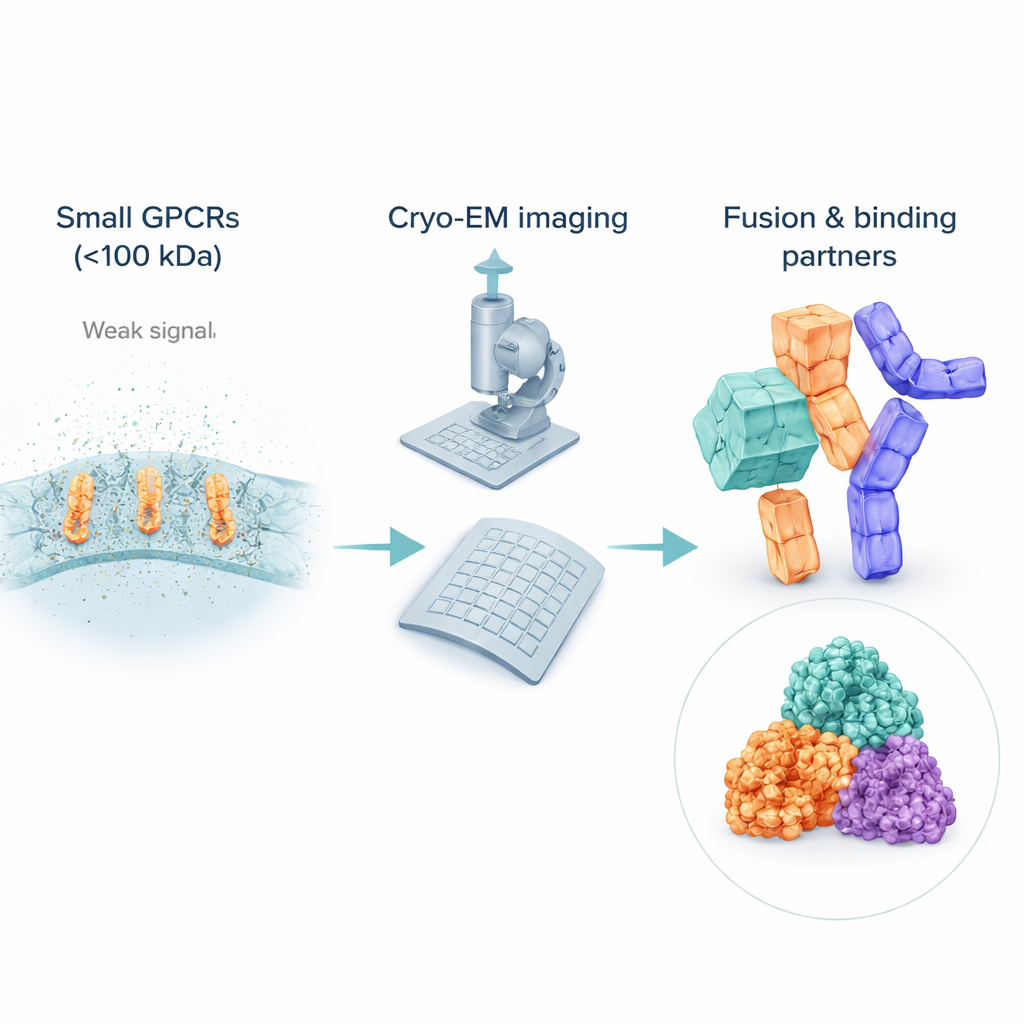
La sfida di vedere recettori molto piccoli
Nonostante la cryo‑EM abbia rivoluzionato la biologia strutturale, incontra ancora difficoltà con molecole piccole e flessibili. Molti GPCR inattivi pesano ben meno di 100 kilodalton, il che li rende difficili da individuare e allineare in immagini rumorose. Per mantenerli solubili, gli scienziati avvolgono questi recettori in bolle di detergente o in mimetici lipidici, che possono in realtà apparire «più grandi» al fascio elettronico rispetto al recettore stesso, sommergendo il segnale della proteina d’interesse. A differenza dei recettori attivi legati a partner voluminosi come le proteine G, i GPCR inattivi spesso mancano di caratteristiche esterne marcate, perciò ai computer è difficile mediare numerose immagini in una vista 3D nitida. Di conseguenza, la maggior parte delle strutture di GPCR inattivi proviene ancora da metodi a raggi X più tradizionali, lasciando una lacuna nella copertura cryo‑EM proprio dove agiscono molti farmaci.
Ingrandire i recettori con aiutanti incorporati
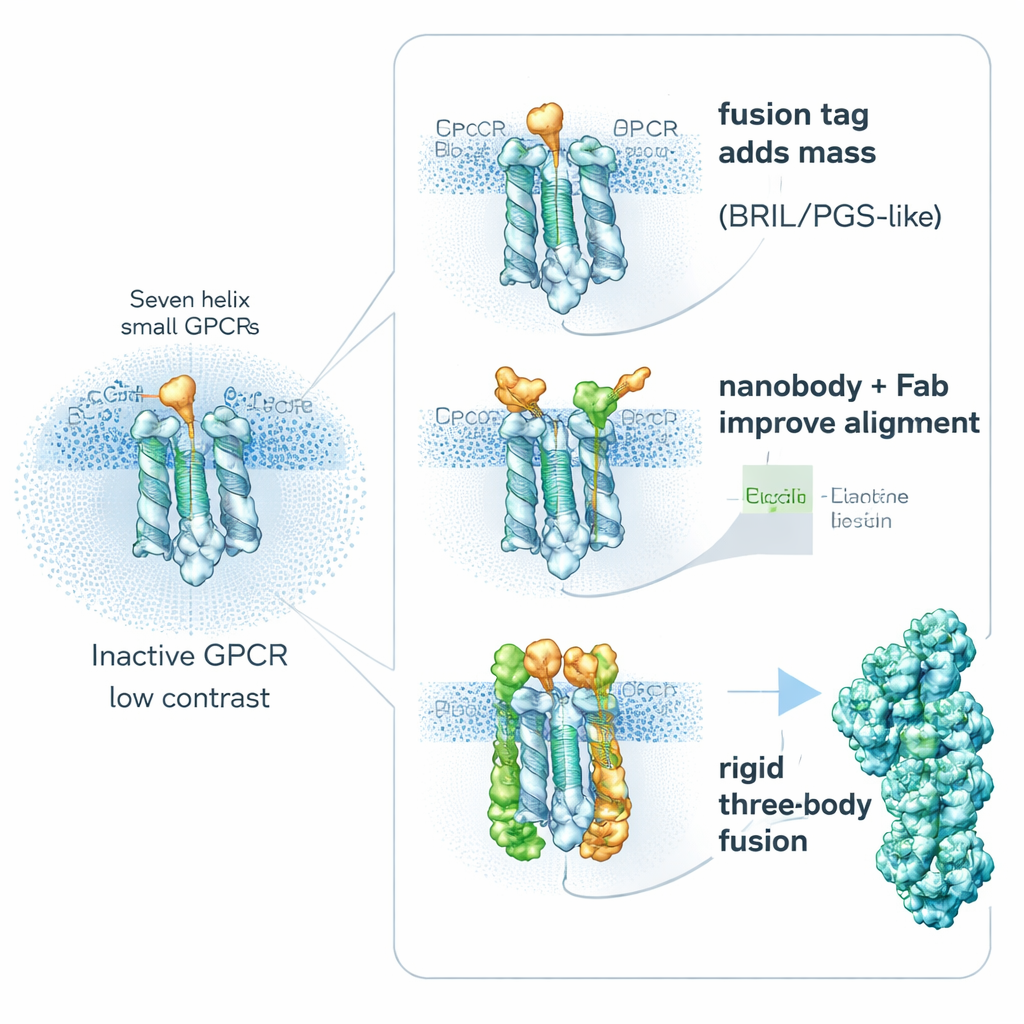
Una strategia chiave è sorprendentemente semplice: rendere il recettore «più pesante» apposta. I ricercatori fondono geneticamente piccole proteine helper stabili su parti flessibili dei GPCR per aumentare la loro dimensione e rigidità, senza bloccare le regioni importanti per il legame dei farmaci. Helper popolari includono BRIL (un bundle di quattro eliche), PGS (un frammento enzimatico termostabile) e una proteina più grande a forma di pinza chiamata calcineurina. Questi partner di fusione sono spesso inseriti in un loop interno mobile che collega due eliche. Rigidificando questa regione, riducono la sfocatura dovuta al movimento molecolare e forniscono forme riconoscibili che aiutano i computer ad allineare le particelle. Studi dimostrano che la posizione e l’orientamento esatti del pezzo di fusione possono fare la differenza: in un recettore, un tag PGS collocato diversamente migliorò la risoluzione da un sfuocato 6 angstrom a un molto più chiaro 3,7 angstrom.
Prendere in prestito anticorpi e leganti progettati come maniglie
Un secondo approccio evita di inserire grandi fusioni nel recettore e invece aggancia dall’esterno «maniglie» ad alta affinità. Piccoli frammenti di anticorpi chiamati nanobody e leganti affini possono essere prodotti per riconoscere GPCR inattivi e aggrapparsi a loop interni flessibili. Un esempio notevole è Nanobody‑6, creato inizialmente come sensore per un recettore oppioide e poi riutilizzato, con lievi modifiche, per stabilizzare diversi altri GPCR nelle loro forme inattive. Poiché si lega in modo decentrato, fornisce a ogni particella un chiaro indizio di orientamento, rendendo l’averaging delle immagini più affidabile. I ricercatori spesso estendono questa idea aggiungendo un secondo livello—un frammento di anticorpo ordinario che riconosce il nanobody stesso—creando un complesso più voluminoso e rigido che si vede con maggiore chiarezza in cryo‑EM. Altri leganti ingegnerizzati, come i DARPin, possono essere usati come distanziatori modulari o come connettori verso gabbie proteiche più grandi, aumentando ulteriormente il segnale da bersagli molto piccoli.
Progettazione intelligente dei campioni e processamento delle immagini potenziato dall’IA
Fondere helper o aggiungere leganti è solo una parte della storia. La recensione sottolinea che buone strutture cominciano con costrutti di recettore attentamente ingegnerizzati: accorciare regioni terminali troppo flosci, introdurre mutazioni stabilizzanti e usare strumenti moderni di predizione strutturale per identificare le parti che possono creare problemi. Sul fronte dell’imaging, trucchi più vecchi come le phase plate, che aumentano il contrasto per particelle deboli, vengono affiancati o persino sostituiti da strumenti basati sull’intelligenza artificiale. Programmi di deep‑learning possono individuare piccole particelle nascoste in micrografie rumorose, e nuovi algoritmi possono classificare le immagini in diverse conformazioni quando i recettori campionano molte forme. Insieme agli helper fiduciali, questi progressi spingono la cryo‑EM a risolvere in modo affidabile proteine di membrana che un tempo erano considerate troppo piccole o troppo dinamiche per essere studiate.
Cosa significa questo per i farmaci del futuro
L’articolo conclude che non esiste un singolo helper «magico» che funzioni per tutti i recettori, ma una cassetta degli attrezzi in crescita di partner di fusione, leganti simili ad anticorpi e metodi guidati dall’IA sta aprendo progressivamente il paesaggio inattivo dei GPCR alla cryo‑EM. Per i non esperti, il punto chiave è che facendo apparire i recettori piccoli più grandi e ordinati al microscopio, gli scienziati possono finalmente ottenere immagini dettagliate delle forme precise a cui molti farmaci preferiscono legarsi. Questi progetti strutturali dovrebbero accelerare la progettazione di medicinali che spengano questi interruttori cellulari in modo più preciso — o ne modulino finemente l’attività — con effetti collaterali ridotti.
Citazione: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Parole chiave: Recettori accoppiati a proteine G, crio‑microscopia elettronica, scoperta di farmaci, biologia strutturale, impalcature nanobody