Clear Sky Science · it
Collegare la tensione molecolare alle trazioni cellulari: un approccio multiscala alla meccanica delle adesioni focali
Come le cellule percepiscono e tirano l’ambiente circostante
Ogni volta che una cellula si muove, si divide o rimodella un tessuto, esercita discreti tratti sul proprio intorno. Questi piccoli tiraggi meccanici sono fondamentali nella guarigione delle ferite, nella diffusione del cancro e nello sviluppo degli organi, ma sono difficili da osservare e ancora più difficili da misurare. Questo studio propone un nuovo modo di guardare a quelle forze su due livelli contemporaneamente: quanto forte una cellula intera tira su un materiale morbido e quanta forza sopportano singole “molle molecolari” all’interno dei siti di ancoraggio della cellula. Collegando queste due prospettive, il lavoro aiuta a spiegare come le cellule percepiscono la rigidità e regolano la loro presa sul mondo circostante.
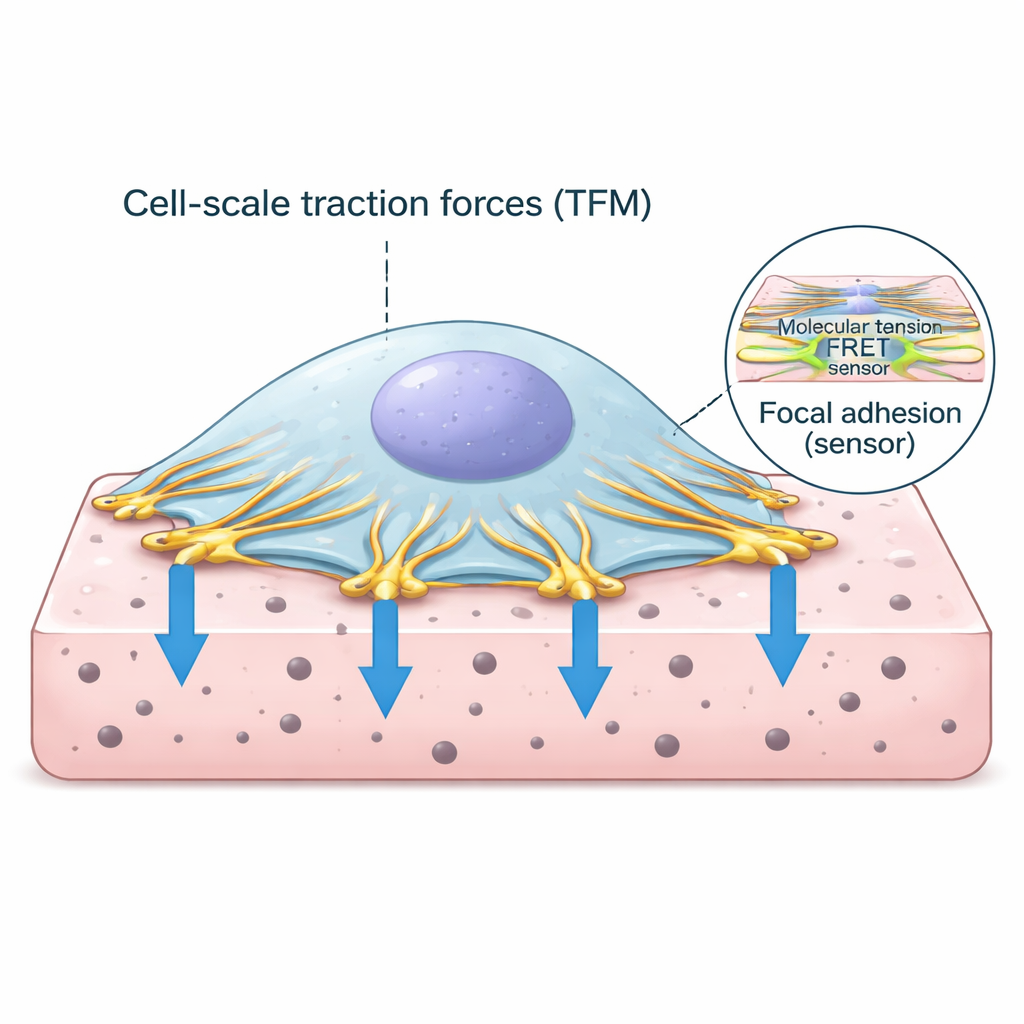
I punti di presa della cellula sul mondo esterno
Le cellule non galleggiano semplicemente nei tessuti; si ancorano tramite punti di contatto specializzati chiamati adesioni focali. In questi punti, l’impalcatura interna di filamenti di actina della cellula si collega a proteine che attraversano la membrana cellulare e si agganciano alla matrice circostante. Una delle proteine chiave in questo complesso di ancoraggio è la vinculina, che si comporta come un collegamento sensibile alla forza. Quando la macchina contrattile della cellula tira sull’actina, la vinculina avverte il carico e contribuisce a rinforzare la connessione. Capire quanta forza passa attraverso questi collegamenti e come ciò si relaziona al tiro complessivo della cellula è centrale per decodificare come i tessuti restano sani o diventano malati.
Due finestre sulla forza cellulare
I ricercatori hanno combinato due tecniche potenti in un unico flusso di lavoro. Innanzitutto, la microscopia delle forze di trazione misura quanto una cellula deforma un substrato morbido e gelatinoso tracciando il movimento di minuscoli granuli fluorescenti nel gel. Da questi spostamenti si può calcolare la distribuzione delle forze di spinta e trazione sotto la cellula. In secondo luogo, una versione di vinculina ingegnerizzata porta un sensore di tensione fluorescente che modifica il suo segnale luminoso quando viene stirato. Usando avanzate tecniche di imaging del tempo di vita del fluoroforo, il gruppo ha convertito questo segnale luminoso in una misura della tensione molecolare sulla vinculina. Hanno progettato idrogel sottili e piani che potevano essere immaginati ad alta risoluzione e scritto software personalizzato per allineare, segmentare e analizzare entrambi i dataset fino ai singoli siti di adesione.
Come la rigidità modifica lo sforzo della cellula
Quando le cellule crebbero su gel morbidi rispetto a gel più rigidi, il loro comportamento complessivo cambiò in modo chiaro. Su substrati più rigidi, le cellule si appiattirono maggiormente ed esercitarono forze di trazione più intense sulla superficie del gel. Allo stesso tempo, la lettura fluorescente dal sensore di vinculina indicò una maggiore tensione molecolare all’interno delle adesioni focali. È interessante notare che le caratteristiche strutturali di base di queste adesioni — come il numero o la dimensione media — non variarono molto tra gel morbidi e rigidi. Ciò che cambiò fu l’organizzazione delle forze. Grandi adesioni orientate radialmente con più vinculina tendevano a sostenere trazioni più elevate, suggerendo che sia la geometria sia la composizione molecolare di questi siti influenzano quanto forte la cellula tira.
Un rapporto complesso tra forze locali e molecolari
Un’osservazione più ravvicinata delle singole adesioni ha rivelato che il legame tra trazione locale e tensione della vinculina non è uniforme. In alcune cellule, le adesioni che generavano trazioni maggiori mostravano anche tensioni maggiori sulla vinculina, implicando che i contatti carichi condividono la forza più direttamente attraverso i loro legami molecolari. In altre cellule apparve il comportamento opposto: regioni di forte trazione erano associate a una minore tensione sulla vinculina, mentre altre adesioni sopportavano più carico molecolare senza produrre grandi spinte verso l’esterno. Molte cellule non mostrarono alcun schema chiaro. Questi comportamenti distinti probabilmente riflettono diversi stati cellulari — come l’espansione attiva, l’adesione stabile o la retrazione — e suggeriscono che le cellule possano ridistribuire le forze attraverso la loro rete di adesioni in modi multipli.
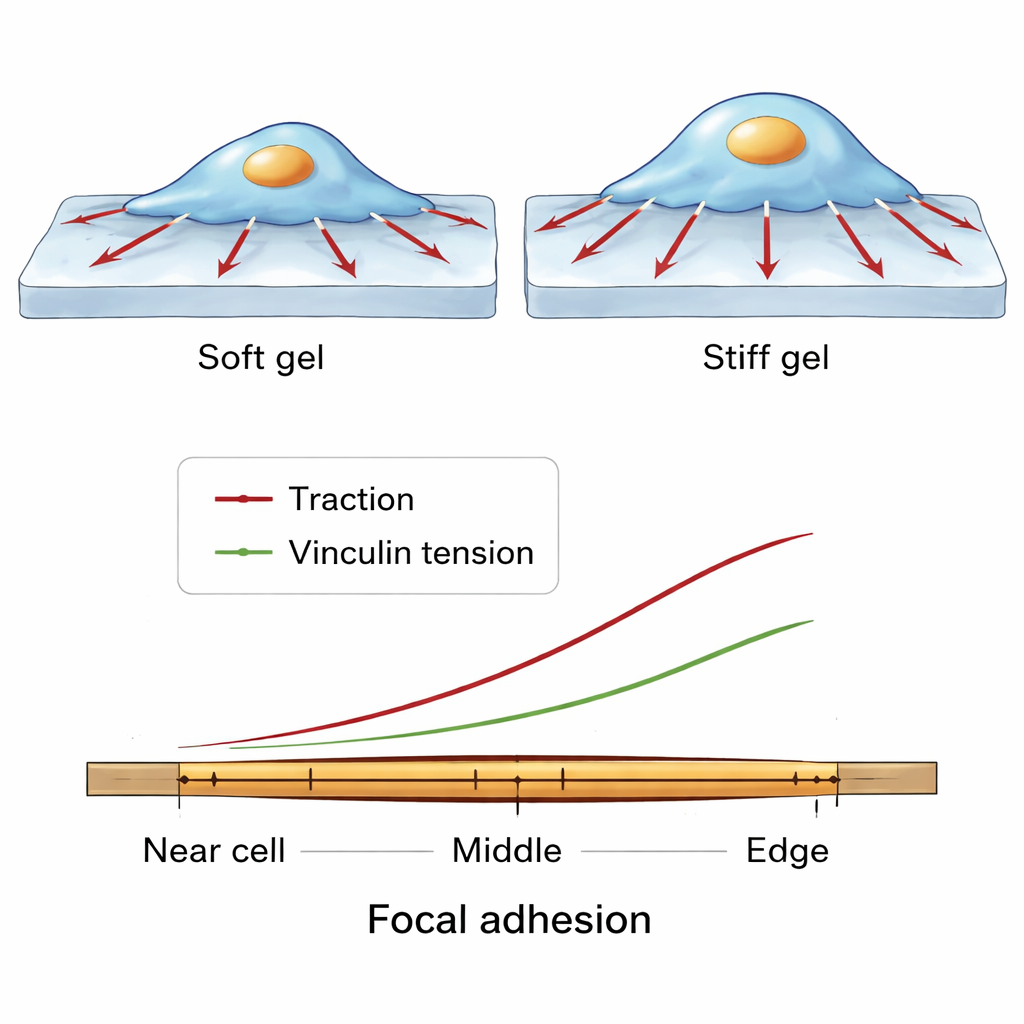
Modelli di forza a scala fine lungo un singolo punto di presa
Il gruppo ha quindi ingrandito ancora di più, esaminando come le forze cambiano lungo la lunghezza di una singola adesione focale, dalla parte più prossima al centro della cellula fino al margine vicino al perimetro cellulare. In molte cellule e condizioni emerse un modello coerente. Le molecole di vinculina erano più densamente impaccate verso il centro dell’adesione. Tuttavia, sia la trazione esercitata sul substrato sia la tensione molecolare sulla vinculina aumentavano verso l’estremità esterna e più periferica. Ciò suggerisce un equilibrio: nelle regioni centrali, molte molecole di vinculina possono condividere il carico, quindi ciascuna sente meno tensione, mentre al bordo esterno poche molecole sopportano relativamente più forza, permettendo una forte trazione locale pur mantenendo l’integrità dell’adesione.
Cosa significa tutto ciò per salute e malattia
Unendo mappe di trazione a livello cellulare con misure di tensione a livello proteico, questo studio offre un quadro multiscala di come le cellule gestiscono la loro presa meccanica. Il lavoro mostra che all’aumentare della rigidità dell’ambiente, le cellule tirano più forte e caricano maggiormente i legami di vinculina, ma che il rapporto dettagliato tra forze verso l’esterno e tensione molecolare varia da adesione ad adesione e da cellula a cellula. Contemporaneamente, sembra essere conservato un robusto schema spaziale di distribuzione delle forze all’interno delle singole adesioni. Per un lettore non specialista, il messaggio chiave è che le cellule regolano finemente sia dove sia come tirano, ridistribuendo la forza attraverso molte piccole “molle” molecolari per adattarsi a diversi ambienti meccanici — un principio che potrebbe essere alla base di processi tanto diversi quanto lo sviluppo tissutale, la fibrosi e l’invasione tumorale.
Citazione: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Parole chiave: meccanica cellulare, adesioni focali, vinculina, microscopia delle forze di trazione, meccano-trasduzione