Clear Sky Science · it
Dinamicità temporale del taglio collaterale dell'RNA da parte di LbuCas13a nelle cellule umane
Trasformare una difesa batterica in un interruttore di autodistruzione preciso
I ricercatori hanno scoperto come trasformare una proteina immunitaria batterica in un interruttore di “autodistruzione” altamente selettivo per cellule umane. Sfruttando un enzima CRISPR chiamato LbuCas13a, possono riconoscere un messaggio RNA scelto all'interno di una cellula e quindi frammentare quasi tutto il resto dell'RNA di quella cellula. Per il lettore non specialista questo è interessante perché i messaggi RNA controllano quali proteine una cellula produce; imparare a cancellarli su comando apre porte a nuovi trattamenti per il cancro, strategie antivirali e potenti strumenti di ricerca.
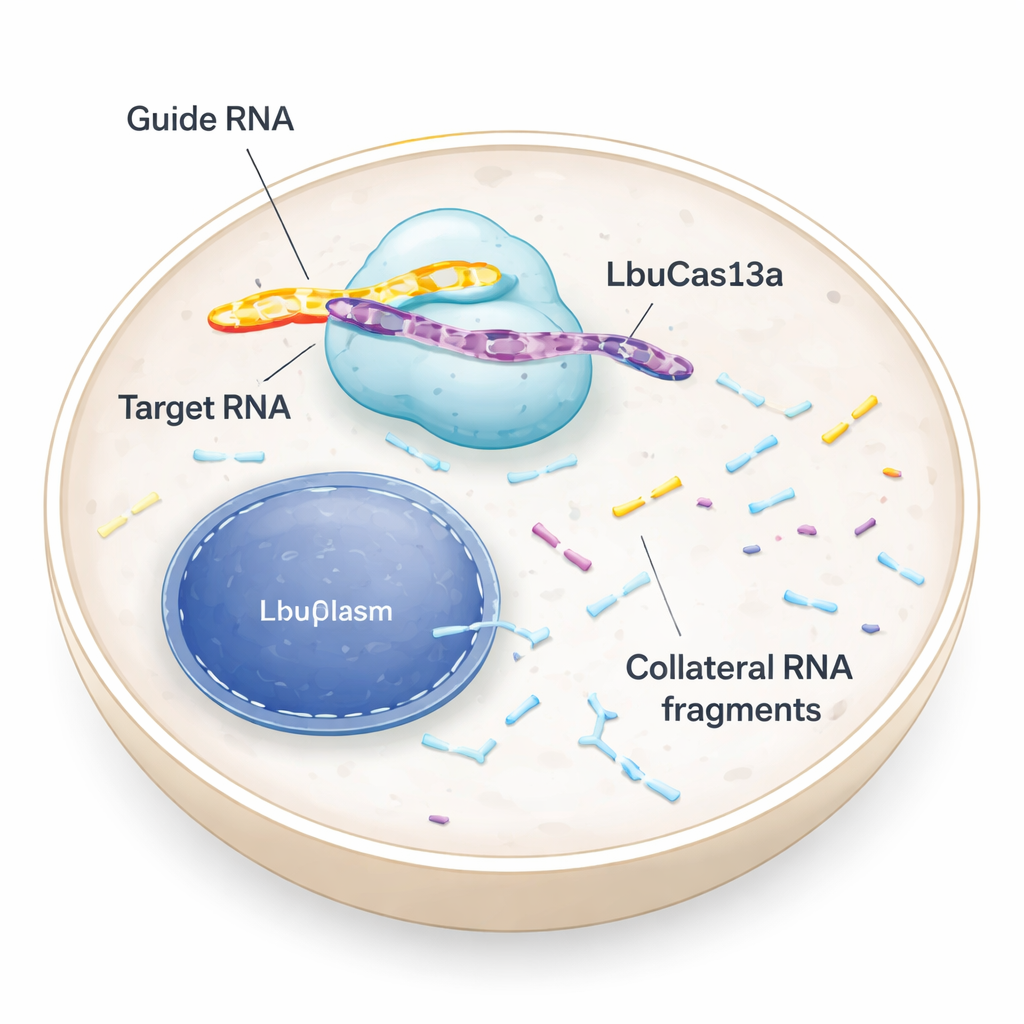
Una forbice molecolare che prende di mira l'RNA, non il DNA
La maggior parte delle persone ha sentito parlare di strumenti CRISPR che tagliano il DNA riscrivendo il codice genetico. LbuCas13a è diverso: riconosce e taglia l'RNA, i messaggi temporanei che trasportano istruzioni dal DNA alle fabbriche proteiche della cellula. Nei batteri, gli enzimi Cas13 fanno parte di una difesa antivirale. Una volta individuato un RNA virale, non solo sezionano quell'invasore ma iniziano anche a tagliare molti altri RNA nelle vicinanze. Questa attività cosiddetta “collaterale” può spingere le cellule infette in dormienza o morte, aiutando a proteggere la comunità batterica. I primi test in cellule animali e umane suggerivano che il taglio collaterale di Cas13 fosse debole o assente, perciò l'enzima veniva usato principalmente come un interruttore preciso per spegnere l'RNA. Il nuovo studio rivede quell'assunzione e mostra che, nelle condizioni giuste, l'attività collaterale nelle cellule umane può essere sia intensa sia utile.
Scatenare il taglio collaterale nelle cellule umane
Il gruppo ha confrontato diverse varianti di Cas13 e ha scoperto che LbuCas13a era particolarmente potente. Hanno fornito proteina LbuCas13a purificata pre‑caricata con un breve RNA guida direttamente nelle cellule umane, una forma di “iniezione” molecolare chiamata consegna di ribonucleoproteine (RNP). Quando la guida corrispondeva a un RNA bersaglio — come un gene marcatore fluorescente o messaggi naturali abbondanti come GAPDH e l'RNA ribosomale 18S — l'enzima prima tagliava quel bersaglio e poi cominciava a degradare molti altri RNA. Nell'arco di circa 50 minuti, il profilo complessivo dell'RNA della cellula cambiava drasticamente, con l'emergere di frammenti di taglio distintivi. Questo effetto collaterale si è osservato con diversi metodi di consegna e in una gamma di tipi cellulari, dimostrando che non era un difetto di una singola linea cellulare o di un bersaglio artificiale.
Dal frantumare l'RNA alla morte cellulare e alla selezione
Cosa succede a una cellula i cui messaggi RNA scompaiono improvvisamente? Utilizzando immagini in cellule vive, i ricercatori hanno osservato che le cellule che esprimevano l'RNA bersaglio entravano gradualmente in apoptosi, una forma ordinata di morte cellulare programmata contrassegnata da segnali di “preallarme” caratteristici prima che la cellula si disintegri. È importante che le cellule vicine che non esprimevano l'RNA bersaglio rimanessero per lo più intatte, dimostrando che l'autodistruzione è specifica. Il gruppo ha quindi sfruttato questa proprietà come strumento di selezione. Mescolando cellule portatrici del bersaglio con cellule normali e attivando LbuCas13a, le cellule con il bersaglio venivano selettivamente deplete nell'arco di alcuni giorni. Ripetere il trattamento più volte riduceva ulteriormente la loro frazione. Hanno mostrato che questo poteva arricchire per cellule effettivamente editate e potenzialmente essere tarato per attaccare cellule tumorali che sovraesprimono un oncogene, qui CDK4, risparmiando cellule correlate che producono molto meno di quell'RNA.
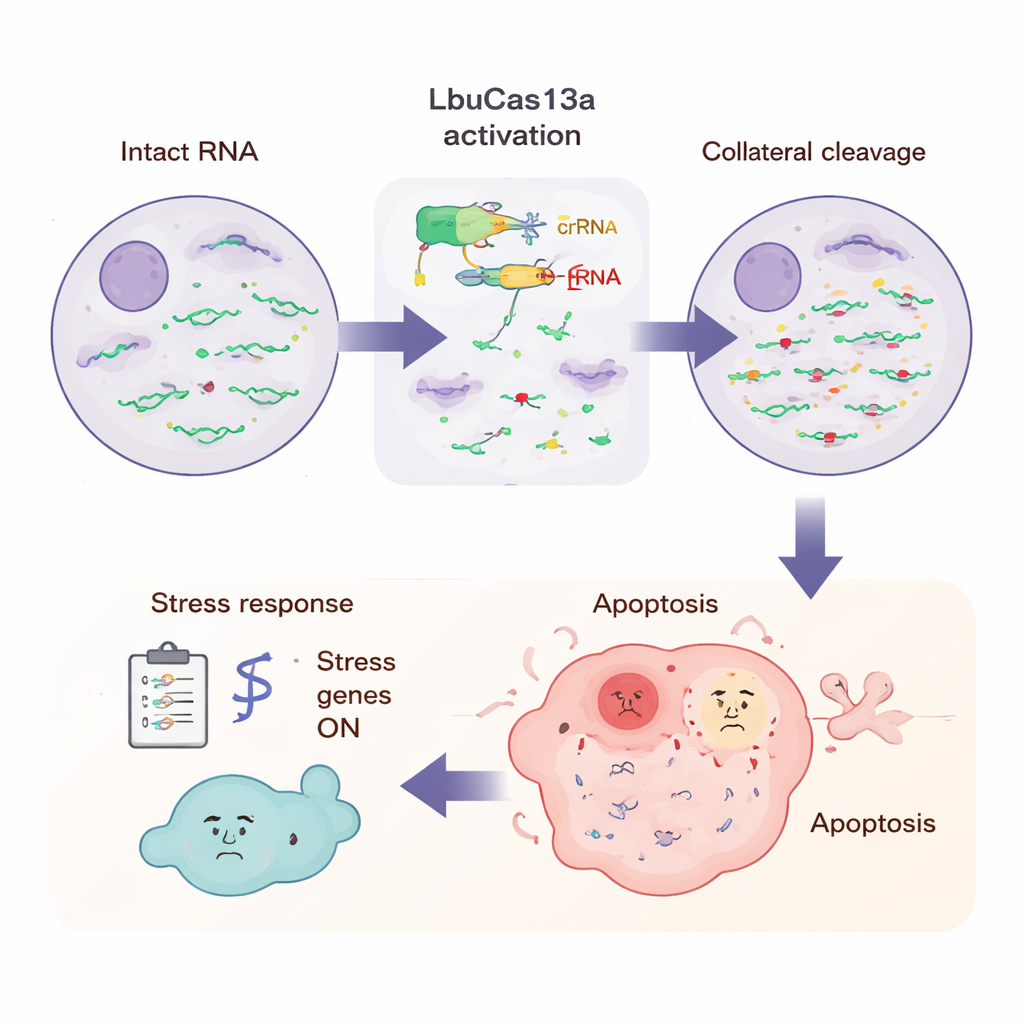
Cosa vive la cellula durante l'attacco
Per vedere il quadro più ampio, gli scienziati hanno misurato tutti gli RNA nella cellula in diversi punti temporali dopo l'attivazione di LbuCas13a. Inserendo standard RNA conosciuti, hanno potuto stabilire che la maggior parte degli RNA codificanti proteine nel citoplasma scese di oltre la metà nell'arco di poche ore, mentre alcuni RNA — come i messaggi mitocondriali e alcuni RNA non codificanti nucleari — erano in gran parte risparmiati. Il sequenziamento a letture lunghe ha rivelato che il taglio avveniva in posizioni nucleotidiche ripetute e specifiche, spesso in regioni a loop flessibili dell'RNA ricche della base uracile, coerenti con i modelli osservati in esperimenti in vitro. Nei tempi successivi molti geni legati allo stress e all'immunità innata si attivavano, inclusi quelli associati a segnali infiammatori e difese antivirali. Questo schema suggerisce che la cellula percepisce l'improvvisa abbondanza di estremità di RNA rotti in modo simile a come rileverebbe un'infezione virale, attivando un programma d'allarme che culmina nell'apoptosi.
Perché è importante e dove potrebbe portare
In termini semplici, lo studio mostra che LbuCas13a può essere trasformato in un “interruttore di morte” guidato dall'RNA: se una cellula produce troppo di un particolare RNA, attivare LbuCas13a contro quell'RNA provoca una perdita quasi globale dell'RNA, un allarme di tipo immunitario e poi la morte cellulare controllata. Poiché il processo dipende fortemente dall'abbondanza dell'RNA bersaglio, potrebbe essere usato per eliminare cellule che sovraesprimono geni dannosi — come certe cellule tumorali — o per ripulire cellule indesiderate in colture miste durante la ricerca o la produzione di terapie cellulari. Allo stesso tempo, il lavoro è un monito: gli strumenti CRISPR mirati all'RNA possono avere effetti collaterali potenti che vanno gestiti con attenzione. Capire quando e come si verifica il taglio collaterale dell'RNA è essenziale per usare in sicurezza le tecnologie Cas13 in medicina e biotecnologia.
Citazione: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Parole chiave: CRISPR-Cas13, Taglio dell'RNA, Morte cellulare, Targeting del cancro, Strumenti di editing genico