Clear Sky Science · it
Modulazione dei recettori B1 della classe GPCR umani da parte dei lipidi della membrana plasmatica
I grassi che rifiniscono i nostri ricevitori di segnali cellulari
Le nostre cellule si affidano a piccole antenne proteiche, chiamate recettori, per percepire ormoni e neurotrasmettitori. Molti farmaci di grande successo agiscono proprio su questi recettori. Questo studio mostra che i grassi comuni presenti nello strato esterno delle nostre cellule fanno molto più che costituire uno sfondo passivo: si legano direttamente e modellano una famiglia intera di recettori chiave, influenzando sottilmente l’attivazione o l’inattivazione dei segnali. Comprendere questo livello nascosto di controllo potrebbe aiutare a progettare farmaci più intelligenti e con meno effetti collaterali.
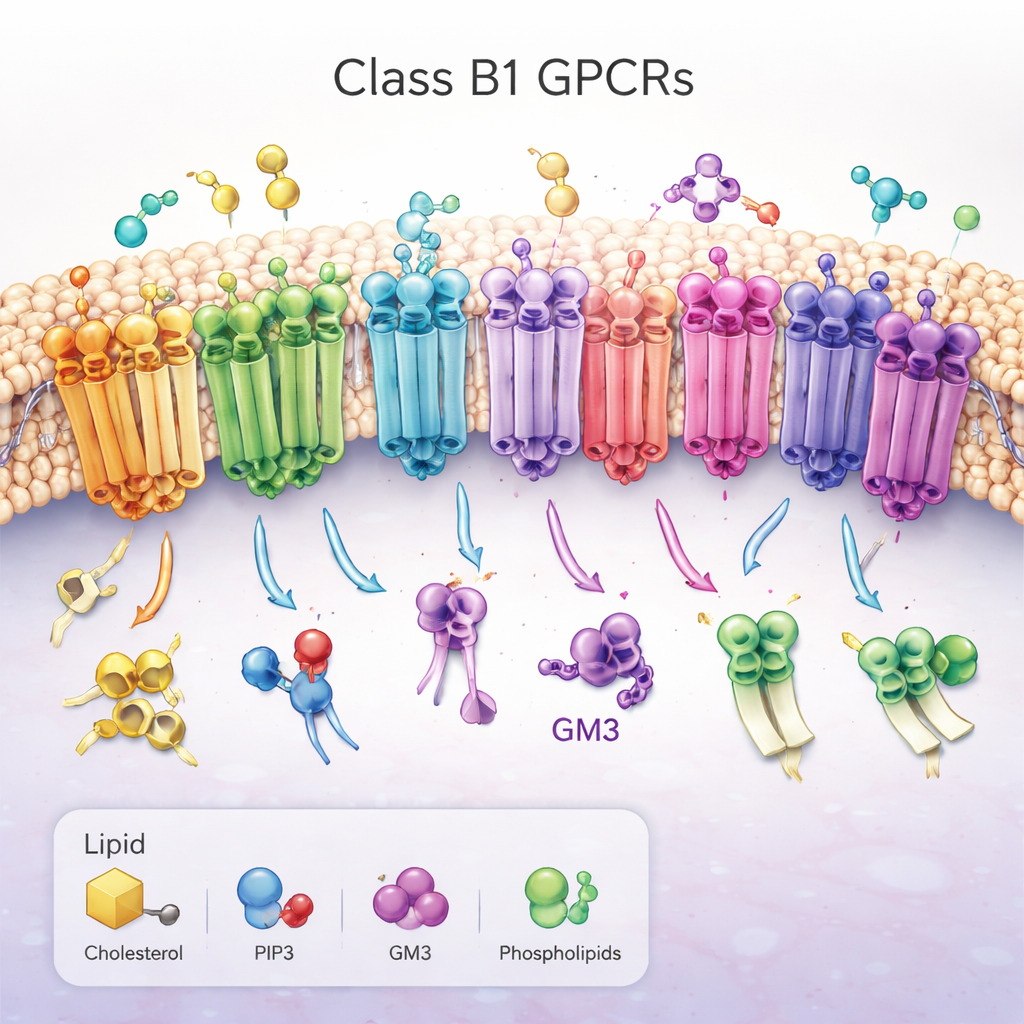
Una famiglia di importanti antenne molecolari
Il lavoro si concentra sui recettori accoppiati alle proteine G di classe B1 (GPCR), un gruppo di 15 recettori strettamente correlati che aiutano a regolare la glicemia, il metabolismo, la crescita e le risposte allo stress. Sono inseriti nella membrana esterna della cellula, con una grande “testa” esterna che cattura molecole di tipo ormonale e un fascio di sette eliche che attraversano la membrana lipidica. Quando vengono attivati, questi recettori cambiano forma sul lato interno della cellula, aprendo una fessura che recluta proteine partner e innesca cascate di segnalazione. Per il loro ruolo centrale in malattie come il diabete e l’obesità, i GPCR di classe B1 sono bersagli farmacologici di primo piano, ma il modo in cui i lipidi della membrana circostante li regolano è rimasto in gran parte oscuro.
Simulare i recettori nel loro ambiente naturale
Invece di studiare i recettori in bolle di detergente artificiali, i ricercatori hanno inserito tutti i 15 recettori umani di classe B1 in membrane costruite al calcolatore che imitano la complessa miscela di lipidi delle cellule reali. Usando una tecnica chiamata dinamica molecolare a grana grossa, hanno eseguito molte simulazioni lunghe per ciascun recettore sia nello stato attivo sia in quello inattivo, per un totale di circa un millisecondo di tempo simulato. Hanno monitorato come tre lipidi “regolatori”—il colesterolo, il lipide di segnalazione PIP2 e il grasso decorato di zuccheri GM3—si avvicinavano, si legavano e si staccavano da diverse regioni di ciascun recettore. Per assicurare che altri possano riprodurre e ampliare questo enorme dataset, hanno catturato ogni passaggio della preparazione e dell’analisi usando uno strumento di workflow open source chiamato aiida-gromacs, e hanno confrontato i loro risultati basati sulla fisica con le predizioni di un nuovo modello di IA (Chai‑1) che ipotizza come le proteine legano piccole molecole.
Tasche nascoste e una presa conservata per i lipidi
Le simulazioni hanno rivelato schemi ricorrenti di legame in tutta la famiglia di recettori. Il colesterolo, noto soprattutto nei discorsi sull’alimentazione, è stato osservato non solo incastrarsi in un sito precedentemente noto su una delle eliche, ma anche in “tasche profonde” nella membrana tra le eliche, con la sua testa polare sepolta in modo insolito nel mezzo della membrana. Un recettore, il recettore della secretina, ha mostrato un legame con il colesterolo particolarmente duraturo in tasche distinte nelle sue forme attiva e inattiva, suggerendo che il colesterolo potrebbe fortemente favorire il suo modo di segnalare. PIP2 ha mostrato un comportamento sorprendentemente conservato: si è raggruppato attorno alla faccia interna dei recettori alla giunzione di due eliche e un breve segmento di coda (TM6, TM7 e H8), in particolare quando i recettori erano nello stato attivo. In questo sito, reti di amminoacidi carichi positivamente afferravano il gruppo testa negativamente carico di PIP2, suggerendo un meccanismo con cui questo lipide potrebbe stabilizzare la forma attiva o aiutare a reclutare partner di segnalazione sul lato interno della cellula.
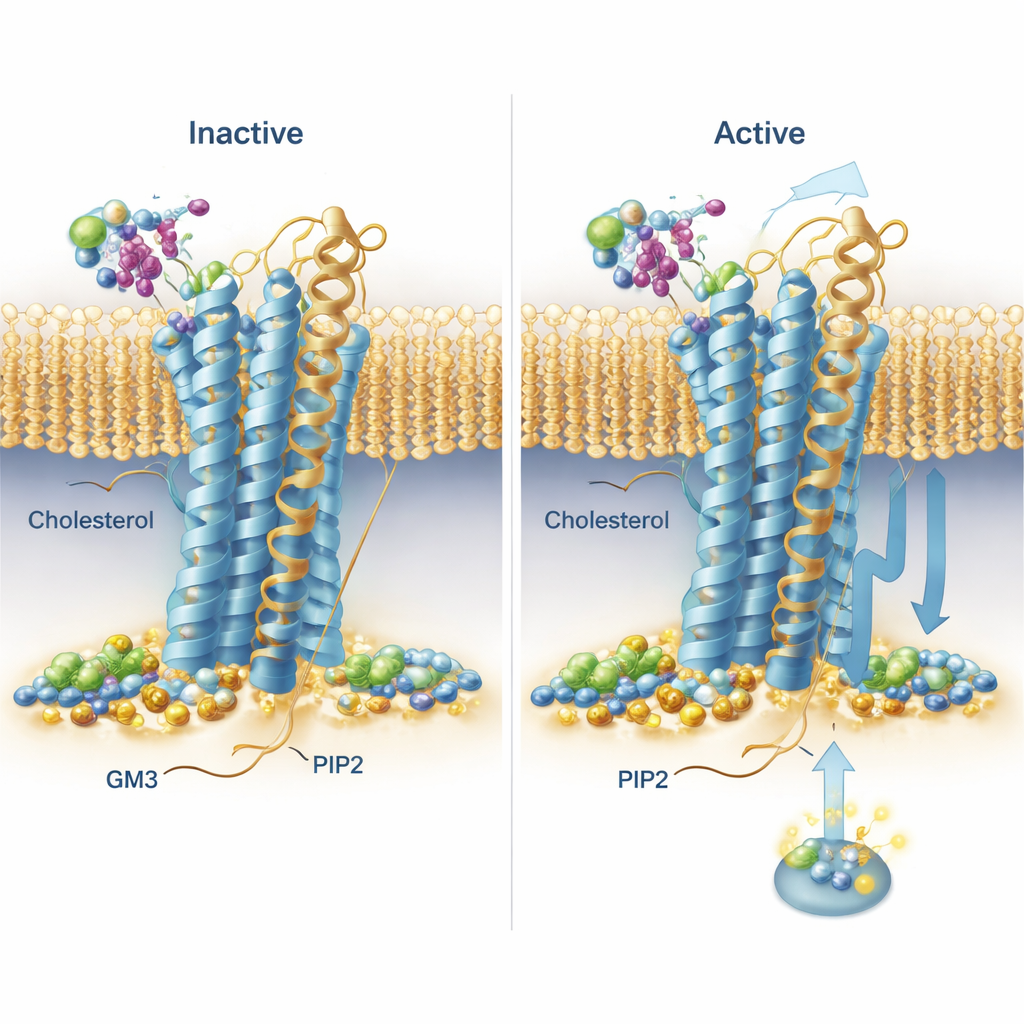
Un lipide ricoperto di zuccheri che spinge il movimento del recettore
GM3, un lipide complesso con una testa zuccherina, interagiva principalmente con le grandi teste esterne dei recettori. Il gruppo ha notato che i domini esterni di alcuni recettori oscillavano e si piegavano molto rispetto alla membrana, mentre altri erano più vincolati. Per due recettori rilevanti per i farmaci—GLP‑1R e GIPR—hanno esaminato in dettaglio il ruolo di GM3. Nelle simulazioni con GM3 presente, il lipide si è piazzato o contro la base del dominio esterno e della tasca di legame del ligando (GLP‑1R) o si è attaccato all’estremità distante del dominio esterno (GIPR), in entrambi i casi influenzando la libertà di movimento di questi domini. Per testare queste predizioni in cellule vive, i ricercatori hanno utilizzato una tecnica basata sulla luce (TR‑FRET) che segnala quanto una testa di recettore etichettata sia vicina alla membrana. Riducendo i livelli di GM3 con un inibitore a piccola molecola, hanno osservato cambi misurabili nello spostamento delle teste dei recettori dopo stimolazione, coerenti con l’idea che GM3 regoli la flessibilità dei recettori in modo specifico per recettore e stato.
Perché queste partnership lipide–recettore sono importanti
Complessivamente, lo studio dipinge i GPCR di classe B1 non solo come interruttori ormonali ma come parti di una danza strettamente coreografata con i lipidi circostanti. Il colesterolo può occupare tasche nascoste e favorire sottilmente certi esiti di segnalazione, il PIP2 forma una “maniglia” interna conservata che potrebbe bloccare i recettori nelle loro forme attive e guidare le proteine partner, e il GM3 modifica il modo in cui le regioni esterne dei recettori si muovono e incontrano i loro ligandi. Per i non specialisti, il messaggio chiave è che la membrana è uno strato regolatorio attivo: piccole differenze nella composizione lipidica possono cambiare il comportamento dello stesso recettore in tessuti o stati patologici diversi. Mappando queste interazioni in dettaglio e condividendo i dati di simulazione sottostanti, questo lavoro pone le basi per progettare futuri farmaci che sfruttino o evitino contatti lipidici specifici, potenzialmente rendendo i trattamenti più selettivi ed efficaci.
Citazione: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Parole chiave: Recettori accoppiati alle proteine G, lipidi di membrana, colesterolo, PIP2, GM3