Clear Sky Science · it
Informazioni strutturali sul trasporto di metallocluster nello scaffold di assemblaggio della nitrogenasi NifEN
Come la Natura Costruisce uno Strumento Chimico Potente
L'azoto è ovunque nell'aria, ma la maggior parte degli organismi non può utilizzarlo in quella forma. Un enzima speciale chiamato nitrogenasi risolve questo problema trasformando l'azoto atmosferico in ammoniaca, un ingrediente fondamentale per la vita e per i fertilizzanti. Al centro della nitrogenasi si trova un denso “cluster” metallico che svolge la chimica più impegnativa, ma il modo in cui le cellule assemblano questo pezzo intricato è rimasto poco chiaro. Questo articolo dà uno sguardo all'interno di quel processo di costruzione, rivelando come una proteina scaffold chiamata NifEN funzioni da dock di carico flessibile e sistema di trasporto per il carico metallico del cluster.
Una Fabbrica Molecolare Dietro Fertilizzanti e Carburanti
La nitrogenasi è l'equivalente naturale dei processi industriali che producono ammoniaca e carburanti liquidi. Invece di enormi reattori, i microbi usano una macchina proteica compatta alimentata dall'energia cellulare. La sua efficienza dipende da un centro metallico straordinariamente complesso, costruito con ferro, zolfo, molibdeno, carbonio e un gruppo laterale organico. Assemblare questo nucleo è troppo delicato per essere lasciato al caso, quindi le cellule impiegano una squadra di proteine ausiliarie. Una delle più importanti è NifEN, che riceve un precursore quasi completo a base totalmente di ferro (chiamato L‑cluster), ne favorisce la conversione nella forma matura (il M‑cluster) e poi lo consegna all'enzima nitrogenasi funzionante. Capire come NifEN gestisca questo traffico potrebbe orientare sforzi per ingegnerizzare microbi per una produzione di fertilizzanti più pulita o per nuovi combustibili a base di carbonio.
Vedere una Macchina in Movimento con Istantanee Congelate
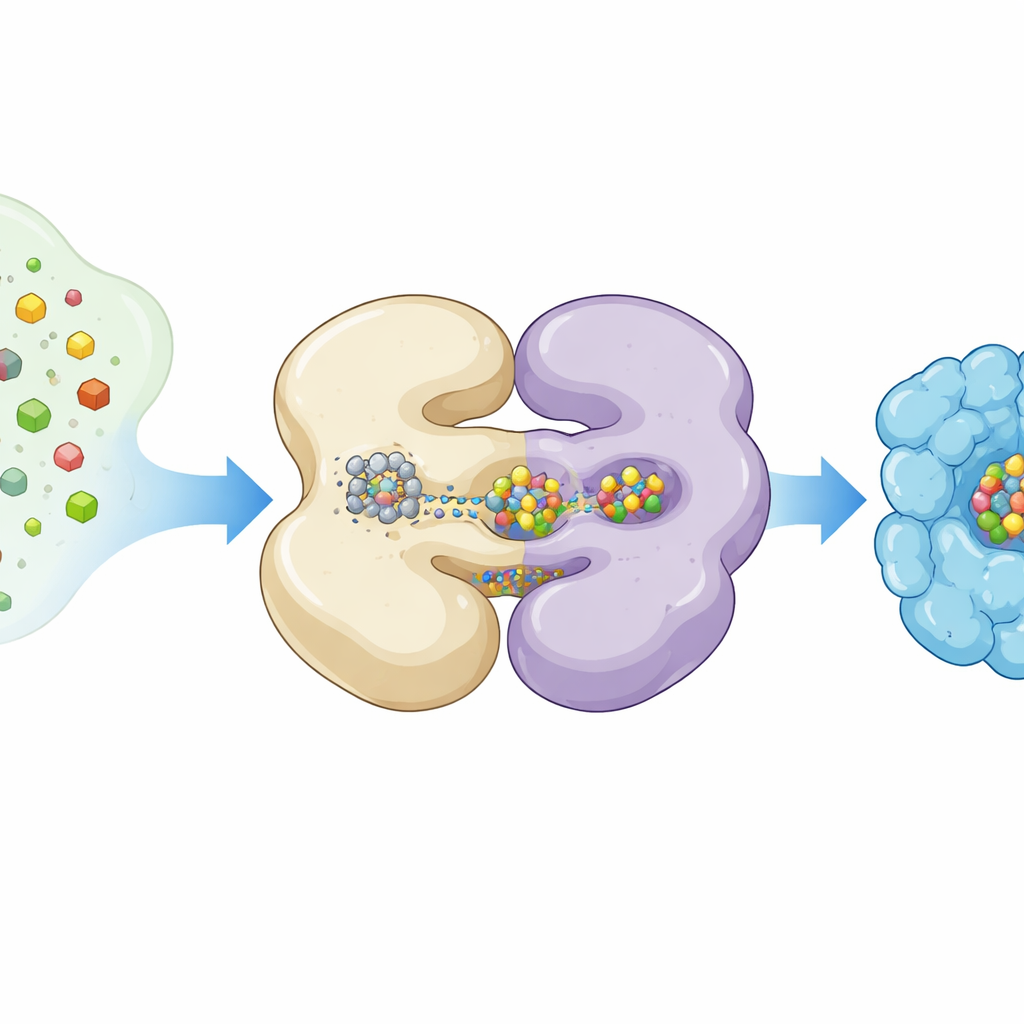
Gli autori hanno usato la crio‑microscopia elettronica, una tecnica che riprende proteine a temperature estremamente basse, per catturare NifEN in diverse pose operative. Hanno espresso NifEN in batteri da laboratorio in modo che alcune copie proteiche portassero un L‑cluster e altre fossero vuote. Ordinando milioni di immagini single‑particle, hanno ricostruito due forme principali: una forma “apo” priva del cluster mobile e una forma “olo” con il cluster legato in una sede interna. Entrambe le forme condividono un core costituito da quattro subunità disposte in due coppie, ma quando il L‑cluster è presente, metà della struttura di NifEN diventa visibilmente più ordinata e diverse eliche ruotano verso l'interno, stringendosi attorno al carico metallico.
Un Tunnel Nascosto per il Carico Metallico
Il confronto tra le strutture vuota e caricata ha rivelato una caratteristica sorprendente: un lungo tunnel che attraversa il dimero di NifEN. Nello stato vuoto, questo passaggio è ampio e aperto; dopo il legame del cluster si restringe mentre la proteina afferra il suo passeggero. Precedenti strutture cristalline avevano mostrato una posizione alternativa “esterna” per l'L‑cluster vicino alla superficie proteica. Mettere insieme tutte le osservazioni ha permesso ai ricercatori di inferire che il cluster può occupare almeno due stazioni su NifEN—una sepolta all'interno e una esposta—e muoversi tra di esse lungo un percorso curvo regolato da spostamenti in un dominio flessibile. Questo movimento sembra essere più rilassato rispetto all'enzima nitrogenasi finale, il cui cluster attivo è tenuto rigidamente in posizione, suggerendo che NifEN sia progettato per il trasferimento piuttosto che per la catalisi a lungo termine.
Partner di Docking e una Rotta Continua
Per capire come NifEN si connette ai suoi partner a monte e a valle, il team ha combinato le loro strutture sperimentali con modelli computazionali di AlphaFold 3 e microscopia elettronica a risoluzione più bassa di complessi proteici. I modelli suggeriscono che l'enzima NifB, che costruisce l'L‑cluster da pezzi più piccoli ferro‑zolfo, si ancorerebbe in una valle su una faccia di NifEN. Lì, è possibile tracciare un tunnel continuo dai centri metallici di NifB direttamente nel tunnel di NifEN e fino alla stazione interna dell'L‑cluster. Sull'altra faccia di NifEN, un diverso sito di docking ospita NifH, la proteina che inserisce il molibdeno e un gruppo laterale organico per completare il cofattore. In questa configurazione, l'L‑cluster si trova nella sede superficiale, idealmente posizionato per la modifica. Mutazioni in aminoacidi chiave che fiancheggiano la rotta proposta interrompono il caricamento, il movimento o la maturazione del cluster, fornendo supporto sperimentale per questo modello a nastro trasportatore.
Perché uno Scaffold Flessibile Conta
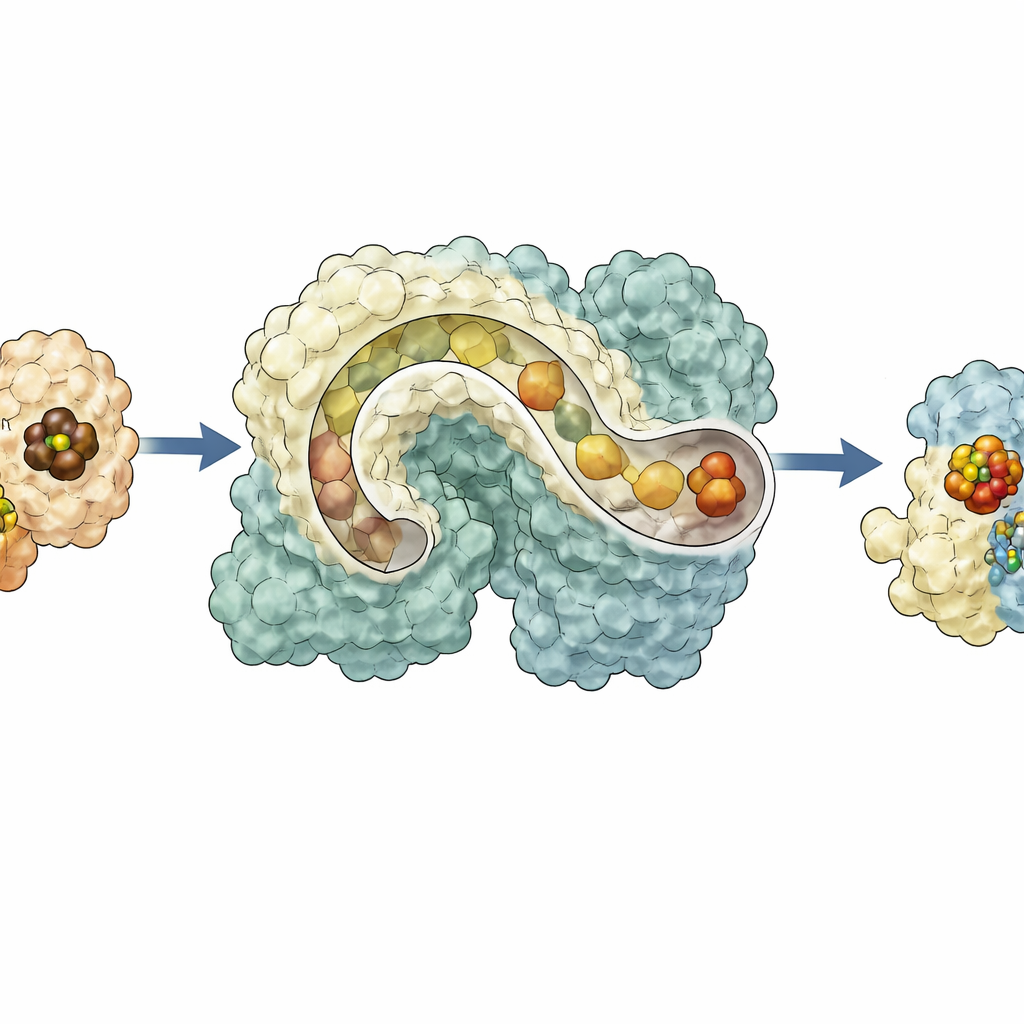
Nel complesso, i risultati dipingono NifEN come un hub dinamico che riceve un nucleo metallico da NifB su un lato, lo sposta in una baia di stoccaggio interna, poi lo presenta sulla superficie opposta per il rifinitura da parte di NifH prima di guidare il cluster maturo di nuovo all'interno per la consegna alla nitrogenasi. Questo schema di traffico regolato dalla conformazione spiega come più passaggi delicati possano essere coordinati all'interno di un singolo quadro proteico e suggerisce come enzimi antichi possano essersi evoluti da scaffold più flessibili verso i catalizzatori altamente specializzati di oggi. Per i non specialisti, il lavoro mostra che anche alla scala nanometrica, la natura si affida a linee di assemblaggio, tunnel e parti mobili per costruire gli strumenti molecolari che sostengono i cicli globali dell'azoto, la produzione alimentare e, potenzialmente, future tecnologie verdi.
Citazione: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Parole chiave: nitrogenasi, assemblaggio di metallocluster, scaffold NifEN, crio microscopia elettronica, fissazione biologica dell'azoto