Clear Sky Science · it
Combinare apprendimento federato e modello viaggiante migliora le prestazioni e apre opportunità per l’equità digitale in sanità
Perché condividere conoscenze mediche senza condividere i dati è importante
La medicina moderna fa sempre più affidamento sull’intelligenza artificiale per individuare schemi nelle immagini diagnostiche e nei registri clinici. Tuttavia i dati dei pazienti sono sensibili e spesso non possono lasciare l’ospedale in cui sono stati raccolti. Questo crea una tensione: come possono gli ospedali di tutto il mondo collaborare per addestrare potenti strumenti di IA senza inviare dati grezzi dei pazienti oltre confine o a grandi server centrali? Questo studio introduce un nuovo modo per farlo, puntando non solo all’accuratezza, ma anche all’equità tra ospedali ben finanziati e cliniche più piccole e con meno risorse.
Due modi per addestrare un’IA senza spostare i dati
Oggi esistono due strategie principali che permettono agli ospedali di addestrare un’IA insieme mantenendo i dati in loco. Nell’apprendimento federato, ogni ospedale addestra in parallelo una copia locale del modello; questi modelli locali vengono poi combinati in un modello “globale” condiviso su un server centrale. Nell’approccio del modello viaggiante, esiste un unico modello che si sposta da un ospedale all’altro addestrandosi su ciascun sito a turno. Entrambi i metodi proteggono la privacy, ma ciascuno ha svantaggi. L’apprendimento federato può avere difficoltà quando alcuni ospedali hanno pochissimi dati o non includono tutti i tipi di pazienti; combinare modelli locali deboli o sbilanciati può portare a un modello globale che riflette soprattutto i siti grandi e ben dotati. Il modello viaggiante è più robusto a questi squilibri ma può essere più lento e più difficile da gestire.
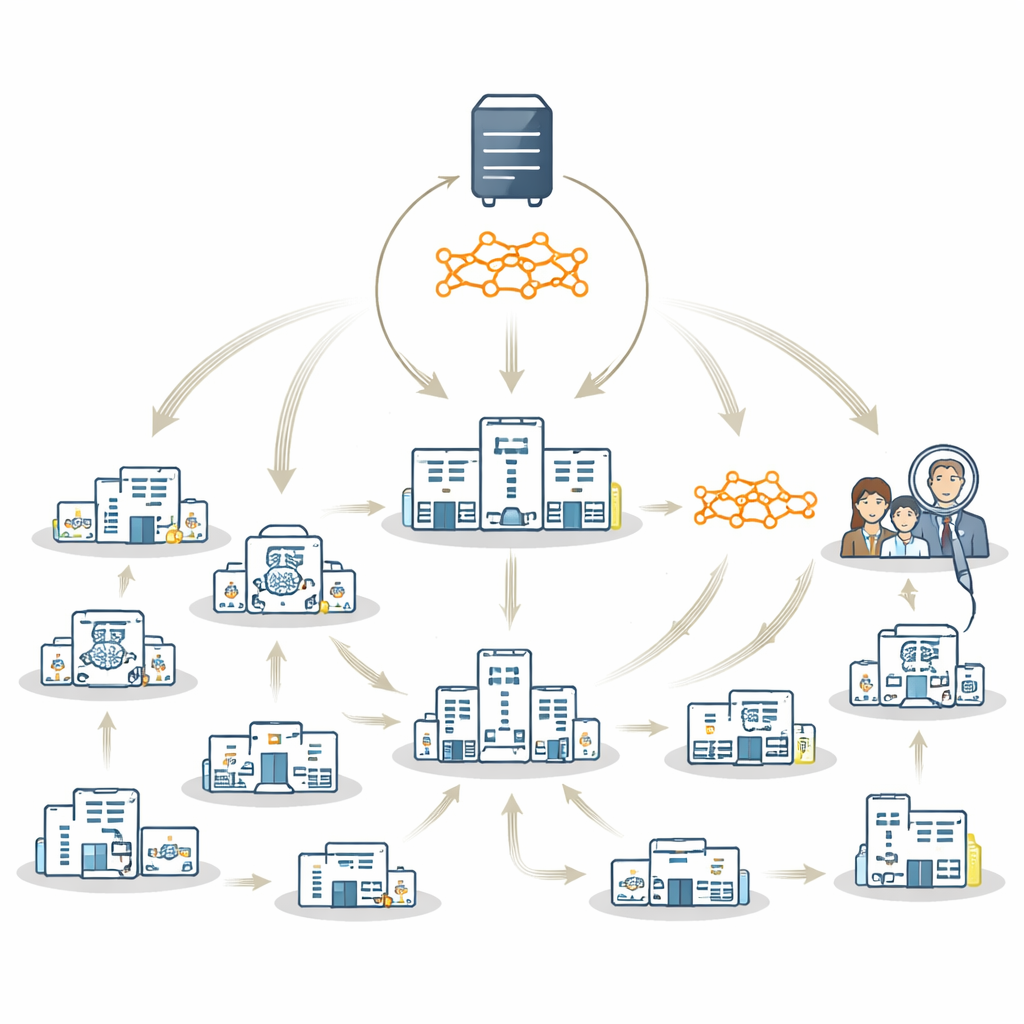
Una strategia ibrida che sfrutta il meglio dei due approcci
Gli autori propongono FedTM, uno schema di addestramento ibrido che fonde i punti di forza dell’apprendimento federato e del modello viaggiante. L’addestramento avviene in due fasi. Prima c’è una fase di “warmup” in cui solo gli ospedali più grandi, con dataset più completi e bilanciati, addestrano il modello in parallelo usando tecniche federate standard. Questo crea un modello di partenza robusto. Poi segue una fase di “rifinitura”, in cui questo modello riscaldato visita ogni sito in sequenza, incluse cliniche molto piccole che possono avere solo poche risonanze cerebrali o anche un solo paziente. In questa seconda fase il modello viene aggiornato gradualmente mentre viaggia, incorporando conoscenza da ciascun sito senza che i loro dati escano mai dal controllo locale.
Testare il metodo sulle risonanze cerebrali per il morbo di Parkinson
Per mettere alla prova FedTM, i ricercatori hanno utilizzato 1.817 risonanze magnetiche cerebrali provenienti da 83 siti di imaging in tutto il mondo per addestrare un sistema di IA a distinguere persone con morbo di Parkinson da individui sani. Questo è un contesto particolarmente impegnativo: più della metà dei siti ha contribuito con meno di dieci scansioni, solo circa un terzo disponeva sia di pazienti che di controlli sani, e i protocolli di acquisizione differivano ampiamente. In queste condizioni reali, il puro apprendimento federato non è riuscito a imparare bene il compito, mentre un modello viaggiante puro ha funzionato meglio ma lasciava ancora margini di miglioramento. FedTM, specialmente quando il warmup coinvolgeva i sette siti più grandi e bilanciati, ha superato chiaramente entrambi: l’area sotto la curva ROC, una misura standard della qualità di classificazione, è passata dal 77% con il solo modello viaggiante a circa l’82% con FedTM, con guadagni simili anche in altri indicatori clinicamente rilevanti come sensibilità, specificità e F1-score.
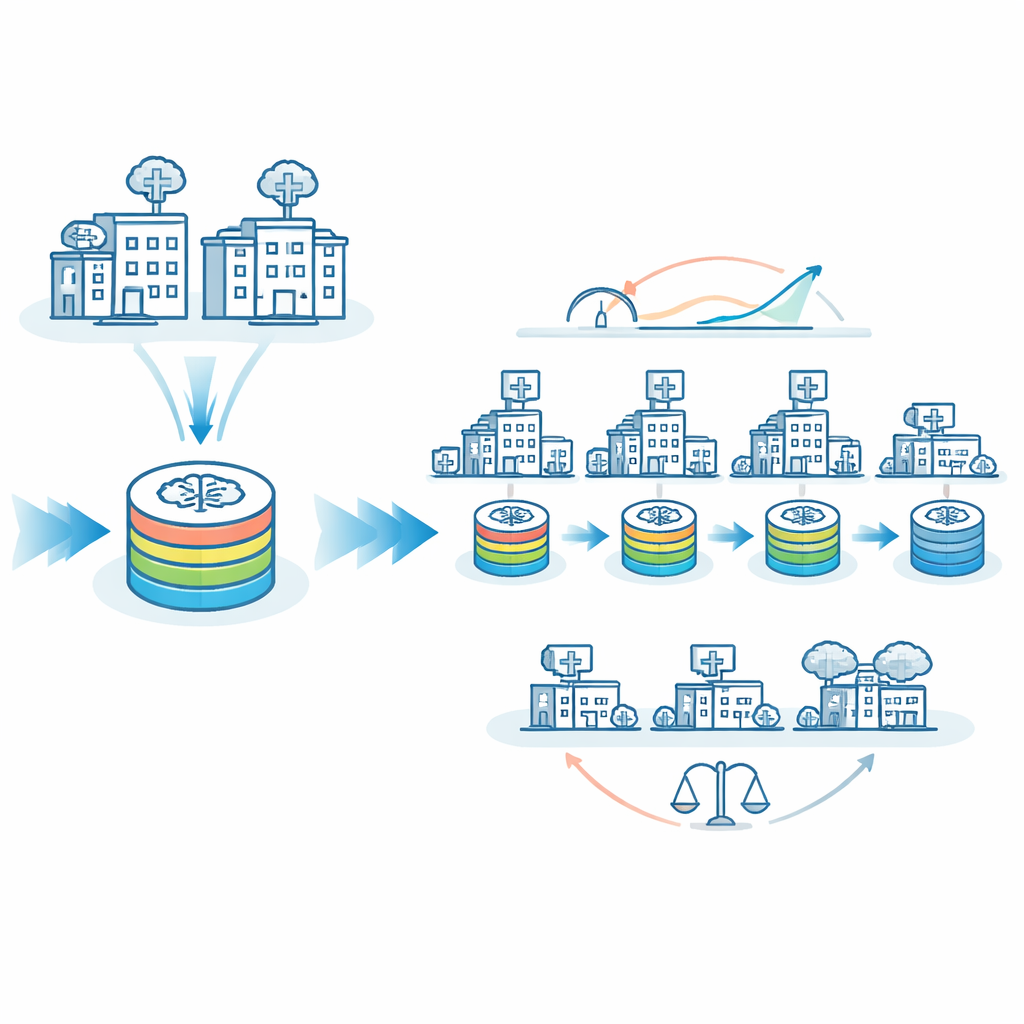
Rendere l’IA più equa tra ospedali grandi e piccoli
Una preoccupazione centrale nell’IA medica è l’equità: un modello funziona allo stesso modo per i pazienti di ospedali piccoli, rurali o con poche risorse come per quelli dei grandi centri accademici? Il team ha analizzato quanto spesso l’IA commettesse errori di classificazione nei siti “più grandi” rispetto a quelli “più piccoli”. Con il solo modello viaggiante, i tassi di errore differivano di circa 8 punti percentuali tra questi gruppi. Con FedTM opportunamente tarato, i tassi di errore per siti grandi e piccoli sono diventati quasi identici, intorno al 26%. In altre parole, il modello è diventato non solo più accurato nel complesso, ma anche più equilibrato. FedTM ha inoltre spostato la maggior parte del carico computazionale nella fase di warmup nei siti meglio dotati, dimezzando quasi il numero di cicli di addestramento che i siti piccoli dovevano eseguire, mantenendo però tempi di addestramento totali simili.
Che cosa significa per la sanità digitale globale
FedTM offre una strada pratica verso strumenti di IA che rispettano la privacy, migliorano le prestazioni e distribuiscono i benefici in modo più equo a livello globale. Permettendo anche ai siti con pochissimi dati di influenzare il modello finale, questo quadro può contribuire a fare in modo che le persone in contesti remoti o con risorse limitate non vengano lasciate indietro quando si sviluppano nuovi strumenti diagnostici. Pur concentrandosi su un unico tipo di scansione cerebrale e su una sola malattia, l’approccio può, in linea di principio, essere adattato a molti altri problemi medici. Con l’adozione crescente di dispositivi mobili e wearable nei sistemi sanitari e con una normativa sempre più attenta alla sovranità dei dati, strategie ibride come FedTM potrebbero diventare fondamentali per costruire un’IA medica affidabile, inclusiva e responsabile.
Citazione: Souza, R., Stanley, E.A.M., Ohara, E.Y. et al. Combining federated learning and travelling model boosts performance and opens opportunities for digital health equity. npj Digit. Med. 9, 294 (2026). https://doi.org/10.1038/s41746-026-02483-y
Parole chiave: apprendimento federato, modello viaggiante, morbo di Parkinson, IA per imaging medico, equità sanitaria