Clear Sky Science · it
Decodificare l’asse immunoregolatorio ERS–CAF attraverso l’IA multimodale e il suo valore prognostico e predittivo terapeutico pancancer
Osservare i tumori senza bisturi
I medici oncologi riconoscono sempre più che ciò che circonda un tumore può essere importante quanto il tumore stesso. Tuttavia campionare ripetutamente questo quartiere nascosto tramite biopsie è invasivo e spesso impraticabile. Questo studio mostra come l’intelligenza artificiale (IA) possa leggere esami di imaging di routine e vetrini microscopici per inferire processi immunitari e cicatriziali difficili da misurare all’interno dei tumori, trasformando potenzialmente gli esami di uso comune in una sorta di “biopsia digitale” applicabile a diversi tipi di cancro.
Le cellule di supporto nascoste che modellano il cancro
Molti tumori solidi sono avvolti in un involucro fibroso e resistente prodotto da cellule di supporto specializzate chiamate fibroblasti. Quando queste cellule sono sotto stress nel loro “stabilimento proteico” (il reticolo endoplasmatico), assumono uno stato aggressivo che favorisce il cancro. Nel condroma, un raro tumore osseo, questi fibroblasti stressati costruiscono una matrice densa e contribuiscono a tenere lontane le cellule immunitarie, rendendo i trattamenti meno efficaci. Ambienti simil‑fibrotici e poveri di cellule immunitarie emergono anche in altri tumori, come quelli del pancreas e del colon‑retto, suggerendo che questa biologia non è unica di una singola malattia. La difficoltà sta nel fatto che i metodi attuali per misurare questi fibroblasti stressati e il loro comportamento immuno‑escludente si basano su campioni tissutali e test molecolari complessi, difficili da ripetere e inclini a perdere regioni importanti del tumore.
Insegnare all’IA a vedere la biologia invisibile
I ricercatori si sono chiesti se le normali risonanze magnetiche preoperatorie e i vetrini istologici H&E contengano già indizi visivi su questa barriera immunitaria dei fibroblasti stressati. Hanno creato tre “score” numerici di riferimento a partire dall’RNA sequencing del tumore: uno che cattura quanto è attivo il programma di stress nei fibroblasti, uno che riassume quanto fortemente queste cellule sembrano segnalare alle cellule immunitarie e uno che descrive la diversità delle popolazioni immunitarie e di supporto circostanti. Invece di prevedere migliaia di geni, la loro IA è stata addestrata a prevedere solo questi tre punteggi biologicamente significativi a partire unicamente dalle immagini. Per farlo, il team ha combinato due rami: uno che analizza trame e caratteristiche morfologiche della risonanza e un altro che scansiona migliaia di piccole regioni nel vetrino digitale e usa un meccanismo di attenzione guidato dal linguaggio per focalizzarsi sulle aree che corrispondono alle descrizioni di esperti di tessuto fibrotico e povero di cellule immunitarie.
Fondere scansioni e vetrini per segnali più robusti
Su 126 pazienti con condroma con MRI, vetrini istologici, dati di RNA e follow‑up corrispondenti, il modello multimodale fuso ha superato i modelli che usavano solo la MRI o solo i vetrini. Le sue predizioni dei tre score molecolari concordavano strettamente con le misure basate sull’RNA e sono rimaste ben calibrate tra ospedali e scanner diversi. Quando i patologi hanno marcato in modo indipendente le regioni fibrotiche e immuno‑escluse, i “punti caldi” individuati dall’IA tendevano ad accendersi nelle stesse aree, suggerendo che stesse tracciando una biologia reale piuttosto che la sola dimensione del tumore. Il modello ha inoltre catturato elementi prognostici: punteggi previsti più alti di stress‑fibroblasti e di segnalazione sono stati associati a una sopravvivenza peggiore, mentre una maggiore diversità del microambiente prevista offriva una protezione parziale. L’aggiunta di questi score derivati dall’IA ai fattori clinici di routine ha migliorato la capacità di separare nel tempo pazienti ad alto e basso rischio.
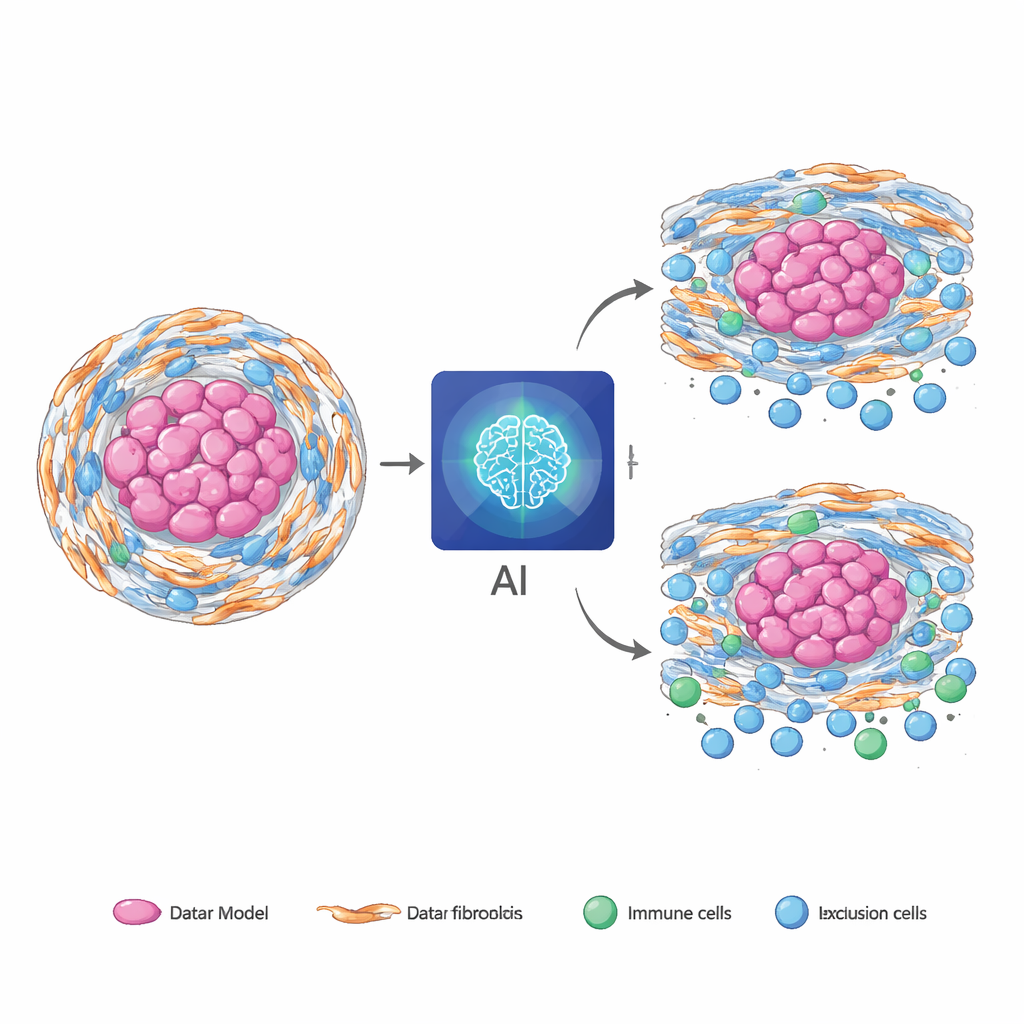
Da tumori rari a tumori comuni
Un test cruciale è stato verificare se un modello addestrato interamente sul condroma potesse essere usato “così com’è” in altri tumori più comuni. Applicata senza ri‑addestramento a tumori del pancreas, dello stomaco e del colon‑retto provenienti da grandi set di dati pubblici, la versione del modello basata solo sui vetrini ha comunque mostrato un allineamento significativo tra le sue predizioni da immagine e i punteggi RNA ricomputati ex novo. In alcuni di questi tumori, gli score dell’IA hanno migliorato la previsione della sopravvivenza dei pazienti oltre le informazioni cliniche standard e hanno aiutato a distinguere quali pazienti erano più propensi a beneficiare della chemioterapia. Per rendere l’approccio più facilmente distribuibile dove la patologia digitale è limitata, il team ha distillato il modello multimodale completo in una versione basata solo sulla MRI che ha mantenuto gran parte della capacità predittiva, funzionando più velocemente e con meno risorse computazionali.
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati supportano l’idea che le immagini mediche di routine contengano discretamente informazioni su cellule di supporto stressate, esclusione immunitaria e diversità del microambiente—caratteristiche che normalmente richiedono costosi test molecolari. Pur essendo il lavoro attuale retrospettivo e richiedendo validazione prospettica, indica un futuro in cui una scansione e un vetrino standard possono segnalare in modo non invasivo tumori con una barriera immunitaria fibrotica ostile, guidare quali pazienti potrebbero beneficiare di test aggiuntivi o terapie mirate e farlo attraverso più tipi di cancro senza gravare ulteriormente sui pazienti.
Citazione: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Parole chiave: microambiente tumorale, imaging oncologico, intelligenza artificiale, fibroblasti, immunoterapia