Clear Sky Science · it
Autoencoding mascherato, preaddestramento generalizzabile e esperti integrati per una segmentazione dei gliomi migliorata
Perché scansioni più intelligenti sono importanti per i tumori cerebrali
I tumori cerebrali chiamati gliomi sono tra i più letali, eppure i medici passano ancora molto tempo a tracciare manualmente i confini dei tumori sulle risonanze magnetiche. Questo accurato contorno guida la chirurgia e la radioterapia, ma può richiedere 15–20 minuti per paziente e deve essere ripetuto nel tempo. Lo studio presenta MAGPIE, un sistema di intelligenza artificiale che impara da decine di migliaia di scansioni cerebrali senza etichette umane, per poi aver bisogno di solo una manciata di casi etichettati da esperti per mappare i gliomi in modo affidabile. Per i pazienti, ciò potrebbe tradursi in una pianificazione del trattamento più rapida e consistente anche in ospedali privi di grandi dataset curati.
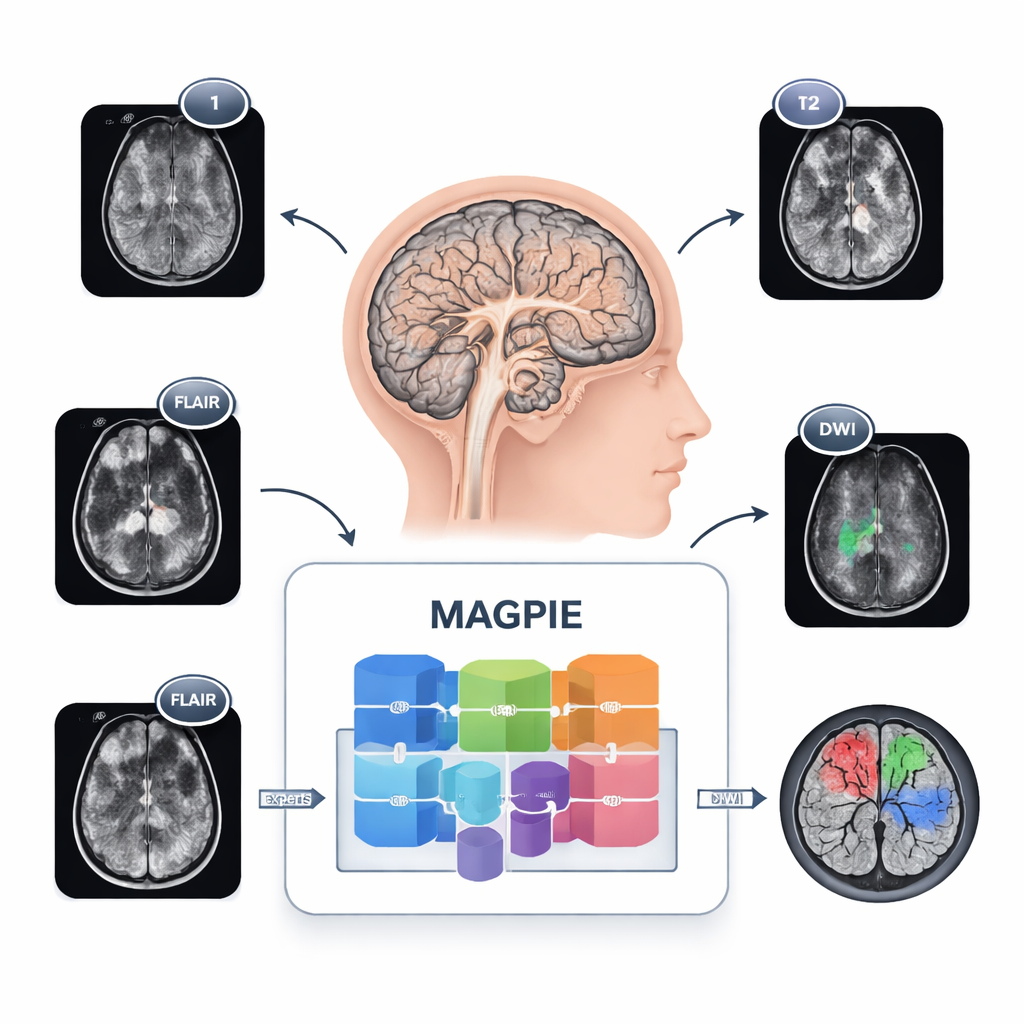
Vedere i tumori in modo nuovo
I gliomi sono difficili da mappare perché non formano masse regolari. Le cellule tumorali si diffondono lungo i collegamenti cerebrali, creando margini sfumati e piccole lesioni satellite difficili da individuare. Inoltre, diversi ospedali usano impostazioni e combinazioni di sequenze RM diverse, per cui uno strumento addestrato in un contesto può fallare in un altro. MAGPIE affronta tutto questo insieme. È stato esposto per primo a 43.505 scansioni cerebrali non etichettate tratte da molti studi e tipi di scanner. In questa fase ha appreso pattern generali di tessuto cerebrale sano e patologico cercando di ricostruire parti mancanti delle immagini e confrontando diverse viste aumentate dello stesso cervello, costringendolo a concentrarsi su caratteristiche stabili e significative piuttosto che su dettagli fragili dei pixel.
Lasciare che più esperti condividano il lavoro
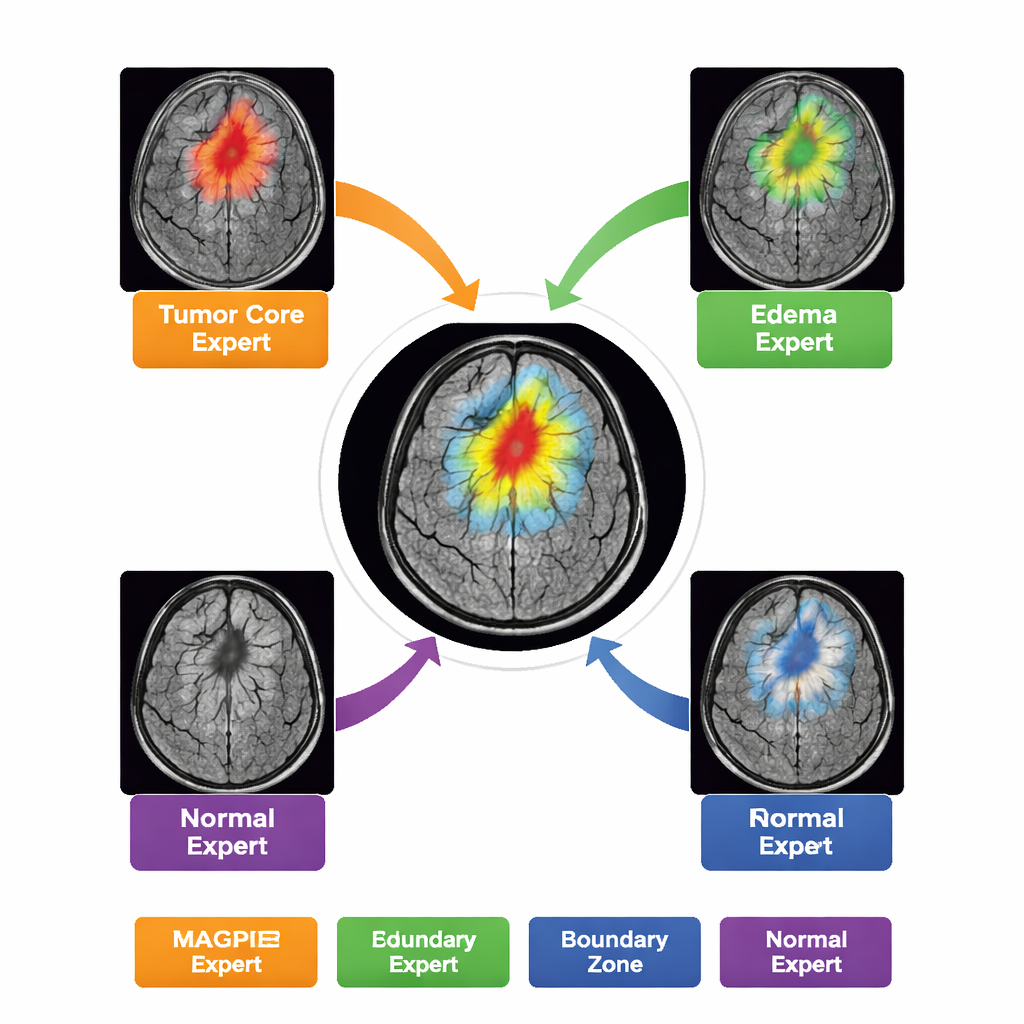
Invece di comportarsi come un unico modello monolitico, MAGPIE contiene una “miscela di esperti” al suo interno. Quando analizza una nuova scansione, attiva solo un piccolo sottoinsieme di otto sotto-reti specializzate per ciascuna regione dell’immagine. Durante l’addestramento questi esperti si dividono naturalmente il compito: alcuni diventano sensibili al bordo brillante e attivamente in crescita del tumore; altri si concentrano sul nucleo necrotico; altri ancora imparano l’anello sfumato dell’edema attorno al tumore; e alcuni si occupano principalmente del tessuto cerebrale sano e dei confini. Gli autori mostrano questo misurando quanto fortemente l’attività di ciascun esperto si sovrappone alle diverse zone tumorali tracciate dai radiologi. Questa divisione del lavoro migliora l’accuratezza mantenendo la computazione gestibile—solo circa la metà dei parametri del modello è attiva per ogni patch analizzata.
Gestire scansioni del mondo reale, disordinate
I protocolli clinici di RM sono tutt’altro che uniformi. Alcuni pazienti hanno quattro sequenze, altri meno; macchine di produttori diversi producono immagini leggermente differenti. Il design di MAGPIE tratta ogni sequenza RM come un “token” separato e impara quanto peso assegnare a ciascuno in tempo reale, invece di aspettarsi un set fisso di input in un ordine fisso. Questo approccio agnostico rispetto ai canali permette al sistema di adattarsi se, per esempio, manca una sequenza con mezzo di contrasto ma è presente la FLAIR. Il modello usa anche meccanismi di attenzione avanzati che gli consentono sia di “vedere lontano”, catturando la diffusione a lunga distanza lungo le fibre della sostanza bianca, sia di “vedere con precisione”, individuando lesioni molto piccole di pochi millimetri.
Fare di più con molte meno etichette
Dopo il preaddestramento, i ricercatori hanno affinato MAGPIE su appena 20 casi di glioma completamente etichettati e lo hanno confrontato con modelli standard addestrati da zero nelle stesse condizioni. Su un importante benchmark per i tumori cerebrali (BraTS21), MAGPIE ha raggiunto un punteggio Dice—una misura comune di sovrapposizione in imaging medico—di circa il 61%, superando la migliore versione addestrata da zero di circa 2,6 punti percentuali e sovraperformando un forte metodo auto-supervisionato precedente senza mostrare alcun “trasferimento negativo” dannoso. Su dati difficili fuori distribuzione—scansioni provenienti da malattie, tipi di scanner e impostazioni d’immagine diverse—si è comportato meglio, raggiungendo oltre il 70% di Dice su un dataset di lesioni della sostanza bianca senza ulteriore messa a punto. Crucialmente, questo livello di prestazioni normalmente richiede dell’ordine di 400 casi etichettati; MAGPIE lo ottiene con solo circa il 5% di quello sforzo.
Cosa potrebbe significare per pazienti e strutture
Per i non esperti, il messaggio centrale è che MAGPIE trasforma una montagna di scansioni RM non etichettate in un assistente potente che richiede pochissimo addestramento di esperti per diventare utile clinicamente. Può delineare tumori cerebrali complessi con confini realistici, rilevare piccole lesioni satellite che altri sistemi perdono e continuare a funzionare in modo affidabile quando le scansioni provengono da macchine sconosciute o mancano di certe sequenze. Questa combinazione potrebbe ridurre del circa 95% il tempo di annotazione dei radiologi, abbassare la barriera per gli ospedali più piccoli nell’adozione di IA avanzata per l’imaging e supportare una pianificazione chirurgica e radioterapica più precisa. Sebbene siano necessari ulteriori studi di validazione su tipi di tumore rari e casi a basso grado, questo lavoro mostra come un apprendimento auto-supervisionato progettato con cura possa avvicinare la segmentazione dei tumori cerebrali, robusta ed efficiente dal punto di vista dei dati, alla pratica clinica quotidiana.
Citazione: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Parole chiave: segmentazione dei gliomi, risonanza magnetica cerebrale, apprendimento auto-supervisionato, miscela di esperti, IA per imaging medico