Clear Sky Science · it
Modelli guidati clinicamente o modelli di base? predire la mielopatia spondilotica cervicale dai fascicoli sanitari elettronici
Perché è importante individuare prima questo problema spinale
La mielopatia spondilotica cervicale (MSC) ha un nome complicato, ma per molti anziani rappresenta una minaccia silenziosa al midollo spinale. Può iniziare con goffaggine, una camminata trascinata o problemi alla toilette e progredire gradualmente fino a una disabilità grave o anche alla paralisi. I medici spesso la trascurano per anni perché i segni sono sfumati e assomigliano a disturbi più comuni come l’artrosi o la sindrome del tunnel carpale. Questo studio pone una domanda attuale: i modelli nascosti nei fascicoli sanitari elettronici possono segnalare persone a rischio di MSC anni prima della diagnosi formale, e quale tipo di intelligenza artificiale (IA) è più adatta al compito?
Una condizione nascosta in una popolazione che invecchia
La MSC si verifica quando l’usura legata all’età restringe il canale vertebrale nel collo e comprime il midollo spinale. La condizione è comune negli anziani: le immagini del collo mostrano una compressione del midollo in circa un terzo delle persone oltre i 60 anni, e una quota consistente di esse svilupperà sintomi. Studi indicano però che i pazienti spesso aspettano da due a sei anni tra i primi segnali e la diagnosi corretta, perdendo tempo prezioso in cui un intervento chirurgico o altre terapie potrebbero prevenire danni permanenti. Con l’invecchiamento delle popolazioni e l’impegno dei medici di base in ambulatori affollati con limitata esperienza dei disturbi della colonna, cresce la necessità di strumenti scalabili per cogliere precocemente la MSC.
Trasformare i fascicoli sanitari in un sistema di allerta precoce
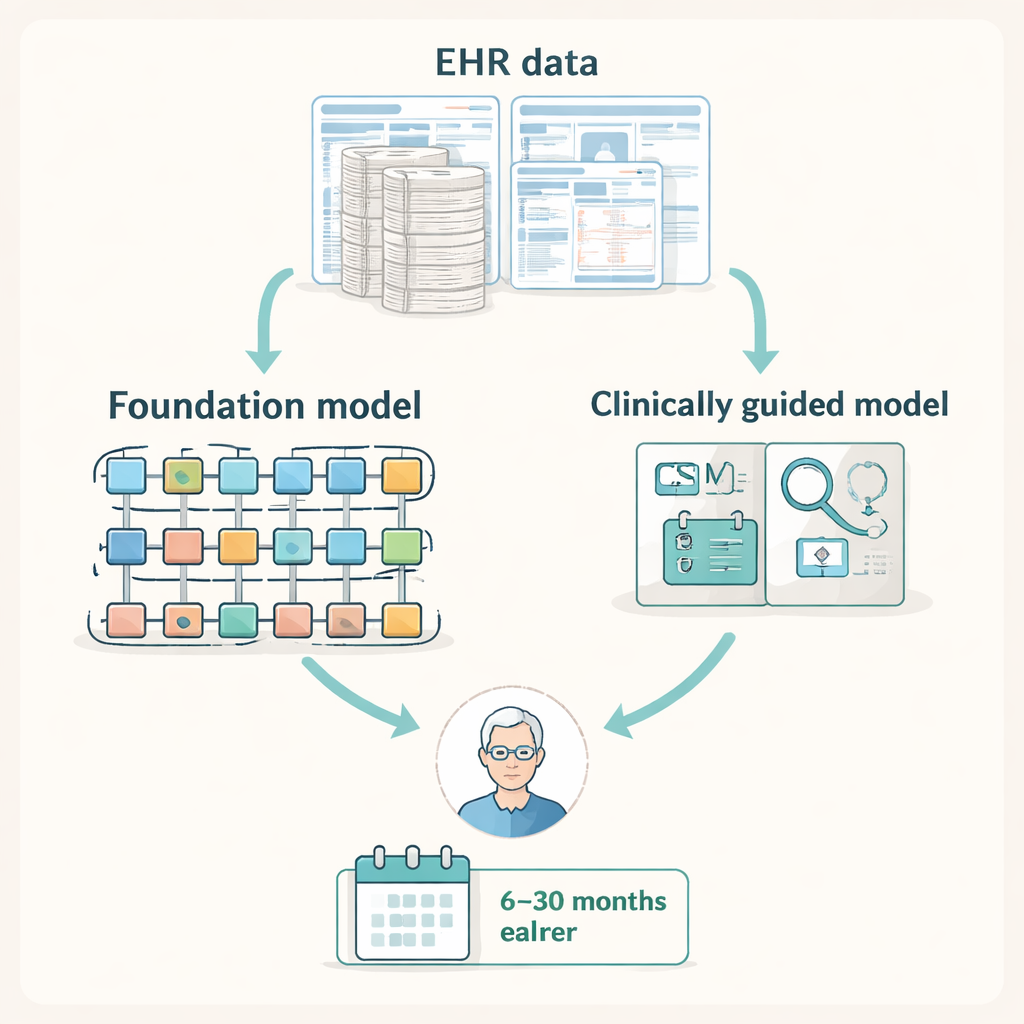
I moderni fascicoli sanitari elettronici (EHR) catturano una traccia dettagliata di diagnosi, esami di laboratorio, procedure e visite ambulatoriali. I ricercatori hanno ragionato che questa traccia probabilmente contiene indizi della MSC precoce — come cadute ripetute, esami neurologici o fisioterapia — molto prima che qualcuno richieda immagini specialistiche della colonna. Hanno raccolto dati di circa 2 milioni di pazienti in due grandi set di dati statunitensi: un database nazionale di richieste di rimborso assicurativo e le cartelle di un sistema sanitario regionale. All’interno di questi, hanno identificato decine di migliaia di persone che in seguito hanno ricevuto una diagnosi di MSC e le hanno abbinate a pazienti simili che non l’hanno ricevuta, creando un grande banco di prova per verificare se l’IA potesse prevedere chi sarebbe stato diagnosticato con MSC in finestre di previsione che andavano da 6 a 30 mesi prima.
IA generica e potente contro strumenti snelli e guidati clinicamente
Il team ha confrontato diversi tipi di modelli di machine learning che elaborano dati EHR. Da un lato c’erano i grandi “modelli di base” — potenti sistemi basati su transformer originariamente addestrati su milioni di cartelle per apprendere pattern generali nei dati sanitari. Dall’altro c’erano modelli più piccoli costruiti solo su una lista concisa di 497 codici di diagnosi, procedure e farmaci selezionati manualmente da specialisti della colonna come altamente rilevanti per la MSC. I ricercatori hanno valutato le prestazioni usando statistiche adatte a malattie rare, chiedendosi quanto ogni modello fosse migliore del caso nel identificare i pazienti che in seguito avrebbero sviluppato MSC attraverso diverse finestre temporali di previsione.
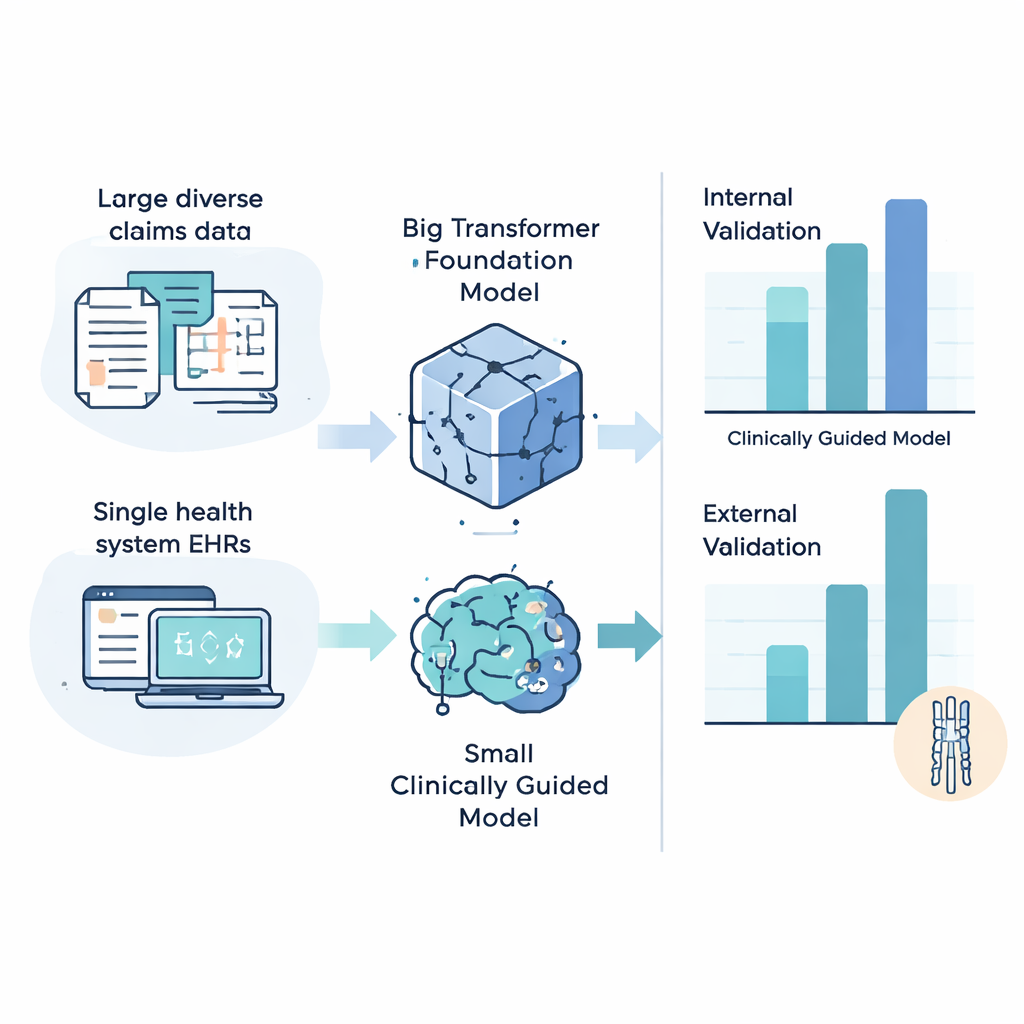
Accuratezza locale, affidabilità in trasferimento
Quando i modelli sono stati addestrati e testati all’interno dello stesso ampio e diversificato dataset assicurativo, il più grande modello di base in genere ha dato le migliori prestazioni, raggiungendo fino a sei-sette volte l’accuratezza di un classificatore non informativo. Tuttavia il quadro è cambiato quando i modelli sono stati valutati sul sistema sanitario indipendente. Qui, i modelli più semplici e guidati clinicamente hanno generalmente superato i complessi transformer e, in alcuni casi, hanno raggiunto prestazioni fino a 13 volte migliori rispetto al caso nel predire quali pazienti avrebbero presto ricevuto una diagnosi di MSC. Un esperimento inverso — addestrare sul singolo sistema sanitario e testare sul dataset nazionale — ha raccontato una storia simile: i modelli più piccoli e focalizzati clinicamente tendevano a trasferirsi meglio tra le istituzioni. Analisi per sottogruppi hanno inoltre rivelato che tutti i modelli funzionavano meglio per i pazienti con visite sanitarie più frequenti, sollevando interrogativi di equità per chi si rivolge meno spesso ai medici.
Cosa significa per pazienti e medici
I risultati suggeriscono che l’IA potrebbe aiutare a segnalare persone ad alto rischio di MSC fino a due anni e mezzo prima della diagnosi, indirizzando potenzialmente i clinici verso esami neurologici e imaging spinale più tempestivi. Lo studio mette però in luce anche un compromesso: mentre i grandi modelli sofisticati possono eccellere sui dati su cui sono stati addestrati, modelli più piccoli, progettati con cura e radicati nell’esperienza clinica possono risultare più affidabili quando vengono spostati in nuovi ospedali e popolazioni di pazienti. Per i pazienti, la conclusione è di speranza ma sfumata: l’uso intelligente dei dati sanitari di routine potrebbe abbreviare la lunga odissea diagnostica che molti con MSC affrontano, ma il successo dipenderà non solo da algoritmi potenti, bensì anche da progettazione attenta dei modelli, test rigorosi in contesti diversi e attenzione all’equità affinché i benefici della rilevazione precoce siano condivisi ampiamente.
Citazione: Yakdan, S., Warner, B., Ghogawala, Z. et al. Clinically-guided models or foundation models? predicting cervical spondylotic myelopathy from electronic health records. npj Digit. Med. 9, 153 (2026). https://doi.org/10.1038/s41746-026-02337-7
Parole chiave: mielopatia spondilotica cervicale, fascicoli sanitari elettronici, apprendimento automatico, modelli di base, diagnosi precoce