Clear Sky Science · it
La caratterizzazione quantitativa di HER2 nei tessuti e nel plasma predice l’attività del trastuzumab deruxtecan nel carcinoma mammario
Perché questa ricerca è importante per i pazienti
Per le persone con carcinoma mammario metastatico, nuovi farmaci possono offrire speranza, ma non funzionano allo stesso modo per tutti. Questo studio pone una domanda pratica: possiamo prevedere meglio chi trarrà il massimo e il più duraturo beneficio da un farmaco mirato ampiamente usato chiamato trastuzumab deruxtecan (spesso abbreviato in T-DXd)? Esaminando con maggiore precisione campioni tumorali e sangue, i ricercatori mostrano che misure fini di una molecola chiamata HER2 — insieme ad alcuni marcatori di DNA e proteine — possono rivelare quali tumori hanno maggior probabilità di rispondere a questo trattamento.
Un farmaco mirato con risultati variabili
T-DXd è un «coniugato anticorpo‑farmaco», una specie di missile guidato che cerca le cellule che esprimono la proteina HER2 e rilascia al loro interno un carico simile a una chemioterapia. Inizialmente usato per tumori con livelli molto alti di HER2, è ora approvato per quasi nove pazienti su dieci con carcinoma mammario metastatico, compresi quelli con HER2 bassa o addirittura assente secondo i test standard. Tuttavia, nella pratica quotidiana alcuni pazienti godono di lunghi periodi di controllo della malattia con T-DXd, mentre altri vedono la progressione dopo pochi mesi. I metodi di laboratorio tradizionali, che classificano i tumori in categorie HER2-positiva, HER2-bassa o HER2-zero, hanno spiegato poco queste differenze.
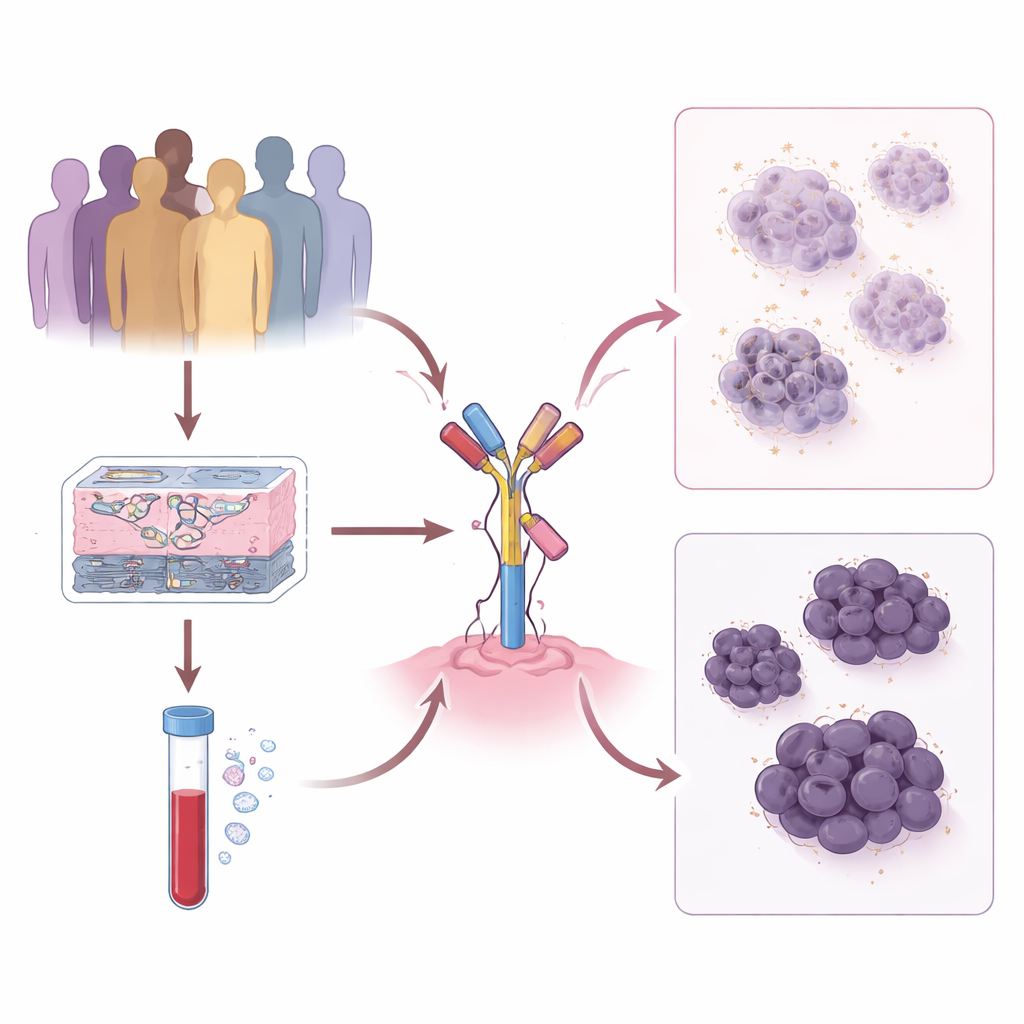
Seguire le variazioni del tumore nel tempo
Il gruppo ha studiato 191 pazienti trattati con T-DXd in due grandi centri oncologici statunitensi, rivedendo il comportamento delle loro neoplasie e come i livelli di HER2 cambiavano dal tumore primario alle metastasi successive. Hanno rilevato che una classificazione unica e puntuale del tumore come HER2‑basso o HER2‑zero perde dinamiche importanti. I pazienti i cui tumori restavano chiaramente HER2‑positivi hanno avuto la maggiore sopravvivenza con T-DXd, seguiti da quelli con tumori che mostravano costantemente livelli bassi ma stabili di HER2. Al contrario, quando HER2 oscillava tra basso e zero nel tempo, il beneficio da T-DXd risultava significativamente più breve. Questi schemi suggeriscono che più stabile è la dipendenza del tumore da HER2, migliore può essere l’efficacia del farmaco.
Misurare HER2 con un metro più fine
Per andare oltre categorie grossolane, i ricercatori hanno applicato una serie di test moderni al tessuto tumorale. Uno ha impiegato l’immunofluorescenza quantitativa per contare con precisione la proteina HER2; un altro ha utilizzato una piattaforma proteica ad alto rendimento; un terzo ha letto profili di espressione genica correlati alla regione genomica di HER2. In tutti e tre i casi il messaggio è stato coerente: livelli quantitativi più elevati di HER2 — misurati come proteina sulla superficie cellulare, forme attivate (fosforilate) o RNA messaggero — erano associati a un intervallo più lungo prima della necessità del trattamento successivo e a una migliore sopravvivenza globale con T-DXd. Negli stessi pazienti, la lettura patologica convenzionale (HER2‑positiva, bassa o zero) distingueva a malapena gli esiti, sottolineando che «quanto» HER2 è presente conta più di quale casella di spunta venga selezionata.
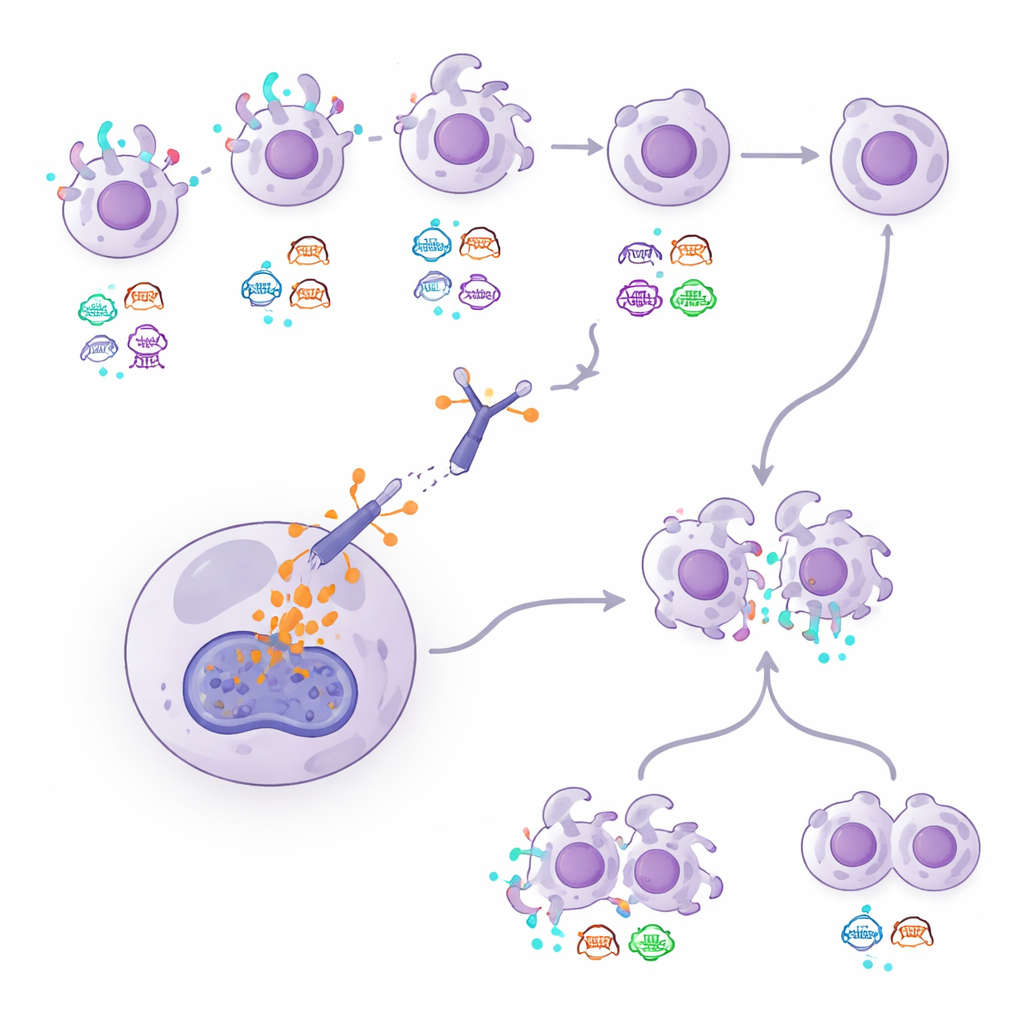
Indizi dai test del sangue e altri marcatori tumorali
Poiché le biopsie ripetute possono essere invasive, lo studio ha testato anche un approccio basato sul sangue che analizza frammenti di DNA tumorale circolante nel torrente ematico. Usando un metodo chiamato DNADX, gli investigatori hanno raggruppato i campioni ematici dei pazienti in cluster biologici e calcolato una firma di DNA correlata a HER2. I pazienti il cui sangue mostrava segnali HER2 più forti tendevano a rimanere più a lungo in trattamento con T-DXd, mentre quelli con pattern di DNA associati a malattie più aggressive e a rapida crescita andavano peggio. I ricercatori hanno inoltre osservato che, nei tumori classificati come HER2‑negativi, alti livelli di una proteina chiamata topoisomerasi 1 all’interno delle cellule tumorali erano collegati a risultati peggiori, suggerendo che il modo in cui la cellula gestisce il carico del farmaco può influenzarne il successo. Alcune perdite o mutazioni geniche, come alterazioni in ERBB2 e TP53 e un arricchimento di mutazioni in ARID1B dopo il trattamento, sono emerse come possibili marcatori di resistenza.
Cosa significa per pazienti e clinici
Nel complesso lo studio mostra che T-DXd è un trattamento efficace nel mondo reale, soprattutto per i pazienti i cui tumori sono fortemente e costantemente guidati da HER2. Ma mette anche in evidenza che il test tradizionale per HER2 è uno strumento troppo rozzo per guidare l’uso di questo potente farmaco. Utilizzando misure più sensibili su tessuto e sangue, i medici potrebbero in futuro individuare con maggiore precisione i pazienti più propensi a beneficiare di T-DXd, risparmiare ad altri terapie inefficaci e pianificare meglio l’ordine in cui impiegare diversi coniugati anticorpo‑farmaco. Sebbene questi test avanzati non siano ancora di routine e richiedano convalida su gruppi più ampi, indicano una direzione verso un futuro in cui le scelte terapeutiche per il carcinoma mammario metastatico saranno basate su ritratti molecolari dettagliati, non solo su etichette generali.
Citazione: Tarantino, P., Kim, SE., Hughes, M.E. et al. Quantitative HER2 tissue and plasma profiling predicts the activity of trastuzumab deruxtecan for breast cancer. npj Precis. Onc. 10, 141 (2026). https://doi.org/10.1038/s41698-026-01365-6
Parole chiave: Test HER2, trastuzumab deruxtecan, carcinoma mammario metastatico, biopsia liquida, coniugati anticorpo-farmaco