Clear Sky Science · it
La risposta a midostaurin in LMA è plasmata da uno stato cellulare di tipo progenitore selettivamente bersagliato da mimetici SMAC
Perché alcuni farmaci per la leucemia smettono di funzionare
Per molte persone affette da un tipo di tumore del sangue chiamato leucemia mieloide acuta (LMA), i nuovi farmaci mirati hanno portato speranza—ma non tutti ne beneficiano e le risposte spesso svaniscono. Questo studio pone una domanda semplice ma cruciale: perché alcune cellule leucemiche ignorano un farmaco ampiamente usato, midostaurin, e possiamo trovare una combinazione intelligente che costringa queste cellule ostinate a morire?
Guardare oltre la mutazione principale
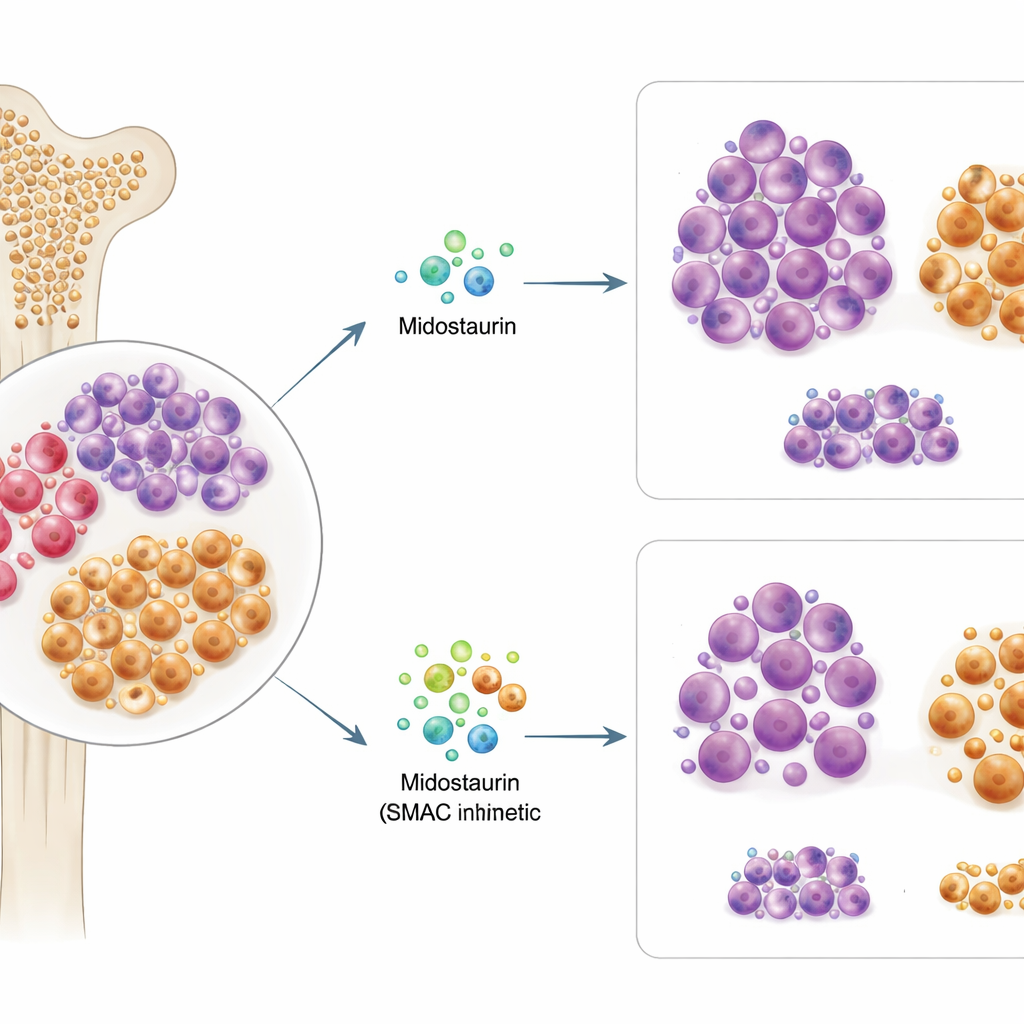
Circa un paziente su tre con LMA porta una variazione in un gene chiamato FLT3, che guida la crescita della leucemia ed è il motivo per cui viene prescritto midostaurin. I ricercatori hanno esaminato campioni di midollo osseo e sangue di 63 pazienti con LMA portatrice di FLT3 mutato, esponendo le cellule a midostaurin e a oltre 500 altri farmaci antitumorali in laboratorio. Hanno scoperto che la sensibilità delle cellule di un paziente a midostaurin ex vivo corrispondeva strettamente alla risposta clinica successiva di quel paziente. Sorprendentemente, il tipo esatto di mutazione FLT3 o la sua abbondanza non prevedevano in modo affidabile il successo di midostaurin, suggerendo che la sola genetica non può spiegare chi trae beneficio.
Un serbatoio nascosto di cellule “seme” ostinate
Approfondendo, il team ha confrontato i modelli complessivi di proteine e attività genica tra cellule sensibili a midostaurin e quelle non sensibili. I campioni non rispondenti erano arricchiti di caratteristiche di cellule progenitrici immature, di tipo staminale—cellule più vicine alla radice della formazione del sangue e ritenute agire come “semi” che possono riavviare la leucemia. Al contrario, i campioni rispondenti apparivano più simili a cellule immunitarie e mieloidi parzialmente maturate. Utilizzando avanzati metodi a singola cellula, gli scienziati hanno identificato una popolazione specifica di cellule leucemiche marcata dalle proteine di superficie CD38 e CD45RA che si comportava come questi progenitori-seme. Queste cellule mostravano un'organizzazione insolita della membrana esterna, suggerendo che molecole di segnalazione chiave erano disposte in modi favorevoli alla sopravvivenza.
Cablatura della sopravvivenza: uno switch delle vie di segnalazione
Midostaurin è progettato per bloccare la segnalazione FLT3, che normalmente alimenta una catena di segnali che include una molecola chiamata STAT5 e può guidare la crescita cellulare. Quando il team ha esaminato la segnalazione in linee cellulari e campioni di pazienti dopo il trattamento con midostaurin, hanno osservato due modelli distinti. Nelle cellule sensibili a midostaurin, l'attività di STAT5 è diminuita rapidamente, coerentemente con un efficace spegnimento di FLT3. Nelle cellule resistenti, tuttavia, ha dominato un'altra via: PI3K/AKT, una classica strada di sopravvivenza che aiuta le cellule a opporsi alla morte. Queste cellule resistenti mantenevano o addirittura aumentavano l'attività di AKT dopo il trattamento e mostravano livelli maggiori di proteine che bloccano l'apoptosi (morte cellulare programmata). In altre parole, il cablaggio interno di queste cellule di tipo progenitore sembrava riallineato per favorire la sopravvivenza anche quando FLT3 era inibito.
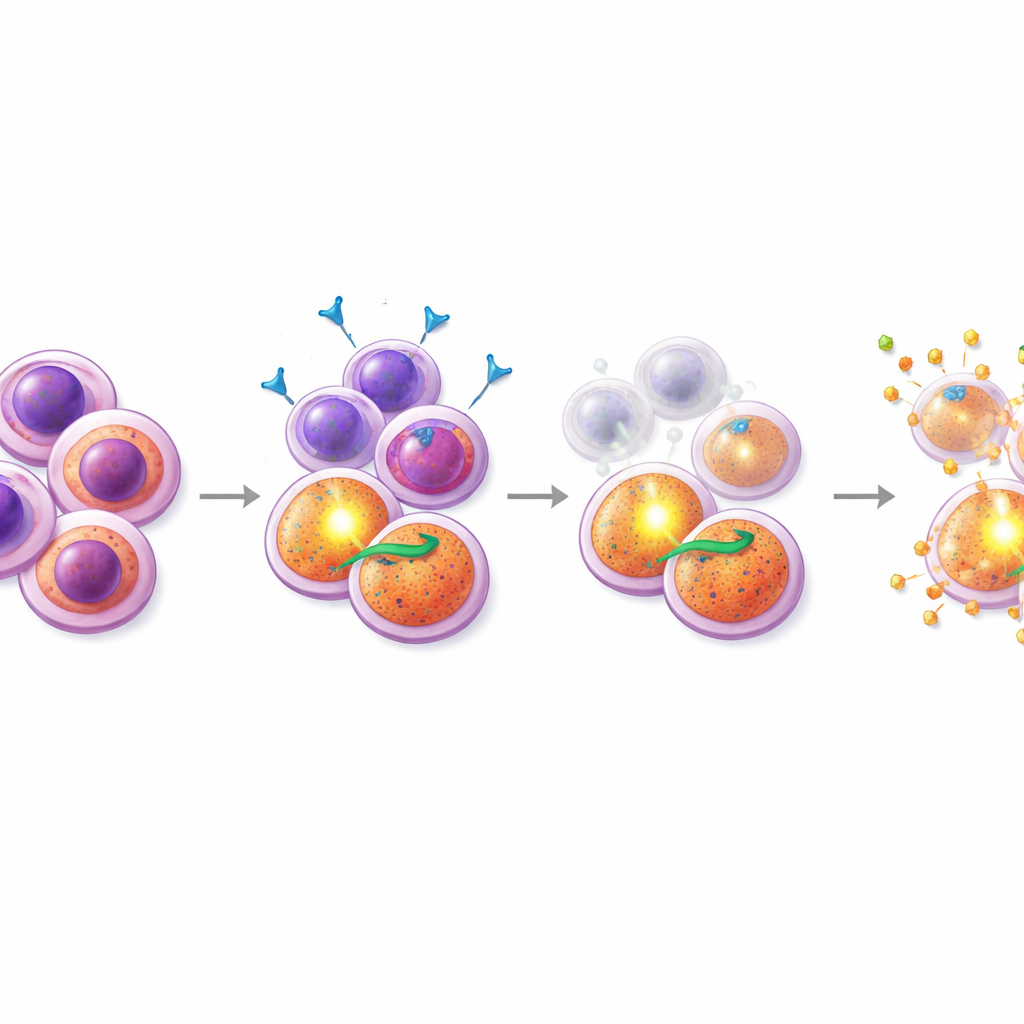
Trovare un farmaco partner che colpisca il punto debole
Con questa intuizione, i ricercatori hanno testato combinazioni di midostaurin con centinaia di altri composti, concentrandosi su farmaci che influenzano la morte cellulare. Un gruppo che ha spiccato è stato quello dei mimetici SMAC, farmaci che disabilitano le proteine “inibitori dell'apoptosi” su cui fanno affidamento le cellule guidate da PI3K/AKT. In campioni di pazienti resistenti e in una linea cellulare resistente con mutazione FLT3, l'aggiunta di mimetici SMAC come birinapant a midostaurin ha prodotto una forte sinergia: insieme, i farmaci hanno ucciso molte più cellule rispetto a ciascuno da solo. Crucialmente, esperimenti dettagliati di citometria a flusso hanno mostrato che la combinazione midostaurin–mimetico SMAC ha deplezionato selettivamente la popolazione progenitrice CD38+CD45RA+ e ridotto i livelli dei suoi marcatori di superficie caratteristici, suggerendo che questa terapia prende di mira specificamente i semi difficili da eliminare. Per contro, le combinazioni con l'inibitore approvato di BCL-2, venetoclax, erano più efficaci contro un diverso sottogruppo ricco di CD34 e non mostravano lo stesso effetto mirato sulle cellule resistenti.
Cosa significa per i pazienti
Questo lavoro suggerisce che la resistenza a midostaurin non riguarda solo la mutazione FLT3 in sé, ma anche lo “stato” delle cellule leucemiche—il loro livello di maturità, l'organizzazione della membrana e le vie di sopravvivenza privilegiate. Un sottogruppo di tipo progenitore CD38+CD45RA+ sembra essere un serbatoio chiave di resistenza, spostando la segnalazione dalla via tipica STAT5 verso un programma di sopravvivenza PI3K/AKT. Accoppiando midostaurin con mimetici SMAC, i ricercatori sono riusciti a riosensibilizzare queste cellule e indurle alla morte cellulare in laboratorio. Sebbene siano necessari studi clinici più ampi, i risultati indicano un futuro in cui i medici potrebbero utilizzare test funzionali e profilazione dello stato cellulare, non solo il sequenziamento del DNA, per scegliere combinazioni mirate a FLT3 che eliminino sia la massa leucemica sia i suoi semi più resistenti.
Citazione: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Parole chiave: leucemia mieloide acuta, inibitori di FLT3, resistenza ai farmaci, cellule staminali leucemiche, mimetici SMAC