Clear Sky Science · it
Fibroblasti associati al cancro con alto livello di COL3A1 orchestrano microambienti metabolici e immunitari per conferire chemioresistenza nel carcinoma mammario
Perché alcuni tumori al seno ignorano la chemioterapia
La chemioterapia può salvare vite nel carcinoma mammario, eppure molti pazienti scoprono che i loro tumori smettono di rispondere o non rispondono bene fin dall’inizio. Questo studio guarda oltre le cellule tumorali stesse verso il quartiere in cui vivono e si chiede: quali cellule vicine aiutano i tumori a sopravvivere al trattamento e come lo fanno? La risposta si concentra su un gruppo speciale di cellule di supporto che rimodellano sia la nutrizione del tumore sia l’immunità locale per proteggere le cellule cancerose dalla chemioterapia.
Gli aiutanti nascosti intorno al tumore
I tumori mammari non sono solo cellule cancerose; sono comunità miste che includono vasi sanguigni, cellule immunitarie e cellule del tessuto connettivo chiamate fibroblasti. Quando i fibroblasti vivono in un tumore, sono noti come fibroblasti associati al cancro, o CAF, e possono sia frenare sia promuovere il cancro. Combinando diverse potenti tecniche di profilazione genetica sui campioni dei pazienti—analisi single-cell, spaziale e bulk—insieme a esperimenti in vitro e su modelli animali, i ricercatori hanno individuato un sottogruppo di CAF che produce alti livelli di una molecola chiamata COL3A1, un componente dell’impalcatura tissutale. I pazienti i cui tumori contenevano più di questi CAF ad alta espressione di COL3A1 avevano maggiori probabilità di risposte scarse alla chemioterapia e di sopravvivenza peggiore.
Una protezione a due punte: carburante e difesa
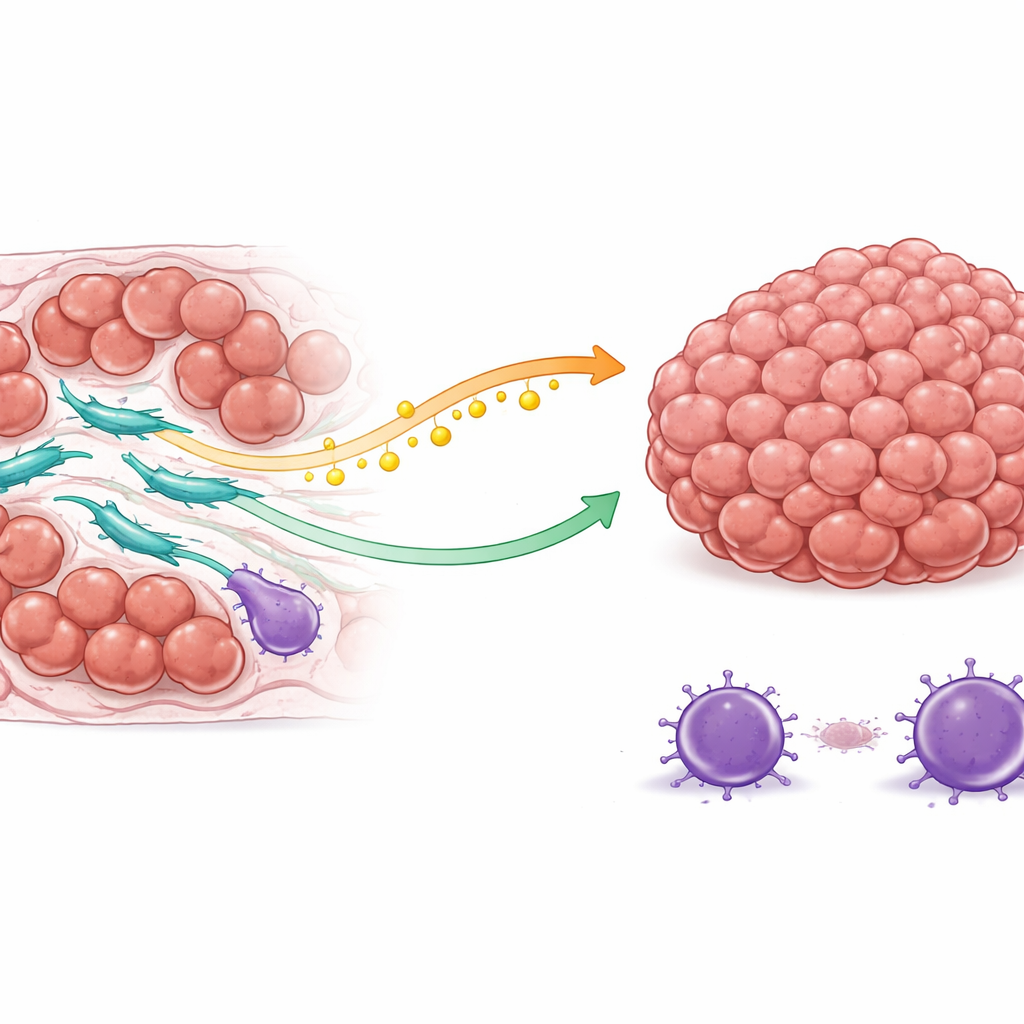
Il team ha scoperto che i CAF ad alta espressione di COL3A1 proteggono le cellule tumorali in due modi principali. Primo, modificano il modo in cui trattano i lipidi. Questi fibroblasti aumentano l’attività di un enzima che produce acido oleico, un tipo di grasso. Invece di trattenere questo combustibile, lo rilasciano nel microambiente tumorale. Le cellule tumorali assorbono questo acido oleico tramite una proteina di superficie e, in risposta, attivano una via di segnalazione intracellulare di sopravvivenza nota per aiutare le cellule a resistere ai segnali di morte. Di conseguenza, quando la chemioterapia tenta di innescare i programmi di autodistruzione nelle cellule tumorali, queste sono meglio attrezzate per opporsi e continuare a proliferare.
Plasmare un quartiere immune ostile
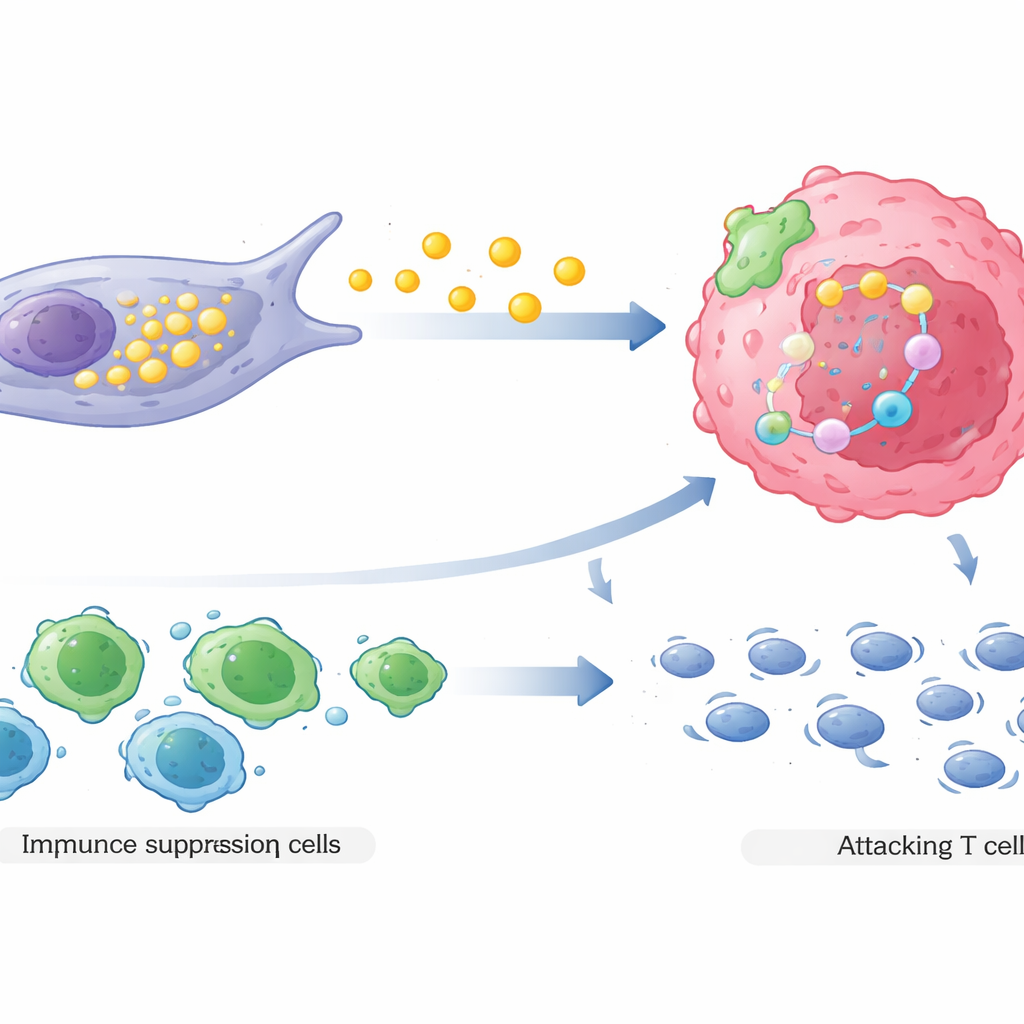
Secondo, i CAF ad alta espressione di COL3A1 rimodellano il paesaggio immunitario locale a favore del tumore. Attraverso complesse interazioni di segnalazione, attraggono cellule T regolatorie, un tipo di cellula immunitaria che attenua gli attacchi immunitari, e allo stesso tempo scoraggiano o indeboliscono le cellule T citotossiche che normalmente attaccherebbero il cancro. Il mapping spaziale di tumori di pazienti reali ha mostrato che questi fibroblasti tendono a localizzarsi vicino sia alle cellule tumorali resistenti ai farmaci sia alle cellule immunitarie soppressive, mentre le efficaci cellule T citotossiche sono spinte più lontano. Questa disposizione crea una zona riparata dove le cellule cancerose affrontano minori minacce immunitarie proprio nel momento in cui diventano anche più difficili da uccidere con i farmaci.
Prove da cellule, topi e pazienti
Per testare causa ed effetto, i ricercatori hanno ridotto COL3A1 nei CAF coltivati in laboratorio. Quando cellule di carcinoma mammario sono state coltivate insieme a questi fibroblasti alterati, hanno formato meno strutture invasive, sono state più facilmente eliminate dal farmaco chemioterapico paclitaxel e hanno mostrato maggiori segni di morte cellulare programmata. In topi impiantati con miscele di cellule tumorali mammarie e CAF, bloccare COL3A1 nei fibroblasti ha rallentato la crescita tumorale sotto chemioterapia e ridotto i livelli dell’enzima lipogenico e del recettore delle cellule tumorali associato all’acido oleico. In un gruppo di 72 pazienti trattati con chemioterapia prima dell’intervento chirurgico, livelli più alti di COL3A1 e dei suoi partner nel metabolismo lipidico corrispondevano fortemente a risposte al trattamento peggiori e a un tempo più breve prima della recidiva.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio mostra che un particolare insieme di cellule di supporto nei tumori mammari agisce come un’unità di guardie del corpo: nutrono le cellule cancerose con una dieta protettiva a base di grassi e richiamano alleati immunitari che smorzano le difese dell’organismo. Queste azioni, insieme, rendono la chemioterapia meno efficace. Misurare l’abbondanza di fibroblasti ad alta espressione di COL3A1 migliora la capacità dei medici di prevedere chi risponderà o meno al trattamento, e le vie che utilizzano—produzione di lipidi, segnali di sopravvivenza intracellulare nelle cellule tumorali e soppressione immunitaria—offrono nuovi bersagli farmacologici. In futuro, terapie che disarmano o riprogrammano questi fibroblasti potrebbero essere abbinate alla chemioterapia standard per impedire ai tumori di sviluppare resistenza.
Citazione: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Parole chiave: carcinoma mammario, chemioresistenza, microambiente tumorale, fibroblasti associati al cancro, metabolismo dei lipidi