Clear Sky Science · it
Validazione clinica di un saggio di arricchimento del metiloma genomico indipendente dal tessuto per monitorare la risposta a pembrolizumab
Monitorare il trattamento del cancro con una semplice prelievo di sangue
Le persone con tumori avanzati e i loro medici spesso devono aspettare settimane o mesi per capire se un farmaco di immunoterapia sta davvero funzionando. Le scansioni possono essere ambigue e le ripetute biopsie tissutali sono invasive o addirittura impossibili. Questo studio esplora un nuovo tipo di esame del sangue che legge piccole marcature chimiche sul DNA tumorale presente nel flusso sanguigno, offrendo un modo più rapido e meno invasivo per capire se il farmaco pembrolizumab sta facendo effetto.
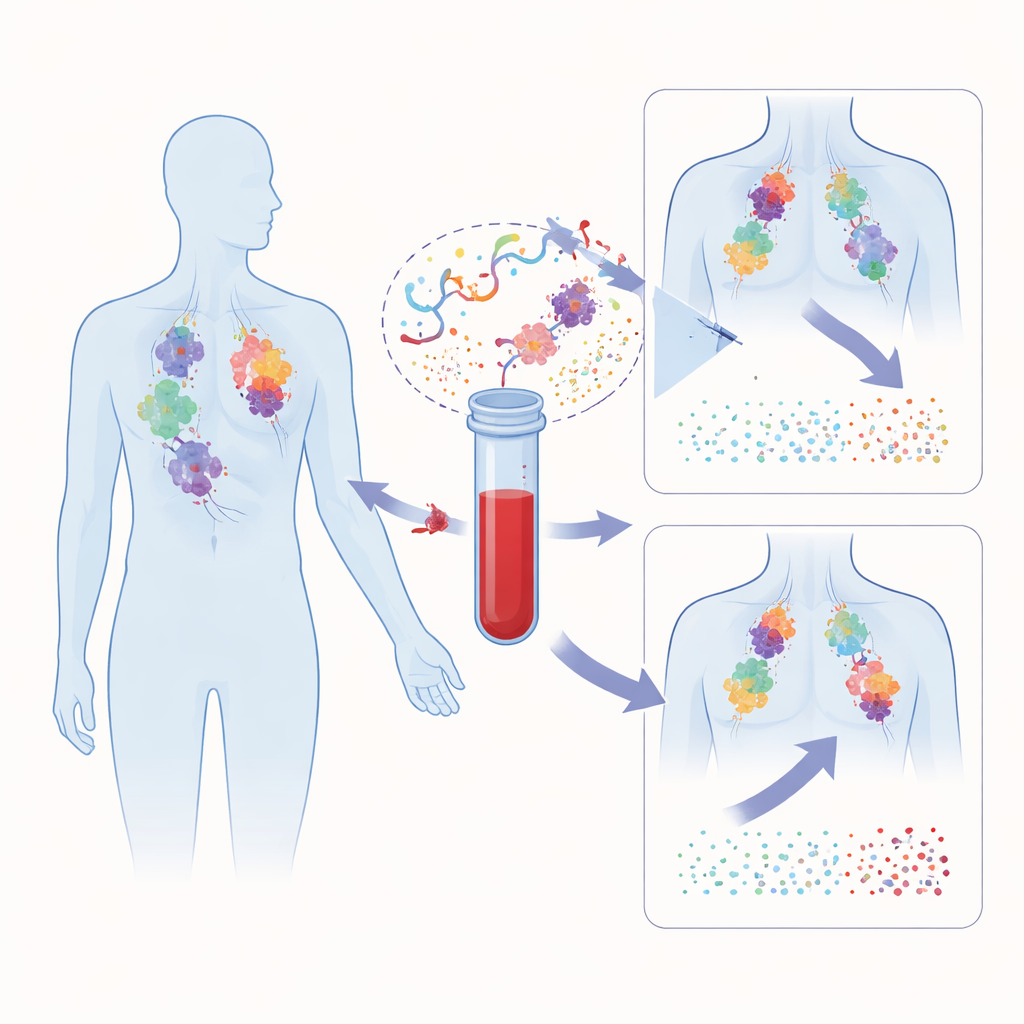
Perché i controlli attuali non sono sufficienti
I farmaci immunoterapici come il pembrolizumab possono dare risposte notevoli e durature, ma solo in una frazione dei pazienti. Oggi i clinici si basano su caratteristiche del tumore come i livelli di PD-L1 o il numero di mutazioni misurate dalle biopsie tissutali, insieme a esami di imaging periodici. Questi approcci hanno limiti importanti: i campioni di biopsia non sono sempre disponibili, possono non rappresentare l’intero tumore e di solito vengono misurati una sola volta prima dell’inizio del trattamento. L’imaging può essere fuorviante perché le cellule immunitarie che invadono il tumore possono temporaneamente farlo apparire più grande, un fenomeno noto come pseudoprogressione. Nel complesso, queste limitazioni fanno sì che i pazienti possano continuare terapie inefficaci per mesi prima che sia chiaro che non funzionano.
Un test del sangue universale invece delle biopsie tumorali
I ricercatori hanno testato un saggio “indipendente dal tessuto” che non richiede un campione preventivo del tumore del paziente. Si concentra invece sulla metilazione del DNA—marcatori chimici stabili che decorano il DNA e differiscono tra cellule sane e tumorali. I tumori rilasciano continuamente frammenti di DNA nel flusso sanguigno, creando il DNA tumorale circolante (ctDNA). Usando una tecnica chiamata cfMeDIP-seq, il gruppo arricchisce e sequenzia solo i frammenti metilati dal plasma e poi applica un classificatore addestrato su ampi set di dati tumorali e non tumorali. Questo produce un punteggio numerico di ctDNA che riflette la quantità di DNA derivato dal tumore presente nel sangue, indipendentemente dal sito d’origine del cancro nel corpo.
Monitorare la risposta a pembrolizumab in molti tipi di cancro
Per verificare se questo test potesse monitorare la risposta all’immunoterapia, gli scienziati hanno analizzato 241 campioni di sangue provenienti da 69 persone con vari tumori solidi avanzati arruolati nello studio INSPIRE. I partecipanti, che non avevano ricevuto immunoterapia in precedenza, sono stati trattati con pembrolizumab in monoterapia e hanno avuto prelievi prima del trattamento e poi ogni tre cicli, a partire circa dal terzo trattamento. La domanda principale era semplice: il punteggio di ctDNA aumenta o diminuisce dall’inizio del trattamento al terzo ciclo? I pazienti sono stati raggruppati di conseguenza e seguiti per le risposte tumorali, il tempo libero da progressione e la sopravvivenza globale.
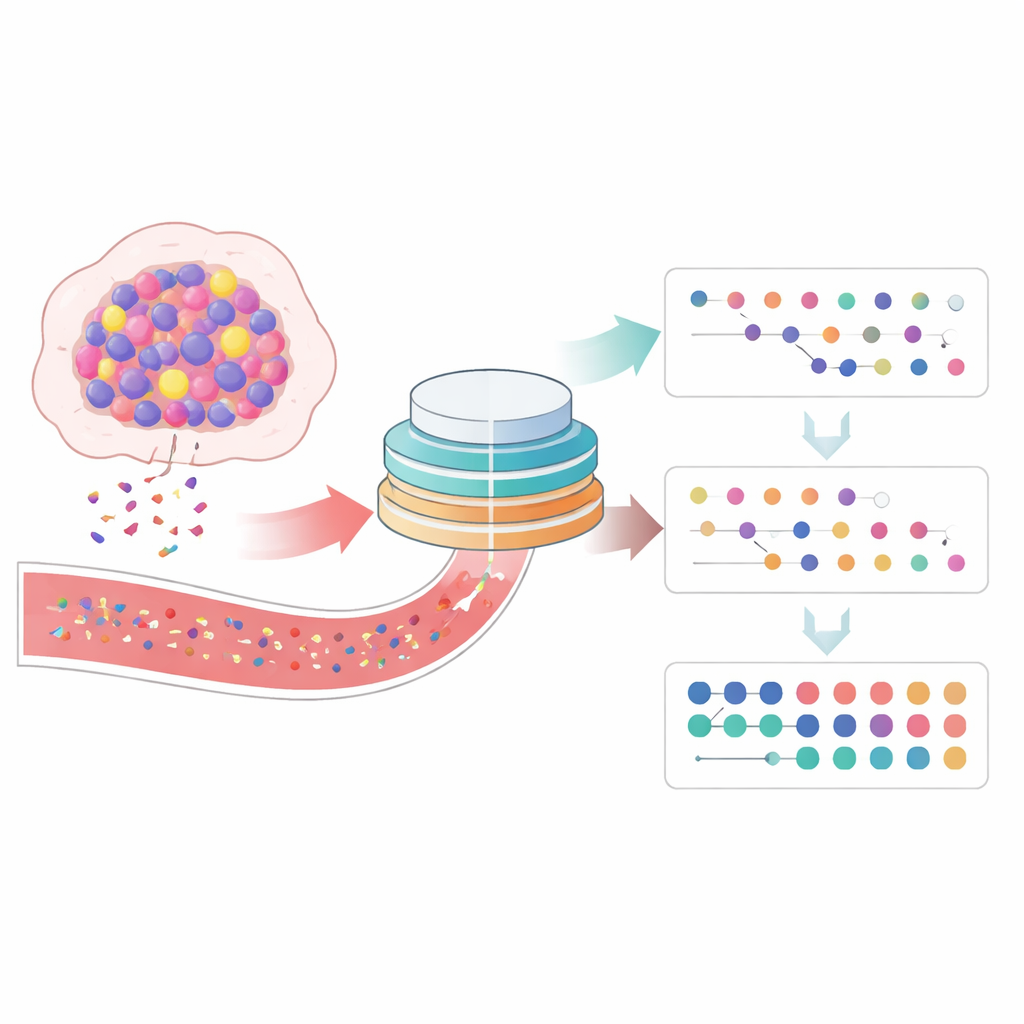
Cosa hanno rivelato i cambiamenti nel DNA tumorale
Metà dei pazienti ha mostrato una diminuzione del punteggio di ctDNA entro il terzo ciclo, e metà ha mostrato un aumento. Il modello precoce è stato impressionante: nessuno dei pazienti il cui ctDNA è aumentato ha avuto una riduzione tumorale significativa, e quasi tutti non hanno tratto beneficio dalla terapia. Al contrario, quasi tutti i pazienti che hanno risposto clinicamente hanno avuto una diminuzione del ctDNA. Un punteggio in calo è stato fortemente associato a maggiori probabilità di riduzione tumorale, periodi più lunghi prima della progressione della malattia e, nelle analisi più semplici, a una sopravvivenza globale più lunga. Quando il team ha guardato oltre quel singolo punto temporale precoce, ha scoperto che i pazienti i cui livelli di ctDNA sono rimasti sotto il valore basale iniziale per tutta la durata del trattamento tendevano a vivere più a lungo e a rimanere liberi da progressione più a lungo rispetto a coloro il cui ctDNA è salito sopra il basale in qualsiasi momento.
Come questo test si confronta con altri indicatori
Il gruppo ha anche confrontato le variazioni di ctDNA con marcatori più familiari come l’espressione di PD-L1 e il carico mutazionale tumorale misurati sul tessuto. Sebbene livelli più alti di PD-L1 mostrassero qualche correlazione con il beneficio nelle analisi di base, questi marcatori tissutali perdevano significatività una volta che le dinamiche del ctDNA venivano incluse in modelli più complessi. Al contrario, i cambiamenti precoci del ctDNA restavano un indicatore forte e indipendente di come i pazienti avrebbero avuto esito, in particolare per la sopravvivenza libera da progressione. È importante notare che questa performance era paragonabile a quella ottenuta in precedenza con test di ctDNA personalizzati e informati dal tumore che richiedono il sequenziamento preventivo del tumore di ogni paziente—eppure il nuovo saggio funziona solo dal sangue e può essere applicato a molti tipi di cancro.
Cosa potrebbe significare per i pazienti
In termini pratici, questo studio suggerisce che un test del sangue specializzato può dire, entro poche linee di trattamento, se il pembrolizumab è probabilmente efficace contro il cancro di un paziente. Una diminuzione coerente del DNA tumorale nel sangue segnala una maggiore probabilità di beneficio, mentre livelli in aumento avvertono che la malattia potrebbe resistere alla terapia. Poiché il metodo non dipende dalla disponibilità di tessuto tumorale e può essere ripetuto nel tempo, potrebbe permettere ai medici di prendere decisioni prima e meglio informate sul continuare, modificare o intensificare il trattamento. Saranno necessari studi prospettici più ampi, ma questo lavoro fornisce solide prove che la lettura dei pattern di metilazione nel DNA tumorale circolante potrebbe diventare uno strumento potente e ampiamente utilizzabile per guidare l’immunoterapia.
Citazione: Stutheit-Zhao, E.Y., Zhong, Y., Melton, C.A. et al. Clinical validation of a tissue-agnostic genome-wide methylome enrichment assay to monitor response to pembrolizumab. npj Precis. Onc. 10, 129 (2026). https://doi.org/10.1038/s41698-026-01327-y
Parole chiave: DNA tumorale circolante, monitoraggio dell’immunoterapia, biopsia liquida, metilazione del DNA, pembrolizumab