Clear Sky Science · it
Prevedere la carenza di ricombinazione omologa e le risposte al trattamento usando un modello di riferimento basato su tomografia computerizzata: uno studio preclinico
Perché questo conta per pazienti e medici
I trattamenti oncologici che danneggiano il DNA, come alcune chemioterapie e nuovi farmaci mirati, possono funzionare in modo particolarmente efficace su tumori i cui sistemi di riparazione sono già compromessi. La sfida è individuare quali tumori presentano queste debolezze nascoste senza ricorrere a biopsie invasive e ripetute. Questo studio esplora se esami di imaging routinari eseguiti su topo, interpretati da un potente modello di intelligenza artificiale, possano rivelare quanto un tumore sia vulnerabile e quanto bene risponderà a un nuovo farmaco sperimentale.
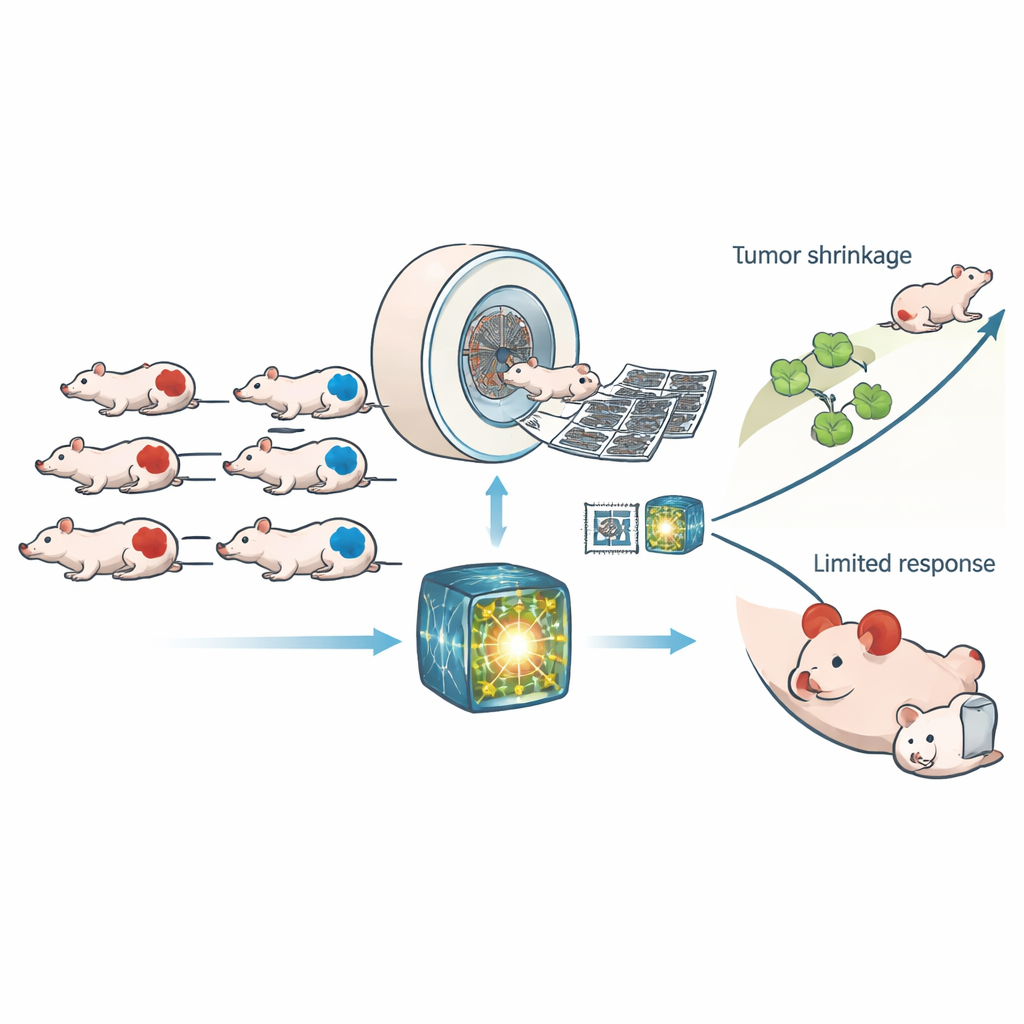
Un punto debole nascosto nelle cellule tumorali
Molti tumori presentano difetti in una via chiave di riparazione del DNA chiamata ricombinazione omologa. Quando questa via fallisce, le cellule accumulano danni nel materiale genetico, una condizione nota come carenza di ricombinazione omologa, o HRD. L’HRD può rendere i tumori più propensi a formarsi, ma al contempo costituisce un tallone d’Achille: farmaci che infliggono ulteriore danno al DNA possono spingere queste cellule già stressate oltre il limite, uccidendole più efficacemente rispetto alle cellule sane. Oggi, l’identificazione di HRD si basa di solito su test genetici o saggi di laboratorio specializzati che sono costosi, richiedono tempo e spesso necessitano di prelevare porzioni del tumore. Gli autori si sono chiesti se l’imaging — lo stesso tipo di scansioni tridimensionali a raggi X ampiamente usate in clinica — potesse offrire una finestra rapida e non invasiva sull’HRD.
Usare scansioni intelligenti invece di più biopsie
I ricercatori hanno lavorato con 307 topi portatori di innesti tumorali umani che erano o HRD o normali nella loro capacità di riparazione. Tutti gli animali sono stati sottoposti a tomografia computerizzata (TC) ad alta risoluzione prima e dopo aver ricevuto o un trattamento di controllo o CP‑506, un farmaco sperimentale che si attiva in regioni a basso ossigeno del tumore e forma legami incrociati nel DNA. Piuttosto che affidarsi a una manciata di misurazioni di immagine artigianali, il gruppo ha usato un moderno “modello di riferimento” addestrato su ampi dataset di TC umane per estrarre migliaia di pattern sottili da ogni scansione. Un semplice classificatore è stato quindi addestrato su questi pattern per decidere se un tumore fosse HRD, e le stesse caratteristiche apprese sono state riutilizzate per prevedere quanto danno al DNA e ritardo di crescita avrebbe indotto il CP‑506.
Quanto bene il modello di imaging ha svolto il compito
Il modello di riferimento ha chiaramente superato sia la radiomica tradizionale sia una rete profonda standard addestrata da zero. Su nuove scansioni di test, ha distinto tumori HRD da non-HRD con un’area sotto la curva di circa 0,88, un livello di accuratezza che si è mantenuto attraverso diverse impostazioni energetiche della TC. Quando entrambi gli approcci di IA erano d’accordo sul tipo di tumore, le prestazioni miglioravano ulteriormente. Il punteggio di HRD basato sull’immagine si è allineato strettamente con lo stato genetico reale in diverse linee tumorali di prostata e colon-retto, sebbene una linea con un comportamento di riparazione insolito sia rimasta più difficile da classificare. È importante sottolineare che le caratteristiche TC associate all’HRD non erano soltanto artefatti statistici: hanno anche previsto quanto danno al DNA persistente il CP‑506 producesse 48 ore dopo il trattamento e quanto tempo impiegassero i tumori a ricrescere fino a quattro volte la dimensione in un esperimento parallelo.
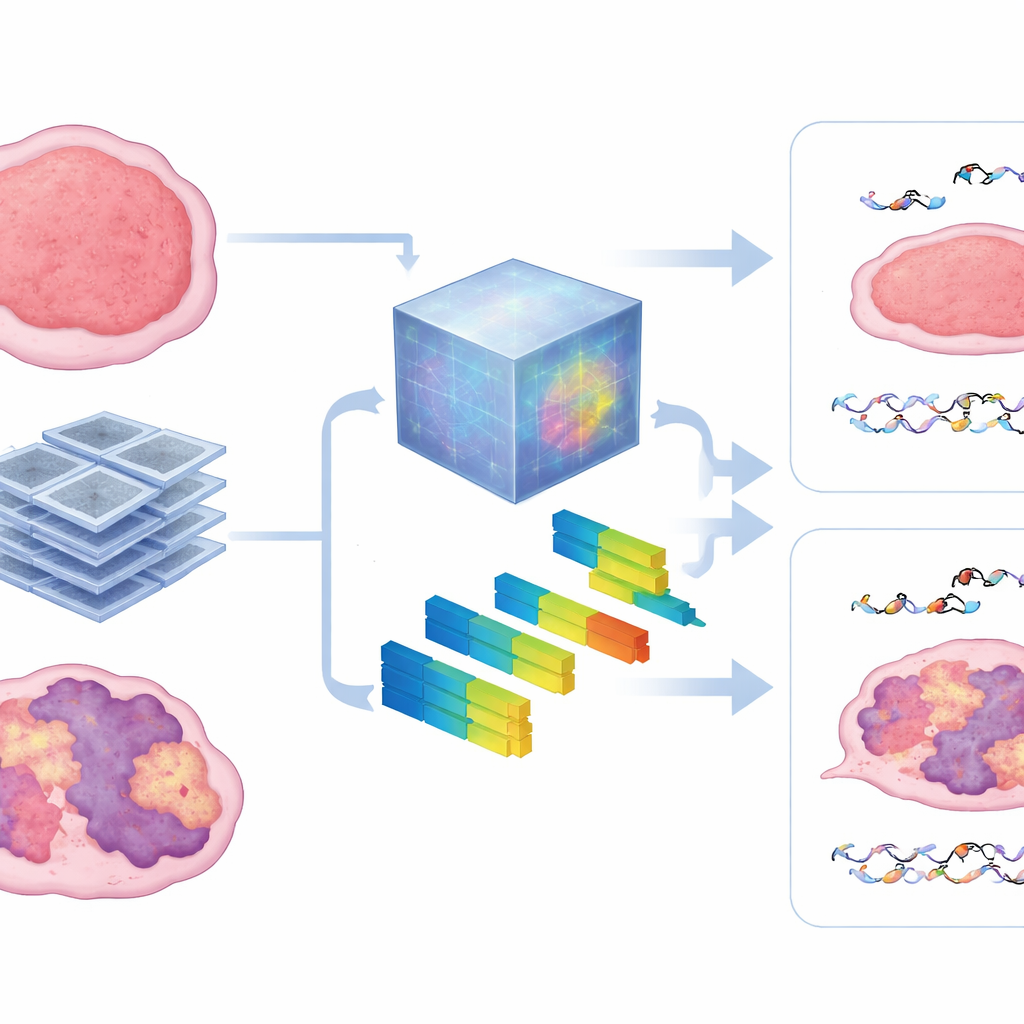
Cosa rivelano le scansioni all’interno del tumore
Per sbirciare dentro la “scatola nera”, gli autori hanno confrontato i pattern appresi dal modello di riferimento con caratteristiche radiomiche standard che descrivono texture e intensità dell’immagine. Hanno scoperto che il modello faceva ampio uso di misure di eterogeneità — quanto il tumore appariva maculato, grossolano o irregolare alla TC. I tumori con firme HRD più marcate tendevano a mostrare texture più disorganizzate, e queste stesse caratteristiche aiutavano a prevedere sia il danno microscopico al DNA sia il controllo macroscopico del tumore. L’approccio è rimasto robusto anche disponendo di meno dati di addestramento, suggerendo che modelli preaddestrati di questo tipo possono superare un ostacolo importante negli studi animali, dove raccogliere grandi dataset di imaging è difficile.
Dagli esperimenti sui topi alla futura cura dei pazienti
Questo lavoro preclinico mostra che una singola scansione TC, interpretata tramite una potente IA preaddestrata, può catturare segnali di riparazione del DNA difettosa e anticipare quanto intensamente un tumore risponderà a un farmaco che danneggia il DNA. Per un lettore non specialista, la conclusione è che scansioni dall’aspetto standard potrebbero presto svolgere una doppia funzione — localizzare un tumore e rivelarne la fragilità — senza procedure aggiuntive. Prima che ciò entri nella pratica clinica di routine, il metodo deve essere testato e validato su pazienti umani. Se tali sforzi avranno successo, le impronte digitali di HRD basate su TC potrebbero aiutare i medici ad abbinare le persone in modo più preciso a trattamenti come CP‑506 e terapie correlate, migliorando gli esiti e risparmiando ad altri terapie inefficaci e tossiche.
Citazione: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Parole chiave: carenza di ricombinazione omologa, imaging oncologico, radiomica, modelli di riferimento, terapia che danneggia il DNA