Clear Sky Science · it
Sviluppo e validazione di un modello basato sull’intelligenza artificiale per diagnosticare masse adnexali benigne, borderline e maligne
Perché questo conta per la salute delle donne
Le masse ovariche e altre lesioni adnexali sono reperti frequenti all’ecografia pelvica, ma stabilire quali siano innocue e quali indichino un cancro in fase precoce resta difficile, anche per gli esperti. Questo studio descrive un nuovo sistema di intelligenza artificiale (IA), chiamato Clinical‑OMTA, che interpreta le immagini ecografiche e aiuta i medici a classificare queste masse in tre gruppi fondamentali — benigne, borderline e maligne — così da garantire alle donne il trattamento adeguato evitando interventi chirurgici non necessari.
Tre tipi di lesioni, tre scelte molto diverse
Non tutte le masse adnexali sono uguali. Le lesioni benigne possono spesso essere sorvegliate o rimosse con interventi semplici. I tumori maligni sono neoplasie pericolose per la vita che richiedono chirurgia specialistica e chemioterapia. I tumori borderline stanno su una linea di confine: possono recidivare ma spesso colpiscono donne più giovani che desiderano preservare la fertilità, quindi i chirurghi cercano di asportare solo quanto strettamente necessario. Purtroppo, all’ecografia queste tre categorie possono apparire molto simili. In particolare i tumori borderline possono mimare sia una cisti innocua sia un carcinoma aggressivo, rendendo le decisioni terapeutiche fonte di stress per pazienti e clinici.
Trasformare scansioni complesse in risposte più chiare
L’ecografia è di norma il primo e più accessibile esame per le masse adnexali, ma interpretare immagini granulose e molto variabili richiede notevole esperienza. I sistemi di punteggio esistenti e i calcolatori di rischio, come il modello ADNEX ampiamente usato, combinano caratteristiche ecografiche specifiche con informazioni cliniche semplici come l’età e un marcatore ematico (CA125), tuttavia dipendono ancora dall’osservatore umano per descrivere correttamente le immagini. I recenti progressi nel deep learning — un ramo dell’IA che apprende pattern direttamente dai pixel — offrono la possibilità di ridurre parte di questa soggettività addestrando i computer a riconoscere sottili firme d’immagine associate ai diversi tipi tumorali.
Un assistente IA addestrato in molti ospedali
Partendo da lavori precedenti, gli autori hanno progettato Clinical‑OMTA, un modello IA a doppio percorso che prima separa le masse benigne da quelle non benigne e poi distingue le borderline dalle maligne. Il sistema elabora immagini ecografiche in scala di grigi e può anche accettare come input opzionali età e valori di CA125. Per addestrare e testare il modello, il team ha assemblato un ampio e diversificato dataset: 2381 donne provenienti da 23 ospedali in tutta la Cina, acquisite con 38 tipi di ecografi. La maggior parte dei casi aveva conferma diagnostica chirurgica; un gruppo più piccolo di cisti chiaramente benigne è stato confermato da almeno sei mesi di follow‑up ecografico. I dati sono stati suddivisi in set di addestramento, set di test interni e due coorti di test esterne completamente indipendenti, comprendenti sia immagini statiche sia brevi sweep video delle ovaie. 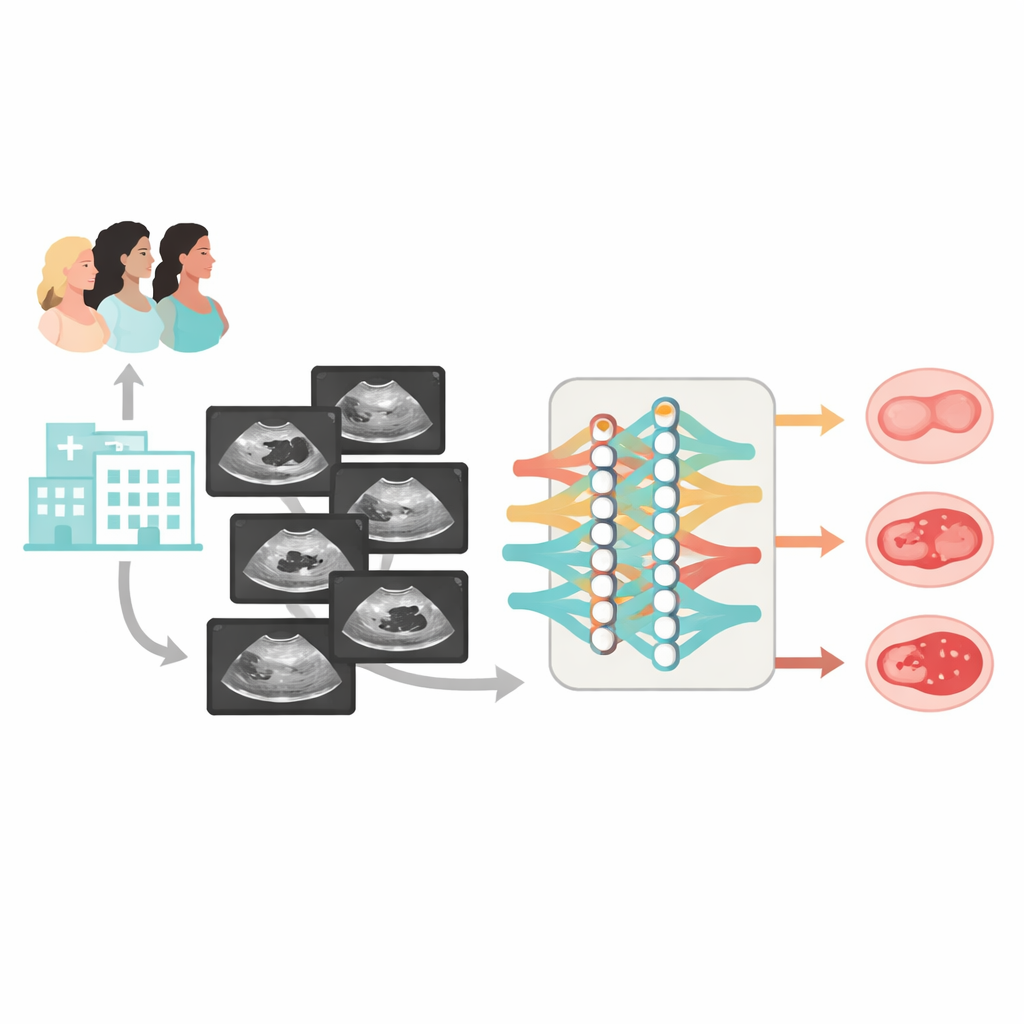
Quanto bene ha funzionato l’IA in contesti reali
Sulle immagini di test esterne, Clinical‑OMTA ha separato correttamente masse benigne, borderline e maligne con un’accuratezza simile sia al modello ADNEX sia al giudizio di un esaminatore ecografico esperto. La performance è risultata stabile tra diverse marche di ecografi, modalità di esame (transaddominale o transvaginale) e nei due ospedali esterni, suggerendo che il modello non è eccessivamente tarato su un singolo dispositivo o centro. Il sistema ha funzionato bene anche su clip video, non solo su fotogrammi statici. È interessante che l’inserimento di età e CA125 non abbia migliorato le decisioni rispetto all’uso delle sole immagini ecografiche, confermando studi precedenti che mostrano come questo marcatore ematico apporti poco quando sono disponibili immagini di alta qualità. 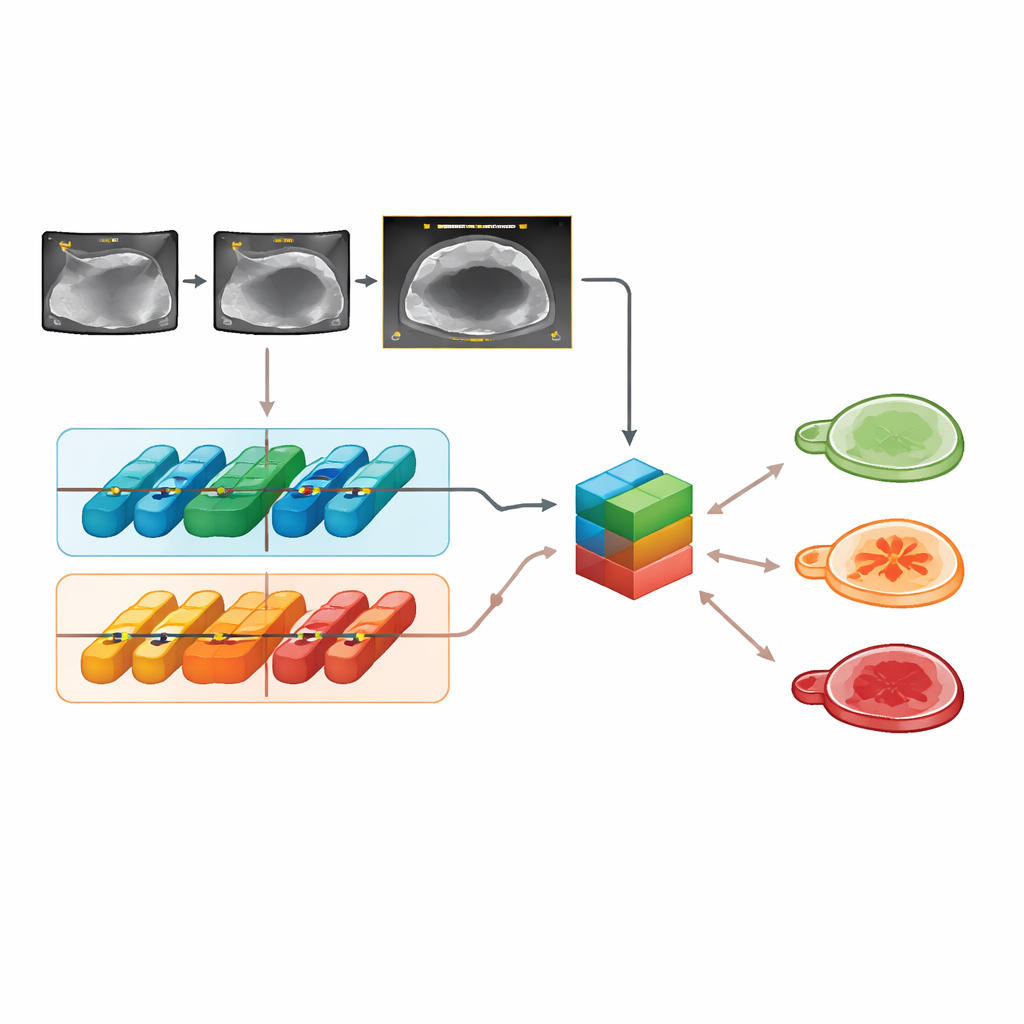
Aiutare i medici meno esperti, e i suoi limiti
I ricercatori hanno quindi chiesto a 11 radiologi — junior, intermedi e molto esperti — di classificare gli stessi casi, prima senza aiuti e poi con l’output dell’IA e sovrapposizioni a mappa di calore che evidenziano le regioni dell’immagine ritenute importanti dal modello. Con l’aiuto di Clinical‑OMTA, l’accuratezza dei medici junior è aumentata di circa 18–20 punti percentuali, e anche i lettori intermedi sono migliorati in modo marcato, raggiungendo performance vicine a quelle degli esperti. L’accordo tra i lettori, che prima era soltanto da discreto a moderato, è salito a livelli molto alti quando hanno utilizzato lo strumento. Allo stesso tempo, lo studio segnala che tale forte allineamento può riflettere un “bias di automazione”, per cui i clinici tendono a fare eccessivo affidamento sull’IA, specialmente nei casi borderline più ambigui. Gli autori quindi sottolineano che le mappe di calore sono strumenti di ricerca, non spiegazioni autonome, e che l’orientamento fornito dall’IA deve essere integrato con cura nella formazione clinica e nei processi decisionali.
Cosa significa per le pazienti
Nel complesso, Clinical‑OMTA dimostra che un sistema IA addestrato su dati ecografici diversificati può eguagliare la performance degli esperti nella classificazione delle masse adnexali in benigne, borderline e maligne, migliorando in modo sostanziale le competenze e la coerenza di radiologi meno esperti. Poiché funziona su diversi dispositivi e in contesti differenti, il modello potrebbe a lungo termine essere integrato negli ecografi o impiegato come software autonomo per supportare i medici in cliniche affollate o con risorse limitate. Gli autori avvertono che sono necessari ulteriori studi prospettici e internazionali prima dell’uso routinario, soprattutto in ambienti con apparecchiature di fascia bassa o operatori non specialisti. Ciononostante, il lavoro indica un futuro in cui un numero maggiore di donne, indipendentemente dal luogo di cura, potrà beneficiare di interpretazioni ecografiche ovariche a livello specialistico e di cure più mirate e tempestive.
Citazione: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Parole chiave: ecografia ovarica, intelligenza artificiale, masse adnexali, tumori ovarici borderline, supporto alle decisioni cliniche