Clear Sky Science · it
ACACA modula l’omeostasi degli R-loop per potenziare il metabolismo lipidico e le interazioni microambientali nel ccRCC
Perché questa storia sul cancro al rene è importante
Il carcinoma renale a cellule chiare è noto per essere sia comune sia difficile da trattare una volta che si diffonde. Uno dei suoi tratti distintivi è che le cellule tumorali diventano sorprendentemente ricche di lipidi, accumulando grassi e riorientando i loro meccanismi di approvvigionamento energetico. Questo studio pone una domanda inaspettata: come sono collegati i cambiamenti nei segnali di stress genomico di una cellula a questa trasformazione oleosa e al modo in cui i tumori comunicano con l’ambiente circostante? Seguendo un singolo enzima, ACACA, i ricercatori svelano un legame molecolare tra lo stress del genoma, il metabolismo lipidico alterato e il tessuto di supporto favorevole alla crescita che si forma intorno ai tumori renali.
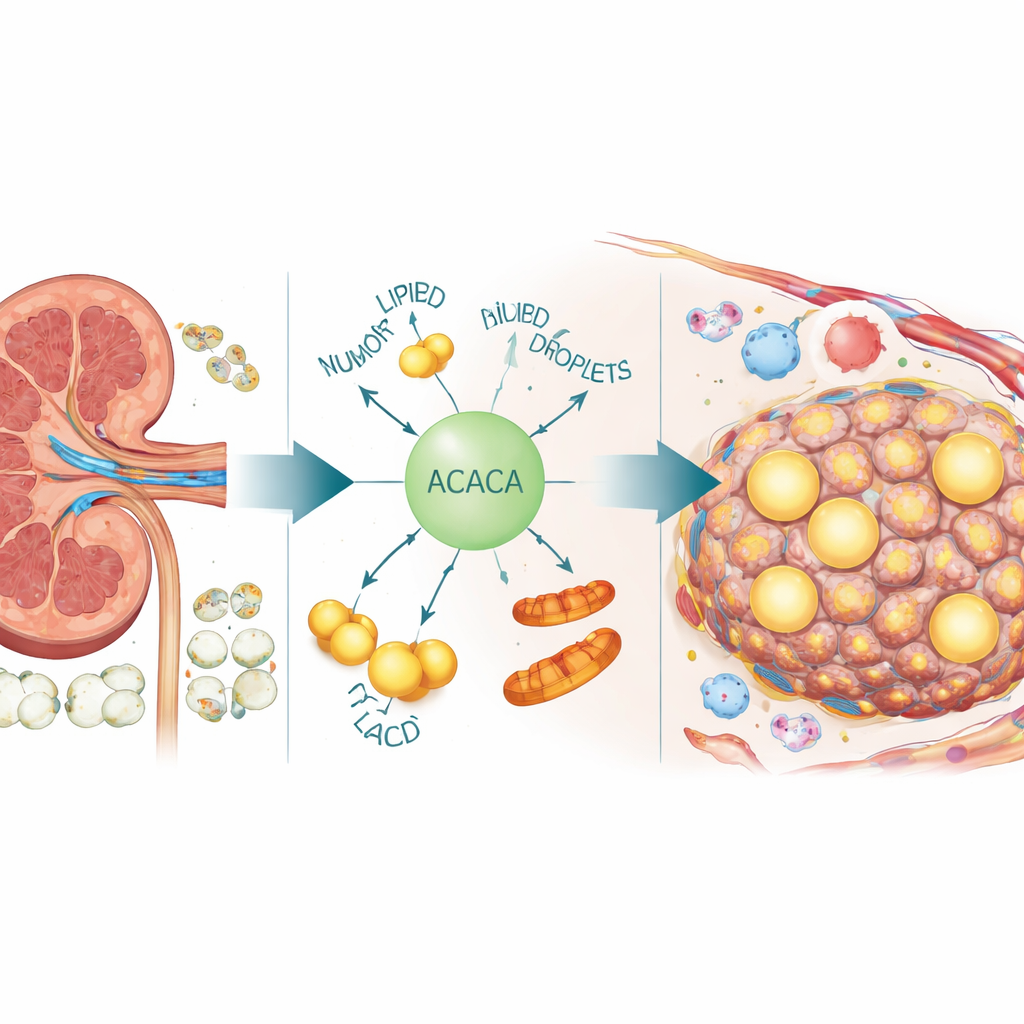
Nodi nascosti a tre fili nel DNA tumorale
All’interno delle nostre cellule, DNA e RNA possono formare brevemente strutture a tre fili chiamate R-loop durante il processo di lettura dei geni. In quantità moderate queste strutture aiutano a regolare il genoma, ma in eccesso possono bloccare la duplicazione del DNA e innescare danni. Usando grandi dataset pubblici di tumori renali e tessuto sano, il gruppo ha costruito un punteggio che riflette l’attività dei geni legati agli R-loop in ogni paziente. Hanno riscontrato che questa attività è chiaramente maggiore nei carcinomi renali a cellule chiare rispetto al tessuto renale normale e aumenta ulteriormente nei tumori avanzati e in quelli metastatici. I pazienti i cui tumori mostravano firme R-loop più pronunciate tendevano ad avere una sopravvivenza peggiore, suggerendo che il controllo alterato di queste strutture è associato a una malattia più aggressiva.
Un singolo enzima emerge dalla folla
Da oltre mille geni associati agli R-loop, i ricercatori hanno ristretto il campo a 44 che risultavano sia deregati nei tumori sia collegati agli esiti dei pazienti. Hanno quindi impiegato diversi modelli lineari di apprendimento automatico per vedere quale combinazione prediceva meglio la sopravvivenza. Attraverso metodi differenti e in coorti di pazienti indipendenti, un gene è emerso costantemente: ACACA, un enzima chiave che guida il primo passaggio impegnativo nella sintesi degli acidi grassi. Livelli elevati di ACACA hanno aiutato a identificare pazienti a rischio maggiore di recidiva o decesso. Quando il team ha combinato l’espressione di ACACA con informazioni cliniche standard—dimensione del tumore, diffusione e grado istologico—ha potuto costruire uno strumento di punteggio pratico che corrispondeva da vicino alla sopravvivenza reale dei pazienti nel corso di molti anni.
Un centro lipidico all’interno delle cellule maligne
Per capire dove si colloca ACACA nell’ecosistema tumorale, gli autori si sono rivolti alla trascrittomica a singola cellula e spaziale, tecnologie che misurano l’attività genica cellula per cellula e la ricollocano sui frammenti di tessuto. Queste analisi hanno mostrato che ACACA non è espresso in modo uniforme: è concentrato nelle cellule maligne, dove coincide con programmi attivi di divisione cellulare e segnali di danno e riparazione del DNA. Le cellule cancerose con alta espressione di ACACA apparivano come nodi di comunicazione, inviando e ricevendo numerosi segnali da cellule immunitarie e endoteliali vicine. Molti di questi segnali transitano attraverso vie correlate ai lipidi che coinvolgono molecole ANGPTL, note per coordinare la gestione dei lipidi con l’infiammazione e la crescita vascolare. Nelle sezioni di tessuto, le regioni ricche di ACACA si sovrapponevano ad aree tumorali dense piuttosto che al tessuto normale circostante.
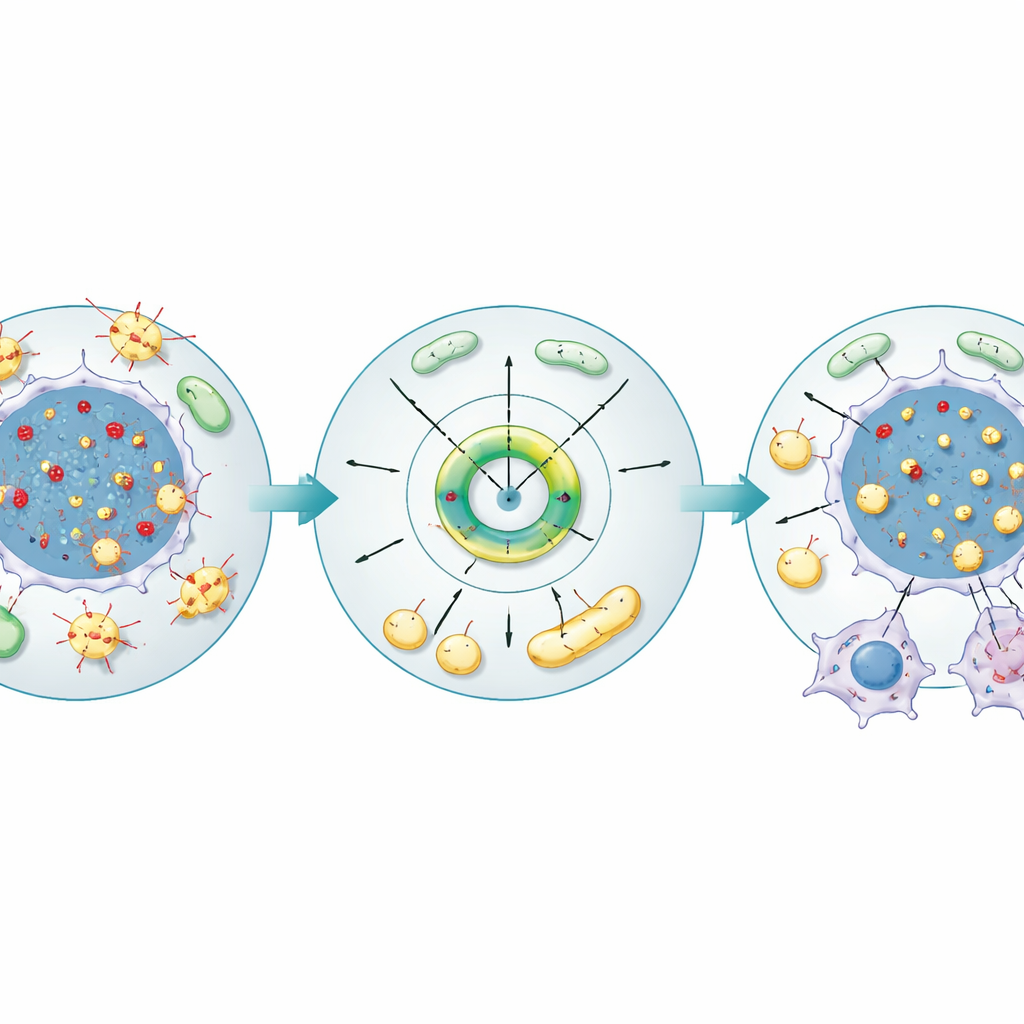
Dallo stress genetico all’approvvigionamento di carburante e alla crescita tumorale
Gli autori hanno quindi testato ACACA direttamente in linee cellulari di carcinoma renale e in tumori murini. Abbassare l’espressione di ACACA rallentava la crescita cellulare, riduceva la motilità e aumentava l’apoptosi, mentre aumentarla aveva l’effetto opposto. La microscopia ha mostrato che livelli bassi di ACACA portavano all’accumulo di R-loop e a un incremento dei segni di danno al DNA, mentre livelli elevati di ACACA riducevano queste strutture. Contemporaneamente, ACACA incrementava il numero di goccioline lipidiche all’interno delle cellule, elevava i livelli di acidi grassi e trigliceridi e migliorava la salute mitocondriale, valutata tramite un potenziale di membrana più forte, un maggior numero di mitocondri e livelli ridotti di specie reattive dell’ossigeno. Nei topi, bloccare ACACA in cellule di carcinoma renale impiantate limitava la crescita tumorale, aumentava i segnali di danno al DNA, diminuiva le riserve lipidiche e indeboliva la funzione mitocondriale, collegando l’enzima sia alla stabilità del genoma sia al bilancio energetico del tumore.
Che cosa significa per i trattamenti futuri
Nel complesso, lo studio descrive ACACA come un interruttore molecolare che aiuta i carcinomi renali a cellule chiare a sopravvivere sotto stress genomico rimodellando il metabolismo lipidico e rafforzando le interazioni con il microambiente circostante. Un’attività elevata degli R-loop segnala tumori più pericolosi, e ACACA emerge come un protagonista centrale che collega questo stress a cellule tumorali ricche di lipidi, energeticamente efficienti e più propense a crescere e diffondersi. Poiché ACACA è un enzima che in linea di principio può essere bersagliato farmacologicamente, questi risultati suggeriscono nuove strade per prevedere quali pazienti sono a maggior rischio e per progettare terapie che interrompano simultaneamente le strategie di protezione del genoma del tumore e le sue linee di vita metaboliche.
Citazione: Zhang, D., Chen, X., He, X. et al. ACACA modulates R-loop homeostasis to enhance lipid metabolism and microenvironmental interactions in ccRCC. npj Precis. Onc. 10, 102 (2026). https://doi.org/10.1038/s41698-026-01319-y
Parole chiave: carcinoma a cellule renali a cellule chiare, R-loop, ACACA, metabolismo lipidico, microambiente tumorale