Clear Sky Science · it
La delezione legata al cromosoma Y di EIF1AY determina differenze sessuali nel mieloma multiplo
Perché alcuni tumori del sangue colpiscono più duramente gli uomini
Il mieloma multiplo è un tumore delle cellule produttrici di anticorpi nel midollo osseo. Nel mondo, gli uomini sviluppano e muoiono per questa malattia più spesso delle donne, ma i motivi non erano chiari. Questo studio indaga un sospetto sorprendente: il cromosoma Y. Gli autori descrivono come la perdita di un singolo gene legato al cromosoma Y, chiamato EIF1AY, contribuisca a orientare l’ambiente immunitario negli uomini verso il sostegno della crescita tumorale, svelando un potenziale nuovo bersaglio per terapie più mirate.
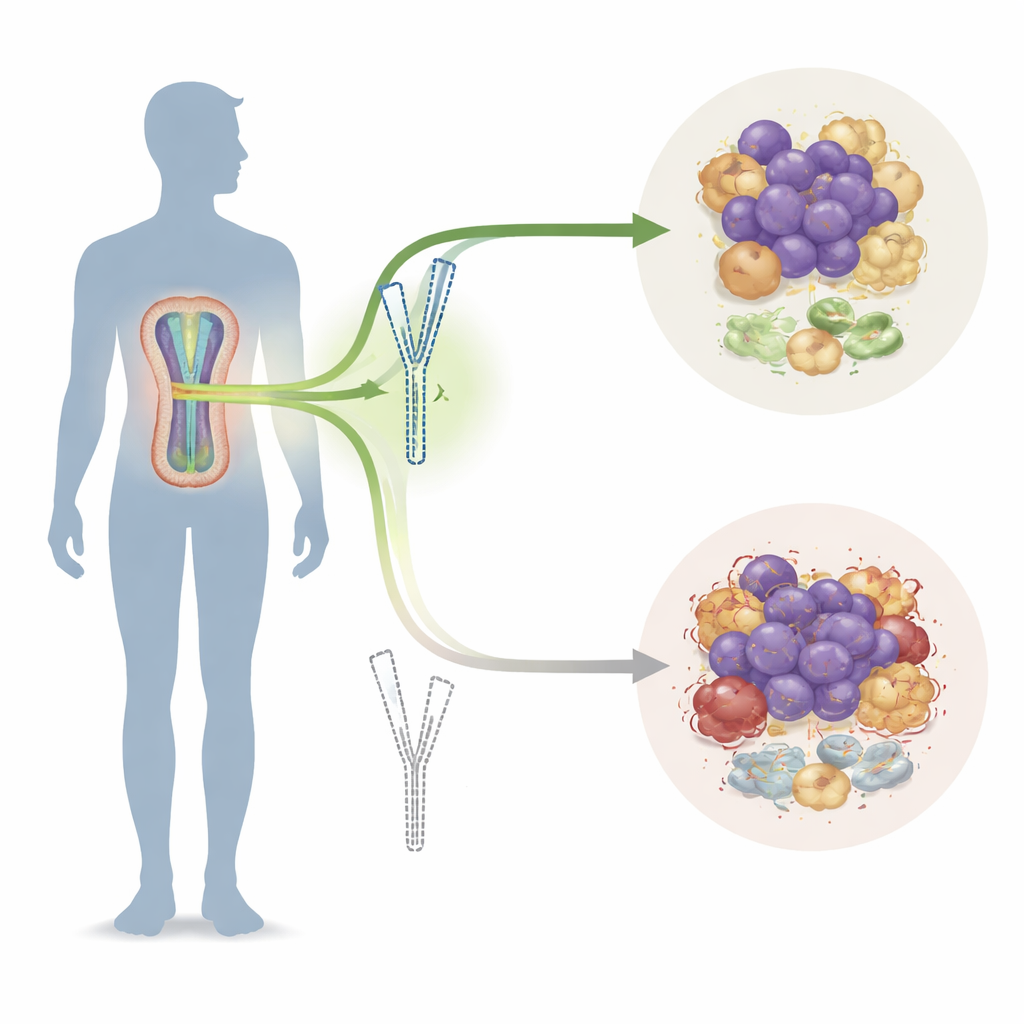
Un indizio legato al sesso nascosto nel DNA del tumore
I ricercatori hanno innanzitutto confermato che gli uomini con mieloma multiplo tendono ad avere esiti peggiori rispetto alle donne: maggiore incidenza, malattia più avanzata alla diagnosi e sopravvivenza più breve. Hanno poi esaminato grandi banche dati genetiche e cliniche per cercare geni che differissero tra pazienti maschi e femmine. Tra molti candidati, tre geni legati al cromosoma Y sono risultati più bassi negli uomini con malattia aggressiva, con EIF1AY che emergeva come il più forte predittore di cattivo esito. Nei campioni di sangue e midollo osseo dei pazienti maschi, EIF1AY era spesso parzialmente delezionato dal cromosoma Y, specialmente negli uomini più anziani e in quelli con mieloma in stadio avanzato e danni cromosomici complessi. I pazienti con livelli più bassi di EIF1AY avevano maggiore carico tumorale e risposte peggiori alla terapia, indicando che questo gene è un fattore protettivo chiave che alcuni tumori riescono a perdere.
Come le cellule immunitarie possono trasformarsi in aiutanti del cancro
Il gruppo ha quindi indagato come EIF1AY influenzi il microambiente tumorale, in particolare i macrofagi—cellule immunitarie che possono attaccare il cancro (stato “M1”) o sostenerlo (stato “M2”). Le analisi dei dataset dei pazienti hanno mostrato che i campioni di mieloma maschili erano più ricchi di macrofagi di tipo M2 rispetto a quelli femminili. Nei modelli di laboratorio, le cellule di mieloma ingegnerizzate per esprimere più EIF1AY crescevano più lentamente in coltura e nei topi. I macrofagi circostanti erano meno propensi ad assumere il programma M2 di supporto tumorale e venivano reclutati meno efficacemente nei tumori. Quando EIF1AY veniva ridotto o perso, si osservava l’effetto opposto: più macrofagi polarizzati M2 si accumulavano ai margini e all’interno della massa tumorale, e questi macrofagi condizionati a loro volta rilasciavano fattori che stimolavano la proliferazione delle cellule di mieloma. In sostanza, EIF1AY agiva come un freno su una partnership viziosa tra cellule tumorali e macrofagi.
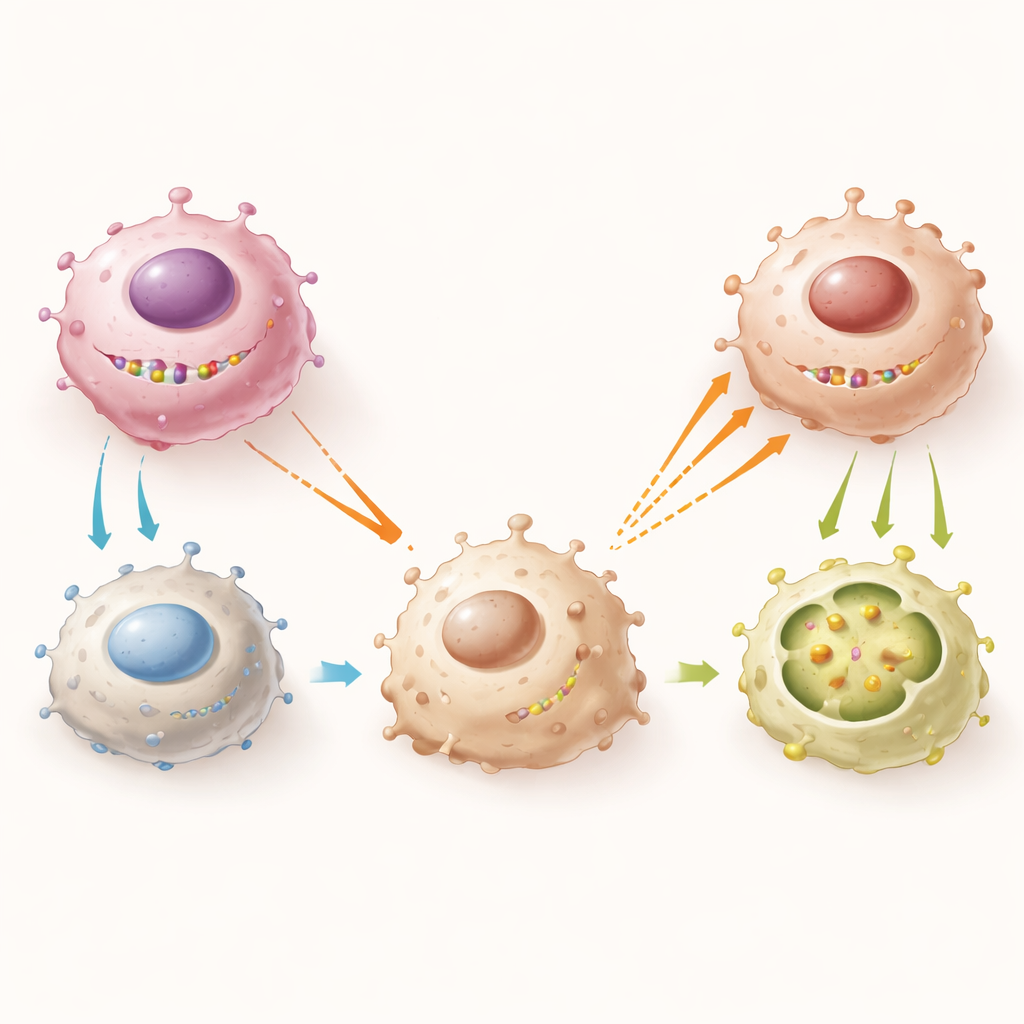
Una catena molecolare dal tumore al macrofago
Approfondendo, gli autori hanno mappato la catena molecolare che collega un gene sul cromosoma Y all’interno della cellula tumorale al comportamento delle cellule immunitarie vicine. EIF1AY si associa a un’altra proteina legata al cromosoma Y, RPS4Y1, per formare un complesso che lega fisicamente e stabilizza l’RNA messaggero di un recettore di superficie chiamato CD134 sulle cellule di mieloma. Quando EIF1AY e RPS4Y1 sono presenti, i livelli di CD134 rimangono più alti. Ciò impedisce alle cellule tumorali di rilasciare grandi quantità di due proteine di segnalazione, IL‑4 e IL‑13. Bassi livelli di IL‑4 e IL‑13 significano che i macrofagi esprimono meno un recettore sensibile al collagene chiamato DDR1, sono meno propensi a diventare di tipo M2 e sono meno attratti nel tumore. Quando EIF1AY viene delezionato, tutto questo asse collassa: i livelli di CD134 calano, IL‑4 e IL‑13 aumentano, DDR1 cresce sui macrofagi e un maggior numero di macrofagi M2 invade il tumore per nutrire la crescita cancerosa.
Collegare le versioni maschili e femminili della stessa salvaguardia
È interessante che le donne non possiedano EIF1AY o RPS4Y1, ma dispongono di geni strettamente correlati sul cromosoma X, EIF1AX e RPS4X. Lo studio ha rilevato che livelli elevati di questi omologhi legati all’X nelle pazienti con mieloma erano anch’essi associati a esiti migliori. Quando i ricercatori hanno sperimentalmente ridotto EIF1AX o RPS4X in linee cellulari di mieloma di derivazione femminile, le cellule crescevano più rapidamente, riproducendo ciò che accade nei maschi quando EIF1AY e RPS4Y1 sono persi. Questo suggerisce che entrambi i sessi possiedono una via protettiva simile, ma gli uomini sono particolarmente vulnerabili perché il cromosoma Y può essere parzialmente perso nelle cellule ematiche con l’età, rimuovendo del tutto EIF1AY e RPS4Y1, mentre i geni legati all’X nelle donne sono mantenuti in modo più stabile.
Cosa significa per i pazienti e le terapie future
In termini chiari, questo lavoro mostra che molti pazienti maschi con mieloma perdono un circuito protettivo che normalmente dice alle cellule tumorali di restare silenti e impedisce ai macrofagi vicini di trasformarsi in complici del cancro. Quando la via EIF1AY–RPS4Y1–CD134 è intatta, mantiene basse certe segnalazioni immunitarie, previene l’acquisizione da parte dei macrofagi di un’identità favorevole al tumore e rallenta la crescita del mieloma. Quando parti del cromosoma Y—e in particolare EIF1AY—vengono delezionate, quel freno viene rimosso, consentendo un circuito auto‑rinforzante di segnali infiammatori e macrofagi di supporto che accelera la malattia. Questi risultati aiutano a spiegare perché gli uomini hanno esiti peggiori rispetto alle donne nel mieloma multiplo e suggeriscono che valutare lo stato di EIF1AY, o ripristinare la sua via a valle, potrebbe guidare immunoterapie più personalizzate per i pazienti maschi.
Citazione: Feng, Z., Bai, J., Li, Y. et al. Y chromosome-linked EIF1AY deletion drives sex differences in multiple myeloma. npj Precis. Onc. 10, 131 (2026). https://doi.org/10.1038/s41698-026-01317-0
Parole chiave: mieloma multiplo, cromosoma Y, microambiente tumorale, polarizzazione dei macrofagi, differenze sessuali nel cancro