Clear Sky Science · it
Il livello successivo: potenziare i modelli fondamentali con apprendimento che preserva la struttura e guida l’attenzione per passare da patch locali a consapevolezza del contesto globale in patologia computazionale
Insegnare ai computer a leggere i vetrini tumorali
Quando un patologo esamina una biopsia tumorale al microscopio, non si limita a osservare singole cellule: valuta schemi, quartieri e il modo in cui tumore, cellule immunitarie e tessuto sano sono disposti insieme. I sistemi di intelligenza artificiale attuali per la patologia digitale sono molto bravi a riconoscere dettagli in piccole patch d’immagine, ma spesso perdono questa prospettiva più ampia. Questo studio presenta EAGLE-Net, un nuovo approccio di IA che aiuta i computer a interpretare i vetrini tumorali più come fanno gli esperti umani, prestando attenzione sia ai dettagli locali sia all’organizzazione generale del tessuto sul vetrino.

Perché la disposizione del tessuto tumorale conta
Un tumore è più di un ammasso di cellule cancerose. Vive in un quartiere affollato, pieno di vasi sanguigni, cellule immunitarie, tessuto connettivo e aree di cicatrizzazione o morte cellulare. Il modo in cui questi elementi sono disposti — le loro distanze, i confini e le mescolanze — può indicare quanto il cancro sia aggressivo e come un paziente potrebbe rispondere alle terapie. I sistemi di IA convenzionali in patologia solitamente suddividono l’immagine dell’intero vetrino in migliaia di piccole tessere e le analizzano quasi in isolamento. Poi cercano di stimare la diagnosi o l’esito del paziente aggregando le informazioni di tutte le tessere. Questa strategia spesso ignora come le tessere si relazionano spazialmente fra loro, indebolendo le predizioni e rendendo le mappe di attenzione dell’IA frammentate o difficili da interpretare.
Un nuovo modo per catturare il quadro più ampio
EAGLE-Net è progettato per colmare il divario tra dettaglio locale e struttura globale. Parte da potenti “modelli fondamentali” che già sanno come estrarre caratteristiche visive ricche da piccole patch di vetrino. Su queste basi aggiunge un nuovo modulo che codifica la posizione di ciascuna patch sul vetrino, preservando la geometria reale del tessuto invece di comprimerla in una griglia distorta. Utilizzando filtri multi-scala, EAGLE-Net apprende pattern che spaziano da minuscole variazioni a livello cellulare fino a strutture tissutali più ampie come i margini tumorali e lo stroma circostante. Poi impiega un meccanismo di attenzione — essenzialmente un modo per assegnare punteggi di importanza — per concentrarsi sulle patch e sui quartieri che sono più rilevanti per prevedere diagnosi o sopravvivenza.
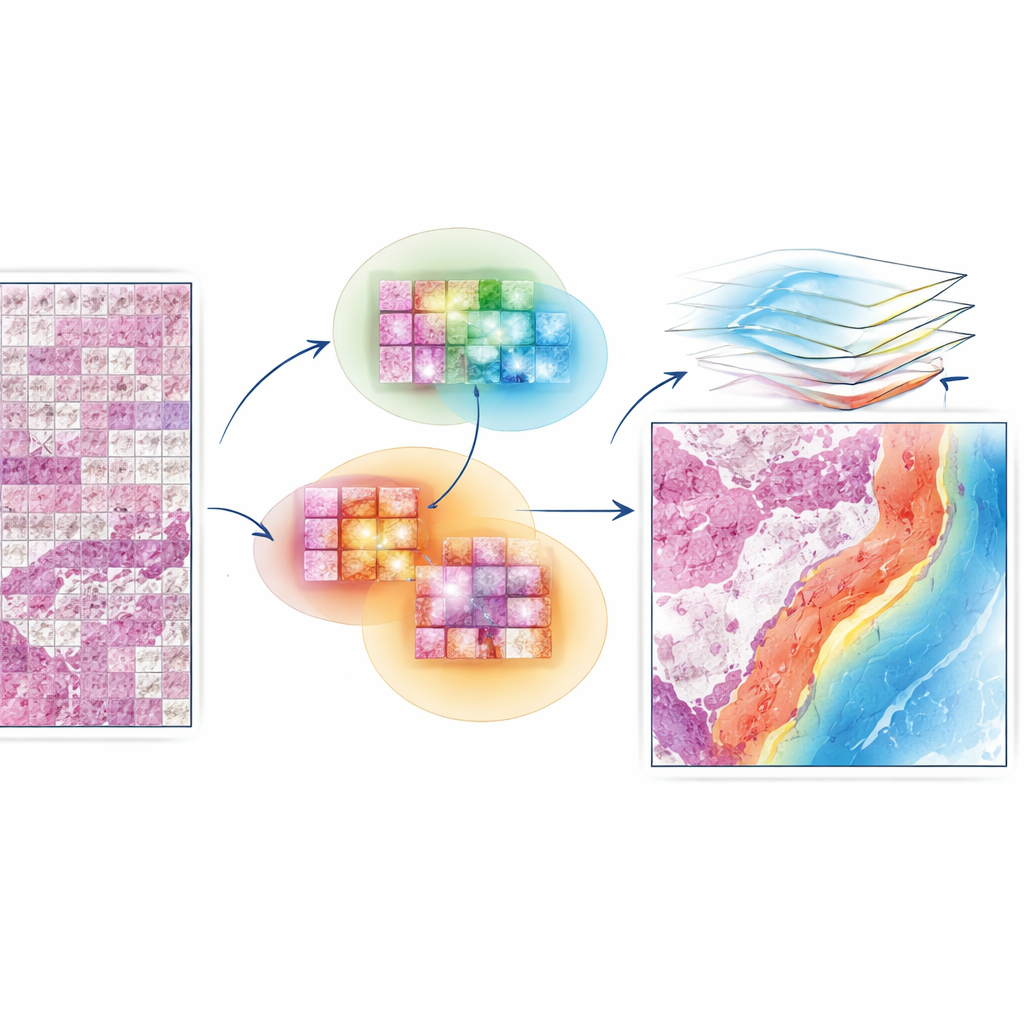
Lascare che il modello impari dai quartieri, non solo dai punti
Un’innovazione chiave di EAGLE-Net è il modo in cui insegna alla rete a valorizzare non solo le tessere più informative ma anche i loro vicini. Durante l’addestramento, il metodo identifica ripetutamente le tessere che il modello ritiene più rilevanti e poi lo incoraggia a considerare le tessere circostanti entro un piccolo raggio come parte della stessa regione significativa. Questo apprendimento “consapevole del quartiere” spinge il modello a formare regioni di attenzione lisce e contigue che si allineano con il modo in cui i patologi osservano fronti tumorali, cluster immunitari e altri microambienti. Allo stesso tempo, un termine aggiuntivo nel processo di training spinge attivamente il modello a ignorare lo sfondo o le aree vuote, riducendo il rischio di evidenziazioni false su artefatti o spazi bianchi.
Dimostrarne il valore su molti tipi di cancro
I ricercatori hanno testato EAGLE-Net su quasi 15.000 immagini di interi vetrini coprendo 10 diversi tumori, tra cui polmone, rene, stomaco, utero, tiroide, colon-retto e prostata. Hanno valutato due compiti principali: prevedere la durata di sopravvivenza dei pazienti e classificare tipi o gradi tumorali. Nella maggior parte delle coorti tumorali, EAGLE-Net ha eguagliato o superato diversi metodi basati sull’attenzione di punta, migliorando spesso i punteggi di predizione della sopravvivenza e l’accuratezza di classificazione di alcuni punti percentuali, un miglioramento che ha rilevanza su scala di popolazione. Ha inoltre mostrato buone prestazioni quando abbinato a tre modelli fondamentali di base molto diversi, dimostrando che il suo design è flessibile e non vincolato a un singolo estrattore di caratteristiche.
Vedere dentro il ragionamento del modello
Oltre alla precisione grezza, il team ha esaminato con attenzione dove EAGLE-Net «guardava» sui vetrini. Rispetto ad altri metodi, le sue mappe di attenzione formavano regioni più uniformi e coerenti che seguivano i confini tumorali e catturavano margini invasivi, tasche necrotiche e cluster di cellule immunitarie. Confronti quantitativi con maschere tumorali disegnate da esperti hanno mostrato che le regioni evidenziate da EAGLE-Net si sovrapponevano meglio al vero tumore, commettendo meno falsi positivi su tessuto normale e riproducendo più fedelmente forme tumorali complesse. Il modello ha inoltre dedicato una porzione maggiore della sua attenzione a compartimenti tumorali, necrotici e immunitari, e meno a polmone normale o vasi sanguigni, rispecchiando le priorità che un patologo adotterebbe nel giudicare la prognosi.
Cosa significa per la cura oncologica futura
In termini pratici, EAGLE-Net dimostra che aggiungere consapevolezza spaziale e ragionamento sui quartieri sopra le IA di patologia esistenti può migliorare sia le prestazioni sia l’interpretabilità. Invece di trattare un vetrino come una borsa di tessere disconnesse, il metodo impara a riconoscere nicchie biologicamente significative — margini tumorali, regioni ricche di cellule immunitarie e schemi di invasione — che contano per gli esiti dei pazienti. Poiché funziona con diversi modelli fondamentali e non richiede etichettature pixel-level dispendiose in termini di lavoro, EAGLE-Net potrebbe essere applicato su larga scala agli archivi digitali di vetrini. Con ulteriori validazioni e integrazione nei flussi clinici, tali sistemi potrebbero aiutare i patologi a stratificare i pazienti in modo più preciso, scoprire nuovi biomarcatori tissutali e, in ultima analisi, guidare terapie oncologiche più personalizzate.
Citazione: Waqas, M., Bandyopadhyay, R., Showkatian, E. et al. The next layer: augmenting foundation models with structure-preserving and attention-guided learning for local patches to global context awareness in computational pathology. npj Precis. Onc. 10, 109 (2026). https://doi.org/10.1038/s41698-026-01312-5
Parole chiave: patologia computazionale, prognosi del cancro, IA in patologia digitale, microambiente tumorale, EAGLE-Net